
21£®(6·Ö)½â£ºÔÚA³ØÖз¢ÉúµÄ·´Ó¦Îª£º
¡¡Ñô¼«(¢Ú¼«)£º4OH-- 4e£=2H2O+O2¡ü
¡¡Òõ¼«(¢Ù¼«)£º2Cu2++4e£=2Cu
¡¡ÈôCu2+ÍêÈ«·Åµçºó»¹ÓУº4H++4e£=2H2¡ü¡¡×ªÒƵç×ÓµÄÎïÖʵÄÁ¿Îª£º2.16¡Â108=0.02(mol)
¡¡Óɵ缫·´Ó¦¿ÉÖª£¬Ã¿×ªÒÆ4molµç×Ó£¬·Å³ö1molO2£¬ËùÒÔ¢Ú¼«ÉÏÎö³öO2µÄÌå»ýΪ£º¡¡0.02¡Â4¡Á22 .4=0.112(L)£¼0.224(L)
.4=0.112(L)£¼0.224(L)
¡¡ËµÃ÷A³ØÊÕ¼¯µ½µÄÆøÌåÖл¹ÓÐH2¡£¢Ù¼«ÉϷųöH2Ϊ£º0.224-0.112=0.112(L)£¬¼´0.005mol¡£
¡¡¢Ù¼«ÉÏÎö³öCuºÍ·Å³öH2¹²»ñµÃ0.02molµç×Ó¡£
¡¡Cu2+µÄÎïÖʵÄÁ¿Îª£º(0.02-0.005¡Á2)/2=0.005(mol)[Cu2+]= 0.005/0.2=0.025(mol/L)¡¡´ð£ºÍ¨µçÇ°A³ØÖÐÔ»ìºÏÈÜÒºCu2+µÄŨ¶ÈΪ0.025mol/L¡£
0.005/0.2=0.025(mol/L)¡¡´ð£ºÍ¨µçÇ°A³ØÖÐÔ»ìºÏÈÜÒºCu2+µÄŨ¶ÈΪ0.025mol/L¡£
20£®(11·Ö)
(1)ï®(1·Ö)¡¡ 4Li£4e£=4Li+(2·Ö)
(2)2SO Cl2+4e£=4Cl£+S+SO2(2·Ö)
Cl2+4e£=4Cl£+S+SO2(2·Ö)
(3)³öÏÖ°×Îí£¬Óд̼¤ÐÔÆøÌåÉú³É(2·Ö)¡¡ SOCl2+H2O=SO2¡ü+2HCl¡ü(2·Ö)
(4)ï®ÊÇ»îÆýðÊô£¬Ò×ÓëH2O¡¢O2·´Ó¦£»SOCl2Ò²¿ÉÓëË®·´Ó¦(2·Ö)
19.(11·Ö)
(1)¡¢Õý¼«(1·Ö)£¬Í(1·Ö)(2)¡¢3.85x103 C(3·Ö)4OH££4 e-£½O2¡ü+2H2O(2·Ö)£¬4Ag++4e-£½4Ag(2·Ö)£¬PH£½1(2·Ö)
e-£½O2¡ü+2H2O(2·Ö)£¬4Ag++4e-£½4Ag(2·Ö)£¬PH£½1(2·Ö)
18. (11·Ö)
(1)Ôµç³Ø(1·Ö)¡¡¡¡ µç½â³Ø(1·Ö)
(2)¸º(1·Ö)¡¡
Fe - 2e- == Fe2+ (2·Ö)¡¡¡¡¡¡ ¡¡¡¡ÎÞÉ«ÈÜÒº±äºìÉ«(2·Ö)
(2·Ö)¡¡¡¡¡¡ ¡¡¡¡ÎÞÉ«ÈÜÒº±äºìÉ«(2·Ö)
(3)¼õÉÙ¡¡ 5.6 (2·Ö)¡¡¡¡ ¼õÉÙ¡¡ 0.8(2·Ö)
16. (5·Ö)(1)¢Ü>¢Ú>¢Ù>¢Û(2·Ö)
(5·Ö)(1)¢Ü>¢Ú>¢Ù>¢Û(2·Ö)
(2)2N2H4(g) + 2NO2(g)£½3N2(g)+4H2O(g)£»¡÷H£½£1135.7kJ/mol(3·Ö)
1 7.(11·Ö)(1)¡¢¦¤H4= -339.2 kJ/mol(3·Ö)
7.(11·Ö)(1)¡¢¦¤H4= -339.2 kJ/mol(3·Ö)
(2)¡¢¸º¼«£ºCd£2e-+2OH£¡¡£½Cd(OH)2(2·Ö)
Õý¼«£º2NiO(OH)+2H2O+2e-£½2Ni(OH)2+2OH£(2·Ö)
Ñô¼«£º2Ni(OH)2+2OH££2e-£½2NiO(OH)+2H2O(2·Ö)
Òõ¼«£ºCd(OH)2+2e- £½Cd+2OH£¡¡(2·Ö)
21£®ÈçͼËùʾ£¬Í¨µç5 minºó£¬µÚ¢Û¼«ÔöÖØ2.16 g£¬Í¬Ê±ÔÚA³ØÖÐÊÕ¼¯µ½±ê×¼×´¿öϵÄÆøÌå224 mL£¬ÉèA³ØÖÐÔ»ìºÏÒºµÄÌå»ýΪ200 mL£¬ÇóͨµçÇ°A³ØÖÐÔ»ìºÏÈÜÒºCu2+µÄŨ¶È¡£
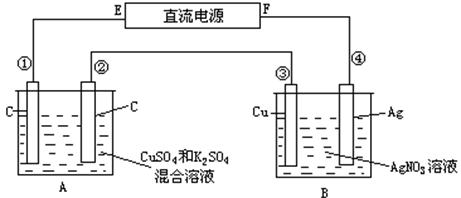
20£®Li-SOCl2µç³Ø¿ÉÓÃÓÚÐÄÔàÆð²«Æ÷¡£¸Ãµç³ØµÄµç¼«²ÄÁÏ·Ö±ðΪ﮺Í̼£¬µç½âÒºÊÇLiAlCl4-SOCl2¡£µç³ØµÄ×Ü·´Ó¦¿É±íʾΪ£º4Li+2SOCl2 =4LiCl+S +SO2¡£
Çë»Ø´ðÏÂÁÐÎÊÌ⣺
(1)µç³ØµÄ¸º¼«²ÄÁÏΪ¡¡¡¡¡¡¡¡¡¡¡¡ £¬·¢ÉúµÄµç¼«·´Ó¦Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(2)µç³ØÕý¼«·¢ÉúµÄµç¼«·´Ó¦Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(3)SOCl2Ò×»Ó·¢£¬ÊµÑéÊÒÖг£ÓÃNaOHÈÜÒºÎüÊÕSOCl2£¬ÓÐNa2SO3ºÍNaClÉú³É¡£ Èç¹û°ÑÉÙÁ¿Ë®µÎµ½SOCl2ÖУ¬ÊµÑéÏÖÏóÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ £¬·´Ó¦µÄ»¯Ñ§·½³ÌʽΪ¡¡¡¡¡¡¡¡¡¡¡¡ £»
(4)×é×°¸Ãµç³Ø±ØÐëÔÚÎÞË®¡¢ÎÞÑõµÄÌõ¼þϽøÐУ¬ÔÒòÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
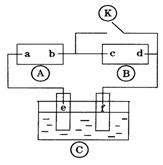
19£®ÏÂͼ ΪֱÁ÷µçÔ´£¬
ΪֱÁ÷µçÔ´£¬ Ϊ½þ͸±¥ºÍÂÈ»¯ÄÆÈÜÒººÍ·Ó̪ÊÔÒºµÄÂËÖ½£¬
Ϊ½þ͸±¥ºÍÂÈ»¯ÄÆÈÜÒººÍ·Ó̪ÊÔÒºµÄÂËÖ½£¬
 Ϊµç¶Æ²Û£®¶Ï¿ª
Ϊµç¶Æ²Û£®¶Ï¿ª £¬½Óͨµç·ºó·¢ÏÖ
£¬½Óͨµç·ºó·¢ÏÖ ÉϵÄcµãÏÔºìÉ«£®ÎªÊµÏÖÌúÉ϶ÆÍ£¬½Óͨ
ÉϵÄcµãÏÔºìÉ«£®ÎªÊµÏÖÌúÉ϶ÆÍ£¬½Óͨ ºó£¬Ê¹c¡¢dÁ½µã¶Ì·£®
ºó£¬Ê¹c¡¢dÁ½µã¶Ì·£®
(1)a¼«Îª¡¡¡¡¡¡ ¡¡e¼«Á¬½ÓµÄµç¼«²ÄÁÏΪ¡¡¡¡¡¡
(2)ÈôͨµçÒ»¶Îʱ¼äºó£¬ÌúÉÏÖÊÁ¿Ôö¼Ó1£®28g£¬ÔòµçÔ´ÌṩµÄµçÁ¿Îª¡¡¡¡ ¿âÂØ£¿( ÿ¸ö
ÿ¸ö µç×ÓËù´øµçÁ¿Îª1.6x10-19C£¬±£ÁôÁ½Î»Ð¡Êýµã)
µç×ÓËù´øµçÁ¿Îª1.6x10-19C£¬±£ÁôÁ½Î»Ð¡Êýµã)
 (3)Èô
(3)Èô ÖÐÁ½¼«ÎªÊ¯Ä«µç¼«£¬µç½âҺΪ400mlµÄAgNO3ÈÜÒº£¬Ôòe£¬fÁ½¼«µÄµç¼«·´Ó¦Ê½·Ö±ðΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡, ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
ÖÐÁ½¼«ÎªÊ¯Ä«µç¼«£¬µç½âҺΪ400mlµÄAgNO3ÈÜÒº£¬Ôòe£¬fÁ½¼«µÄµç¼«·´Ó¦Ê½·Ö±ðΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡, ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
ͨ¹ýºÍ(2)ÏàͬµÄµçÁ¿ºóÈÜÒºµÄPHΪ¡¡¡¡¡¡¡¡¡¡ (¼ÙÉèµç½âºóÈÜÒºÌå»ý²»±ä,PH= -lgc(H+) )
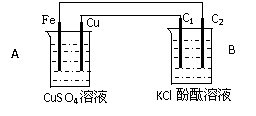
18£®°´ÓÒͼװÖýøÐÐʵÑ飬²¢»Ø´ðÏÂÁÐÎÊÌâ
¢ÅÅжÏ×°ÖõÄÃû³Æ£ºA³ØΪ___________
¡¡B³ØΪ___________
¢ÆÌú¼«Îª__________¼«£¬µç¼«·´Ó¦Ê½Îª___________
ʯī°ôC2¸½½ü·¢ÉúµÄʵÑéÏÖÏóΪ_________________
¢Çµ±C2¼«²úÉú2.24LÆøÌå(±ê׼״̬)ʱ£¬ÌúµÄÖÊÁ¿±ä»¯(Ôö¼Ó»ò¼õÉÙ)____ÁË ____g.CuSO4ÈÜÒºµÄÖÊÁ¿±ä»¯(Ôö¼Ó»ò¼õÉÙ)____ ÁË____g
17£®(1)¡¢ÒÑÖª¢ÙCO(g) + 1/2 O2(g) =CO2(g)¡¡¡¡ ¦¤H1= -283.0 kJ/mol
¢ÚH2(g) + 1/2 O2(g) = H2O(l)¡¡ ¡¡¦¤H2= -285.8 kJ/mol
¢ÛC2H5OH(l) + 3O2(g) = 2 CO2 (g) + 3H2O(l)¡¡¡¡ ¦¤H3=-1370 kJ/mol
ÊÔ¼ÆËã¢Ü2CO(g)+ 4H2(g)=
H2O(l)+C2H5OH(l) ¡¡¡¡µÄ¦¤H4¡¡¡¡¡¡¡¡
?
CO2 (g) + 3H2O(l)¡¡¡¡ ¦¤H3=-1370 kJ/mol
ÊÔ¼ÆËã¢Ü2CO(g)+ 4H2(g)=
H2O(l)+C2H5OH(l) ¡¡¡¡µÄ¦¤H4¡¡¡¡¡¡¡¡
?
(2)¡¢ÄøïÓ(Ni-Cd)¿É³äµçµç³ØÔÚÏÖ´úÉú»îÖÐÓй㷺ӦÓã¬Äøïӿɳäµçµç³ØÖеĵç½âÖÊÈÜҺΪKOHÈÜÒº£¬Cd(OH)2¡¢Ni(OH)2¡¢NiO(OH)¶¼ÄÑÈÜÓÚKOHÈÜÒº¡£ËüµÄ³ä·Åµç·´Ó¦°´ÏÂʽ½øÐУº

 Çë·Ö±ðд³ö¸Ãµç³ØÔڷŵ缰³äµçʱµÄµç¼«·´Ó¦Ê½¡£
Çë·Ö±ðд³ö¸Ãµç³ØÔڷŵ缰³äµçʱµÄµç¼«·´Ó¦Ê½¡£
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com