
1.(4分)完成方程式(反应体系内有4mol离子): HNO3+2H2SO4(100%)=___ _______+___ ______+___ ______
3.(5分)将5.6 g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入水中,还有 mL气体(S.T.P)不能溶解。(相对原子质量 H.1 N.14 O.16 Fe.56)
2.(5分)稠环芳香烃并m苯(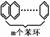 )的一氯取代物的同分异构体有______种;二氯取代物的同分异构体有______种。
)的一氯取代物的同分异构体有______种;二氯取代物的同分异构体有______种。
1.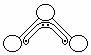 (5分)1994年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如右图,呈V型,键角116.5o,与SO2近似,三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个大π键--三个O原子均等地享有这4个电子。在1.01×105Pa,273OC时,O3在催化剂作用下能迅速转化为O2,当生成该状态下22.4L O2时,转移电子数 _________mol。
(5分)1994年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如右图,呈V型,键角116.5o,与SO2近似,三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个大π键--三个O原子均等地享有这4个电子。在1.01×105Pa,273OC时,O3在催化剂作用下能迅速转化为O2,当生成该状态下22.4L O2时,转移电子数 _________mol。
15.答案:设氢气的体积已折合为标准状况,则:氢气:0.0893mol;氯气:0.0705mol,氢气是过量的;80.0mL 9.00%NaOH溶液的质量为:88.0g;其中含NaOH的量:0.198mol;吸收HCl气体后尚剩余NaOH为:0.057mol;中和NaOH需要的H2SO4 0.0285mol(保留1位有效数字);需要0.100mol/L的H2SO4溶液的体积为:285mL(说明:计算步骤不同时,有效数字可能有差别,答280-290均可按正确答案论:此题主要目的是心理测试。)
14.答案;14-1、碳化钼,碳化钨。
14-2.Mo2C;WC。说明:每个钨原子的d轨道上平均多了4个电子,相当于Pt的电子结构,每个钼原子的d轨道上多了2个电子,相当于Ru原子的电子构型。
13.答案:见图A、B和C。说明:必须给出3种结构式,每个结构式3分,共计9分。双键的位置划错不给分。此题未给出催化氢化的温度,未涉及开环反应。若学生在应答时指出可能有开环反应而不会有四元环和三元环的结构式存在也应按正确论。
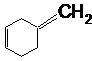 (A)
(A) 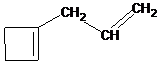 (B)
(B) 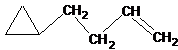 (C)
(C)
12.答案;12-1、 SOCl2+H2O=SO2+2HCl(说明:写成H2SO3也按正确答案论)
12-2向水解产物的水溶液加入硫化氢应得到硫磺沉淀。向另一份水解产物的水溶液加入硝酸银应得到白色沉淀。[说明:检出1种水解产物得1分。]
11.答案:11-1.从海底取出的甲烷水合物将融化并放出甲烷气体。因为该晶体是分子晶体。甲烷分子和水分子都是由有限数目的原子以共价键结合的小分于,水分子和甲烷分子之间范德华力,而水分子之间是范德华力和氢键。(2分)
11-2.假设甲烷气体体积是折合成标准状况下的数据,则1 m3水合物中有甲烷164m3÷22.4 m3kmol=7.32kmol;假设甲烷水合物固体中的水的密度为1g/cm3,则其中有水l m3×1000kg/m3÷18kg/mol=55.56 kmol;因此有:CH4︰H2O=7.32kmol︰55.6kmol≈1︰7.6。
[说明:甲烷水合物的组成可能是6CH4·46H2O;以上是最简单的参考答案,设密度为1g/cm3也可包含甲烷,只要答案为CH4·6-9H2O,均可按满分计。但设密度为0.9g/cm3又包含甲烷则不能认为是合理的(岂不会漂到海面上来?另外,必须给出解题时的假设,否则不能得满分。)]
10.答案:10-1、见下图
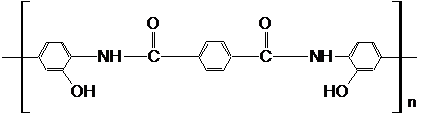
10-2、PHA高分子键的共轭较差,加热容易发生键的旋转,是柔性骨架,所以PHA具有热塑性,而PBO高分子键的代轭程度高,加热不容易发生键的旋转,所以PBO是热固性的。(2分)[注:只要能对高分子骨架的键的性质能作正确的描述,均可得分]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com