
25°¢(8∑÷)ƒ—»ÐµÁΩ‚÷ ‘⁄ÀƻГ∫÷–¥Ê‘⁄◊≈µÁ¿Î∆Ω∫‚°£‘⁄≥£Œ¬œ¬£¨»Ð“∫¿Ô∏˜¿Î◊”≈®∂»“‘À¸√«ªØ—ߺ∆¡ø ˝Œ™∑Ω¥Œµƒ≥Àª˝ «“ª∏ˆ≥£ ˝£¨Ω–»Ð∂»ª˝≥£ ˝ °£¿˝»Á£∫
°£¿˝»Á£∫ °£µ±»Ð“∫÷–∏˜¿Î◊”≈®∂»∑Ω¥Œµƒ≥Àª˝¥Û”⁄»Ð∂»ª˝ ±£¨‘Ú≤˙…˙≥¡µÌ£¨∑¥÷ÆπÃûÐΩ‚°£
°£µ±»Ð“∫÷–∏˜¿Î◊”≈®∂»∑Ω¥Œµƒ≥Àª˝¥Û”⁄»Ð∂»ª˝ ±£¨‘Ú≤˙…˙≥¡µÌ£¨∑¥÷ÆπÃûÐΩ‚°£
(1)ƒ≥ »Ð“∫¿Ô
»Ð“∫¿Ô £¨»Áπ˚…˙≥…
£¨»Áπ˚…˙≥… ≥¡µÌ£¨”¶µ˜’˚»Ð“∫pH£¨ π÷Æ¥Û”⁄________________°£
≥¡µÌ£¨”¶µ˜’˚»Ð“∫pH£¨ π÷Æ¥Û”⁄________________°£
(2)“™ π »Ð“∫÷–
»Ð“∫÷– ≥¡µÌΩœŒ™ÕÍ»´( π
≥¡µÌΩœŒ™ÕÍ»´( π ≈®∂»Ωµ÷¡‘≠¿¥µƒ«ß∑÷÷Æ“ª)‘Ú”¶œÚ»Ð“∫¿Ôº”NaOH»Ð“∫£¨ π»Ð“∫pH÷µŒ™___________°£
≈®∂»Ωµ÷¡‘≠¿¥µƒ«ß∑÷÷Æ“ª)‘Ú”¶œÚ»Ð“∫¿Ôº”NaOH»Ð“∫£¨ π»Ð“∫pH÷µŒ™___________°£
24°¢(9∑÷)(1)”–“ª∆ø±ª∆Ø∞◊π˝µƒ∆∑∫Ï ‘“∫£¨º◊Õ¨—ß»œŒ™ «±ªCl2∆Ø∞◊£¨““Õ¨—ß‘Ú»œŒ™ «±ªSO2∆Ø∞◊¡À£¨«Î”√ºÚµ•µƒ µ—È∑Ω∑®≈–∂œ≥ˆµΩµ◊ƒƒŒªÕ¨—ßµƒ≤¬≤‚ «’ʵƒ____________________________________°£
 (2)25°Ê ±£¨
(2)25°Ê ±£¨ µƒ¥◊À·»Ð“∫µƒpH‘ºŒ™3£¨œÚ∆‰÷–º”»Î¥◊À·ƒ∆æß㨵»æßûÐΩ‚∫Û∑¢œ÷»Ð“∫µƒpH‘ˆ¥Û°£∂‘…œ ˆœ÷œÛ”–¡Ω÷÷≤ªÕ¨µƒΩ‚ Õ£∫º◊Õ¨—ß»œŒ™¥◊À·ƒ∆ÀÆΩ‚≥ ºÓ–‘£¨
µƒ¥◊À·»Ð“∫µƒpH‘ºŒ™3£¨œÚ∆‰÷–º”»Î¥◊À·ƒ∆æß㨵»æßûÐΩ‚∫Û∑¢œ÷»Ð“∫µƒpH‘ˆ¥Û°£∂‘…œ ˆœ÷œÛ”–¡Ω÷÷≤ªÕ¨µƒΩ‚ Õ£∫º◊Õ¨—ß»œŒ™¥◊À·ƒ∆ÀÆΩ‚≥ ºÓ–‘£¨ ‘ˆ¥Û¡À£¨“Ú∂¯»Ð“∫µƒpH‘ˆ¥Û£ª““Õ¨—ß»œŒ™¥◊À·ƒ∆»Ð”⁄ÀƵÁ¿Î≥ˆ¥Û¡ø¥◊À·∏˘¿Î◊”£¨“÷÷∆¡À¥◊À·µƒµÁ¿Î£¨ π
‘ˆ¥Û¡À£¨“Ú∂¯»Ð“∫µƒpH‘ˆ¥Û£ª““Õ¨—ß»œŒ™¥◊À·ƒ∆»Ð”⁄ÀƵÁ¿Î≥ˆ¥Û¡ø¥◊À·∏˘¿Î◊”£¨“÷÷∆¡À¥◊À·µƒµÁ¿Î£¨ π ºı–°£¨“Ú¥À»Ð“∫µƒpH‘ˆ¥Û°£
ºı–°£¨“Ú¥À»Ð“∫µƒpH‘ˆ¥Û°£
¢ŸŒ™¡À—È÷§…œ ˆΩ‚ Õƒƒ÷÷’˝»∑£¨ºÃ–¯◊ˆ»Áœ¬ µ—È£∫œÚ µƒ¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øœ¬¡–ŒÔ÷ ÷–µƒ_______(ÃÓ–¥±ý∫≈)£¨»ª∫Û≤‚∂®»Ð“∫µƒpH°£
µƒ¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øœ¬¡–ŒÔ÷ ÷–µƒ_______(ÃÓ–¥±ý∫≈)£¨»ª∫Û≤‚∂®»Ð“∫µƒpH°£
°° A°¢πÃÃÂCH3COOK°°°°°° B°¢πÃÃÂCH3COONH4
°° C°¢∆¯ÃÂNH3°°°°°°°°°°°° D°¢πÃÃÂNaHCO3
¢⁄»Ùº◊Õ¨—ßµƒΩ‚ Õ’˝»∑£¨»Ð“∫µƒpH”¶_________£ª»Ù““Õ¨—ßΩ‚ Õ’˝»∑£¨»Ð“∫pHµƒ÷µ”¶_________ÃÓ(°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±)
23°¢(14∑÷)º◊°¢““°¢±˚°¢∂°∫ՌόÂ÷÷»Ð“∫£¨∑÷±”… °¢
°¢ °¢
°¢ °¢
°¢ °¢
°¢ ∫Õ
∫Õ °¢
°¢ °¢
°¢ °¢
°¢ °¢
°¢ ÷–µƒ“ª÷÷◊È≥…(¿Î◊”≤ª÷ÿ∏¥≥ˆœ÷)°£∆‰÷–»˝÷÷»Ð“∫ π◊œ…´ Ø»Ô ‘“∫±‰∫Ï£¨““»Ð“∫≥ ºÓ–‘£¨º◊∫Õ““∑¥”¶ø……˙≥…∞◊…´≥¡µÌ∫Õ∆¯Ã£¨∂°ø…∑÷±”κ◊°¢““°¢±˚∑¥”¶…˙≥…∞◊…´≥¡µÌ°£∏˘æð…œ ˆ ¬ µÕ∆∂œ…œ ˆ»Ð“∫÷–»Ð÷ µƒªØ—ß Ω°£
÷–µƒ“ª÷÷◊È≥…(¿Î◊”≤ª÷ÿ∏¥≥ˆœ÷)°£∆‰÷–»˝÷÷»Ð“∫ π◊œ…´ Ø»Ô ‘“∫±‰∫Ï£¨““»Ð“∫≥ ºÓ–‘£¨º◊∫Õ““∑¥”¶ø……˙≥…∞◊…´≥¡µÌ∫Õ∆¯Ã£¨∂°ø…∑÷±”κ◊°¢““°¢±˚∑¥”¶…˙≥…∞◊…´≥¡µÌ°£∏˘æð…œ ˆ ¬ µÕ∆∂œ…œ ˆ»Ð“∫÷–»Ð÷ µƒªØ—ß Ω°£
(1)º◊_____________ ““_____________ ±˚_____________
∂°_____________ ŒÏ_____________
(2)–¥≥ˆº◊°¢““∑¥”¶µƒ¿Î◊”∑Ω≥à Ω________________________________________°£
(3)”√¿Î◊”∑Ω≥Ã Ω±Ì æŒÏ»Ð“∫≥ À·–‘µƒ‘≠“Ú «____________________________°£
22°¢(10∑÷)‘⁄20L∫„»ðµƒ√б’»ð∆˜÷–£¨º”»Î3molSO3(g)∫Õ1mol—ı∆¯£¨‘⁄ƒ≥Œ¬∂»œ¬ π∆‰∑¥”¶£¨∑¥”¶÷¡4min ±£¨—ı∆¯µƒ≈®∂»Œ™0.06mol/L£¨µ±∑¥”¶µΩ8min ±£¨∑¥”¶µΩ¥Ô∆Ω∫‚°£
(1)0min-4minƒ⁄…˙≥…O2µƒ∆Ωæ˘ÀŸ¬
v(O2)=________________
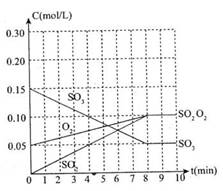 (2)’˚∏ˆπ˝≥Ã÷–£¨∏˜ŒÔ÷ µƒ≈®∂»”Î ±º‰πÿœµ»ÁÕºÀ˘ 棨‘Ú∏√Œ¬∂»œ¬µƒ∆Ω∫‚≥£ ˝
(2)’˚∏ˆπ˝≥Ã÷–£¨∏˜ŒÔ÷ µƒ≈®∂»”Î ±º‰πÿœµ»ÁÕºÀ˘ 棨‘Ú∏√Œ¬∂»œ¬µƒ∆Ω∫‚≥£ ˝
K=_____________________
(3)»Ù∆ º ±∞¥œ¬±Ì ˝æðÕ∂¡œ£¨œýÕ¨Œ¬∂»œ¬¥ÔµΩ∆Ω∫‚ ±£¨»˝—ıªØ¡Ú≈®∂»¥Û”⁄0.05mol/Lµƒ «__________£¨¥À ±µƒ∆Ω∫‚≥£ ˝”Î(2)–°Ã‚±»Ωœ_____________(ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±)
|
°° |
A |
B |
C |
D |
|
SO3 |
1mol |
3mol |
3mol |
0mol |
|
SO2 |
2mol |
1.5mol |
0mol |
6mol |
|
O2 |
2mol |
1mol |
0mol |
5mol |
(4)ŒÔ÷ µƒ≈®∂»≤ª‘Ÿ∏ƒ±‰±Í÷æ∏√∑¥”¶“—¥Ô∆Ω∫‚£¨œ¬¡–ªπø…“‘Àµ√˜∏√∑¥”¶“—¥Ô∆Ω∫‚µƒ «_____(ÃÓ–Ú∫≈)
¢ŸÃÂœµƒ⁄—π«ø≤ª‘Ÿ∏ƒ±‰
¢⁄»ð∆˜ƒ⁄∆¯Ãµƒ√Ð∂»≤ª‘Ÿ∏ƒ±‰
¢€ªÏ∫œ∆¯Ãµƒ∆Ωæ˘∑÷◊”¡ø≤ª‘Ÿ∏ƒ±‰
¢Ð
¢ð
21°¢(10∑÷)±Íøˆœ¬≥‰¬˙HClµƒ…’∆ø◊ˆÕÍ≈Á»™ µ—È∫Ûµ√µΩœ°—ŒÀ·£¨”√±Í◊ºÃºÀ·ƒ∆»Ð“∫µŒ∂®’‚÷÷—ŒÀ·≤‚∂®À¸µƒ◊º»∑≈®∂»£¨«Îƒ„ªÿ¥œ¬¡–Œ £∫
(1)”√±Í◊ºÃºÀ·ƒ∆»Ð“∫µŒ∂®’‚÷÷—ŒÀ· ±£¨ÃºÀ·ƒ∆»Ð“∫”¶◊∞‘⁄_________ ΩµŒ∂®πÐ÷–£¨»Ù”√º◊ª˘≥»◊˜÷∏ 溡£¨¥ÔµΩµŒ∂®÷’µ„ ±£¨»Ð“∫¥”________…´±‰≥…_________…´°£
(2)œ÷≈‰÷∆»˝÷÷≈®∂»µƒ±Í◊ºÃºÀ·ƒ∆»Ð“∫£¨ƒ„»œŒ™◊Ó∫œ µƒ «œ¬¡–µ⁄_______÷÷°£
°°°°°° ¢Ÿ2.500mol/L°°°°°° ¢⁄0.25mol/L°°°°°° ¢€0.025mol/L
(3)»Ù≤…”√…œ ˆ∫œ µƒ±Í◊ºÃºÀ·ƒ∆»Ð“∫µŒ∂®£¨”√c(Na2CO3)±Ì 棨µŒ∂® ± µ—È ˝æ𡖱̻Áœ¬£∫
|
µ—È¥Œ ˝±ý∫≈ |
¥˝≤‚—ŒÀ·Ãª˝(mL) |
µŒ»ÎúÀ·ƒ∆»Ð“∫ê˝(mL) |
|
1 |
20.00 |
18.80 |
|
2 |
20.00 |
16.95 |
|
3 |
20.00 |
17.05 |
«Û’‚÷÷¥˝≤‚œ°—ŒÀ·µƒŒÔ÷ µƒ¡ø≈®∂»(”√Â÷–À˘∏¯ ˝æð¡–≥ˆº∆À„ Ωº¥ø…)°£
c(HCl)=_____________________________________________°£
(4)»Ù ¢◊∞Na2CO3»Ð“∫µƒµŒ∂®πБ⁄µŒ∂®«∞Œ¥”√±Í◊º“∫»Ûœ¥£¨‘Ú◊Ó∫ÛÀ˘≤‚—ŒÀ·≈®∂»________£¨»ÙµŒ∂®Õͱœ∫Û∂¡ ˝ ±∏© ”£¨‘Ú µ—ÈŒÛ≤ÓŒ™________(“‘…œ¡Ωø’ÃÓ°∞∆´∏þ°±°¢°∞∆´µÕ°±ªÚ°∞ŒÞ”∞œÏ°±)
20°¢
 ƒ≥Ã˛µƒΩ·ππºÚ ΩŒ™£∫CH°° C-C°° CHCH2CH3£¨∏√∑÷◊”÷–∫¨”–Àƒ√ÊÃÂΩ·ππµƒÃº‘≠◊”
ƒ≥Ã˛µƒΩ·ππºÚ ΩŒ™£∫CH°° C-C°° CHCH2CH3£¨∏√∑÷◊”÷–∫¨”–Àƒ√ÊÃÂΩ·ππµƒÃº‘≠◊”
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° ©¶
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° C2H5
(º¥±•∫Õú‘≠◊”) ˝Œ™a£¨‘⁄Õ¨“ª÷±œþ…œµƒÃº‘≠◊” ˝◊Ó∂ýŒ™b£¨“ª∂®‘⁄Õ¨“ª∆Ω√ʃ⁄µƒÃº‘≠◊” ˝Œ™c£¨‘Úa°¢b°¢c∑÷±Œ™(°°°° )
A°¢4°¢3°¢5°°°° °°B°¢4°¢3°¢6°°°°°° C°¢2°¢5°¢4°°°°°° D°¢4°¢6°¢4
µ⁄IIæÌ(∑«—°‘Ò£¨π≤60∑÷)
19°¢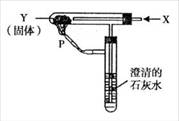 ∞¥”“Õº◊∞÷√≥÷–¯Õ®»Î∆¯ÃÂX£¨≤¢‘⁄πÐø⁄P¥¶µ„»º£¨ µ—ÈΩ·π˚ π≥Œ«Â ت“ÀƱ‰ªÎ◊«£¨‘ÚX°¢Yø…ƒÐ «(°°°° )
∞¥”“Õº◊∞÷√≥÷–¯Õ®»Î∆¯ÃÂX£¨≤¢‘⁄πÐø⁄P¥¶µ„»º£¨ µ—ÈΩ·π˚ π≥Œ«Â ت“ÀƱ‰ªÎ◊«£¨‘ÚX°¢Yø…ƒÐ «(°°°° )
¢Ÿ °°°° ¢⁄CO∫ÕNa2CO3
°°°° ¢⁄CO∫ÕNa2CO3
¢€CO∫ÕCuO°°°°°°°° ¢ÐH2∫ÕFe2O3
A°¢¢Ÿ¢Ð°°°°°° B°¢¢Ÿ¢€°°°°°° C°¢¢⁄¢€°°°°°° D°¢¢€¢Ð
18°¢ŒÔ÷ µƒ¡ø≈®∂»∏˜Œ™ µƒ
µƒ ∫Õ
∫Õ »Ð“∫µ»Ãª˝ªÏ∫œ∫Û£¨»Ð“∫≥ À·–‘°£œ¬¡–πÿœµ Ω’˝»∑µƒ «(°°°° )
»Ð“∫µ»Ãª˝ªÏ∫œ∫Û£¨»Ð“∫≥ À·–‘°£œ¬¡–πÿœµ Ω’˝»∑µƒ «(°°°° )
A°¢
B°¢
C°¢
D°¢
17°¢œ¬¡– µº ”¶”√”ΗŒµƒÀÆΩ‚÷™ ∂ŒÞπÿµƒ «(°°°°°° )
A°¢∫∏Ω” ±”√NH4Cl»Ð“∫≥˝–‚
B°¢ π”√≈ðƒ≠√ª∆˜ ±£¨ π¡ÚÀ·¬¡”α•∫Õ–°À’¥Ú»Ð“∫ªÏ∫œ
C°¢±•∫Õ¬»ªØÃ˙»Ð“∫µŒ»Î∑–ÀÆ÷–÷∆±∏Fe(OH)3Ω∫ÃÂ
D°¢…˙ªÓ÷–”√µÁΩ‚ ≥—ŒÀƵƒ∑Ω∑®÷∆»°œ˚∂æ“∫
16°¢”√pHæ˘Œ™2µƒ—ŒÀ·∫Õ¥◊À·»Ð“∫£¨∑÷±÷–∫Õµ»Ãª˝°¢µ»ŒÔ÷ µƒ¡ø≈®∂»µƒ«‚—ıªØ»Ð“∫£¨µ±«‚—ıªØƒ∆«°∫√±ªÕÍ»´÷–∫Õ ±£¨œ˚∫ƒ—ŒÀ·∫Õ¥◊À·»Ð“∫µƒÃª˝∑÷±Œ™V1∫ÕV2£¨‘ÚV1∫ÕV2µƒπÿœµ’˝»∑µƒ «(°°°° )
A°¢V1£æV2°°°°°° B°¢V1£ºV2°°°°°° C°¢V1=V2°°°°°° D°¢V1°ÐV2
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com