
2.有两种原子,一种原子核内有6个质子和6个中子,另一种原子核内有6个质子和7个中子,则这两种原子不相等的是( )
A.原子的带电量 B.原子的核电荷数
C.原子的质量大小 D.核外电子数
1.下列关于分子和原子的说法中,不正确的是( )
A.分子、原子都是构成物质的粒子 B.分子可分成原子,原子不能再分
C.原子可以再分为质子、中子、电子 D.分子是保持物质化学性质的最小粒子
17.已知碳12原子的质量为1。993×10-26kg,A原子的质量为5.146×10-26kg,若A原子核内质子数比中子数少一个,求:(1)A原子的相对原子质量;(2)A原子的核外电数
作业
16.填表:
|
原子种类 |
原子核 |
核外电子数 |
相对原子质量(取整数) |
||
|
核电荷数 |
质子数 |
中子数 |
|||
|
氢 |
1 |
|
|
|
1 |
|
磷 |
|
|
|
15 |
31 |
|
铁 |
26 |
|
30 |
|
|
|
硫 |
|
16 |
16 |
|
|
观察上表,我们可以得出:
(1)在原子中, = = ;
(2)在原子中, ≈ + ;
(3)不是所有的原子中都有 ,且 不一定等于 ;
(4)原子的种类由 决定。
15.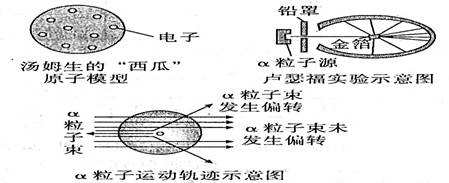 (烟台中考题)人们为揭示原子结构的奥秘,经历了漫长的探究过程。1897年汤姆生发现电子并提出类似“西瓜”的原子模型;1911年卢瑟福等人为探索电子的内部结构又进行了下面的实验:用一束带正电的、质量比电子大得多的高速运动的
(烟台中考题)人们为揭示原子结构的奥秘,经历了漫长的探究过程。1897年汤姆生发现电子并提出类似“西瓜”的原子模型;1911年卢瑟福等人为探索电子的内部结构又进行了下面的实验:用一束带正电的、质量比电子大得多的高速运动的 粒子轰击金箔,发现:①大多数
粒子轰击金箔,发现:①大多数 粒子能穿透金箔而不改变原来的的运动方向;②一小部分
粒子能穿透金箔而不改变原来的的运动方向;②一小部分 粒子改变了原来的运动方向;③有极少数
粒子改变了原来的运动方向;③有极少数 粒子被弹了回来。
粒子被弹了回来。
根据对原子结构的认识,分析出现上述现象的原因:
(1)现象① ;
(2)现象② ;
(3)现象③ ;
14.以相对原子质量为23的钠原子为例说明:
(1)构成原子的粒子有哪几种?
(2)以上各种粒子是怎样构成原子的
(3)整个原子显电性吗?为什么?
13.在①分子 ②原子 ③原子核 ④质子 ⑤中子 ⑥电子等粒子中,将符合下列条件的粒子的序号填在相应的横线上:
(1)在一定情况下,能保持物质的化学性质的粒子是 ;
(2)化学变化中的最小粒子是 ; (3)带正电荷的粒子是 ;
(4)能直接构成纯净物的是 ;
(5)构成分子的粒子是 ; (6)构成原子的粒子是 ;
(7)不显电性的粒子是 ;(8)带负电荷的,质量最小的粒子是 ;
(9)在同种原子中数目一定相等的是 ;
12.一种碳原子和镁原子的相对原子质量分别为12和24,则一个碳原子和一个镁原子的质量之比为 ( )
A.2∶1 B.1∶2 C.1∶24 D.24∶1
11.某原子的质子数为26,中子数比质子数多4,则该原子中所含微粒总数为( )
A.26 B.56 C.82 D.86
10.下列原子各1g,其中所含原子个数最少的是( )
A.氧原子 B.氧原子 C.碳原子 D.镁原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com