
5、中共七大召开的地点是( ) A.北平 B.南京 C.西安 D.延安
4、中共七大中毛泽东作的争取中国光明前途报告是( ) A.《论解放区战场》 B.《论联合政府》 C.《关于修改党的章程的报告》 D.《关于统一战线的报告》
2、日本帝国主义被迫宣布无条件投降是在( ) A.1945年8月15日 B.1945年9月2日 C.1945年9月9日 D.1945年10月 3、抗日战争取得胜利的最主要的因素是( ) A.中共的正确领导 B.国际反法西斯力量的协同作战 C.全民族的抗战 D.抗日战争的正义性
1、中共为争取抗战的最后胜利和实现中国光明前途做准备的会议是( ) A.中共一大 B.中共二大 C.中共七大 D.中共八大
30.(15分)金属是现代生活和工业生产中应用极为普遍的一类材料。
 (1)已知在相同的条件下,金属的活动性越强,金属和酸反应
(1)已知在相同的条件下,金属的活动性越强,金属和酸反应
产生气泡(氢气)的速度就越快。Al、Cu、Fe三种金属在稀
盐酸里的反应现象如右图所示。
①右图中Y所代表的金属是 (填“Cu”或“Fe”);
②Al、Cu、Fe三种金属的活动性由强到弱的顺序为 ;
③铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是
;
(2)金属的开发和利用是人类文明和社会进步的标志。
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800 ℃左右,即可得到与黄金外观相似的“药金”。
I.用上述方法不能制得真正的黄金(Au)是因为 ;
II.“药金”是 (填“纯金属”或“合金”);
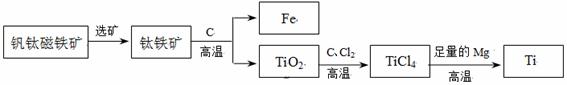 ②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”。由钒钛磁铁矿提取金属钛的主要工艺过程如下:
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”。由钒钛磁铁矿提取金属钛的主要工艺过程如下:
I.TiCl4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
。
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入_________________除去。
(3)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究。
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应。
①请完成证明金属粉末中存在Fe和Cu的实验设计:
|
实验操作 |
实验现象 |
结论 |
|
I.取少量的金属粉末于试管中,加入足量的 (填试剂名称)。 |
|
仅除去铝 |
|
II.将试管静置,弃去上层清液,加入足量的稀硫酸。 |
|
证明含有铁 |
|
III.将试管静置,弃去上层清液,加水,多次洗涤剩余固体 |
剩余固体呈紫红色 |
证明含有铜 |
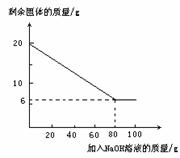 ②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与图象如下:
②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与图象如下:
|
加NaOH溶液的次数 |
第一次 |
第二次 |
第三次 |
… |
|
剩余固体的质量/g |
1 6.5 |
n |
9.5 |
… |
I.分析以上数据可知,上表中n的值为 ;
II.该金属粉末中Al的质量分数为 %
III.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
29.(7分)长途运输鱼苗时,常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
[提出问题]当把过氧化钙投入足量水中时,最终生成什么物质?
[进行猜想]甲同学:生成氧化钙和氧气; 乙同学:生成氢氧化钙和氧气。
同学和老师都认为甲同学的猜想是错误的,其理由是 ;
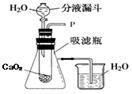 [实验探究]
[实验探究]
(1)打开右图装置中分液漏斗的活塞,控制滴加水速度,观察到
试管内有气泡产生。
① (填实验操作),
说明生成的气体是氧气。
②实验过程中,发现烧杯中有气泡出现,该现象说明 。
(2)请设计一个实验方案来验证过氧化钙和水反应产生的另一种物质是氢氧化钙:
|
实验步骤及操作方法 |
预期的实验现象 |
结论 |
|
①取少量过氧化钙放入试管中,加足量水,振荡, ② 。 |
①
产生气泡, ② 。 |
过氧化钙和水反应产生的另一种物质是氢氧化钙 |
[问题讨论]
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是 ;
(2)过氧化钙和水反应的化学方程式为 。
28.(7分)结合图示实验装置,回答下列问题。
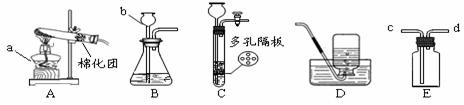
(1)图中a、b仪器的名称:a ,b 。
(2)用高锰酸钾固体制氧气,选用的发生装置是_________(填“A”、“B”或“C”),装入药品前应先 ;如用D装置收集O2,则气体收集完毕时,应先___
(填“从水中取出导气管”或“熄灭酒精灯”)。
(3)实验室制取二氧化碳时,如用E装置收集CO2,则气体应从______端通入(填“c”或“d”)。
(4)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是 (答出一点即可)。
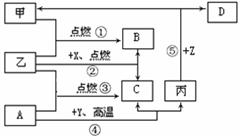
27.(5分)右图是初中化学中常见物质间的转化关系,
其中甲、乙为气态单质,丙为固态单质;A、B、C
均为氧化物,常温下B为液态。化合物D的水溶液
呈浅绿色。
(1)写出有关物质的化学式:A 、X ;
(2)指出反应④在生产实际中的应用: (举一例说明);
(3)将A、C两种氧化物区别开来,可使用的一种溶液为 (填名称);
(4)写出反应⑤的化学方程式: 。
26. (3分)找规律(用化学符号填空):
(3分)找规律(用化学符号填空):
(1)H2→ →O2→Fe3O4→Fe,
(2) →Cl2→NaClO→KClO3→HClO4;
(3)C2H4→C3H6→ →C5H10 。
25.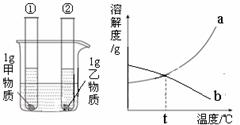 (4分)如图所示,烧杯中盛装20℃的水,试管①中盛装甲物质的溶液,试管②中盛装乙物质的溶液,且两试管中各有1g未溶解的固体(两支试管预先均经过充分振荡)。当两支试管中溶液的温度由20℃升到80℃时,发现试管①中甲固体消失,而试管②中的乙固体增加。
(4分)如图所示,烧杯中盛装20℃的水,试管①中盛装甲物质的溶液,试管②中盛装乙物质的溶液,且两试管中各有1g未溶解的固体(两支试管预先均经过充分振荡)。当两支试管中溶液的温度由20℃升到80℃时,发现试管①中甲固体消失,而试管②中的乙固体增加。
请你据此现象回答下列有关问题:
(1)80℃时,试管___________(填“①”或“②”)中溶液可能是不饱和溶液;
(2)上图能表示甲物质的溶解度曲线的是__________(选填“a” 或“b” );
(3)若将试管②从烧杯中取出冷却至20℃后,试管②中的固体质量为__________g;
(4)在温度_________时,乙物质的饱和溶液一定比甲物质的饱和溶液溶质质量分数大。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com