
29.(15分)化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为
。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的电子式为 ;Z分子的结构呈
②A的化学式是
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是 。
28.(16分)星形聚合物SPLA可经下列反应路线得到(部分反应条件未注明)。
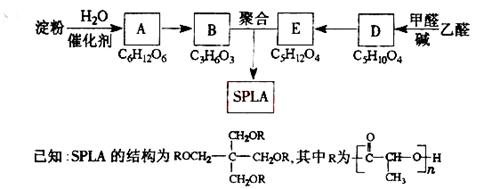
(1)淀粉是 糖(填“单”或“多”);A的名称是 。
(2)乙醛由不饱和烃制备的方法之一是 (用化学方程式表示,可多步)。
(3)D E的化学反应类型属于
反应;D结构中有3个相同的基团,且1molD能与2molAg(NH3)2OH反应,则D的结构简式是
;D与 溶液反应的化学方程式为
。
E的化学反应类型属于
反应;D结构中有3个相同的基团,且1molD能与2molAg(NH3)2OH反应,则D的结构简式是
;D与 溶液反应的化学方程式为
。
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO3溶液反应,又不能与新制Cu(OH)2反应,且1molG与足量Na反应生成1mol H2,则G的结构简式为 。
(5)B有多种脱水产物,其中两种产物的结构简式为 和 。
27.(15分)两个学习小组用题27图装置探究乙二酸(HOOC-COOH)受热分解的部分产物。
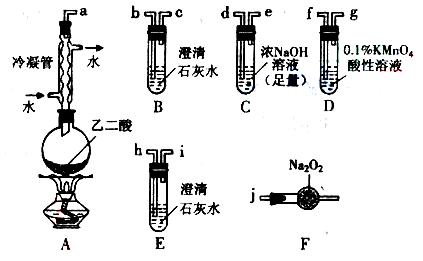
(1)甲组:
①按接口顺序:a-b-c-d-e-f-g-h连接装置进行实验。B中溶液变浑浊,证明分解产物有 ;装置C的作用是 ;E中溶液变浑浊,D中的现象是 ,证明分解产物有 。
②乙二酸受热分解的化学方程式为 。
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要反应的化学方程式为 。
②从A-F中选用装置进行实验,证明甲组通入D的气体能否与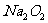 反应。
反应。
最简单的装置接口连接顺序是 ;实验后用F中的固体进行验证的方法是 (可另选试剂)。
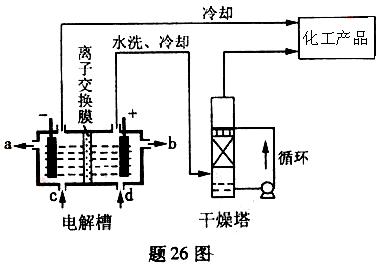
26.(14分)工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的液体是 。
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2 H2(g)+Si(s)⇌4 SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气  (标准状况)。
(标准状况)。
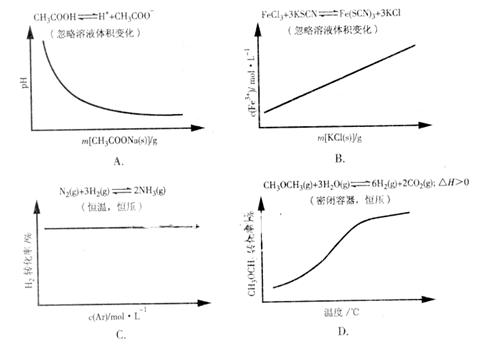
13.各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
12.下列热化学方程式数学正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g); ΔH=-1367.0kJ/mol(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l); ΔH=+57.3kJ/mol(中和热)
C.S(s)+O2(g)===SO2(g);ΔH=-269.8kJ/mol(反应热)
D.2NO2===O2+2NO; ΔH=+116.2kJ/mol(反应热)
11.下列对有机物结构或性质的描述,错误的是
A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
B.苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚弱
C.乙烷和丙烯的物质的量共1mol,完成燃烧生成3mol H2O
D.光照下2,2-二甲基丙烷与Br2反应其一溴取代物只有一种
10.物质的量浓度相同的下列溶液,pH由大到小排列正确的是
A.Ba(OH)2、Na2SO3、FeCl3、KCl
B. Na2SiO3、Na2SO3、KNO3、NH4Cl
C. NH3∙H2O、H3PO4、Na2SO4、H2SO4
D. NaHCO3、C6H5COOH、C2H5OH、HCl
9.下列叙述正确的是
A.SO2具有还原性,故可作漂白剂
B.Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg
C.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色
D.Fe在Cl2中燃烧生成FeCl2,故在与其他非金属反应的产物中的Fe也显+3价
8.下列各组离子,能在溶液中大量共存的是K+、Al3+、Cl-、SO2-4 、Mg2+、I-、NO-3 Na+、K+、CO2-3 、Cl- Na+、Fe3+、NO-3、SO2-4
A. Na+、Mg2+、AlO-2、Br- B. H+、Fe2+、SO2-4 、NO-3
C. K+、NH+4、CO2-3 、OH- D.Ca2+、Al3+、NO-3 、Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com