
6.若幂函数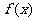 的图象经过点
的图象经过点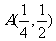 ,是它在A点处的切线方程为 ( )
,是它在A点处的切线方程为 ( )
A. B.
B.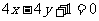
C.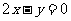 D.
D.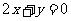 [来源:学.科.网Z.X.X.K]
[来源:学.科.网Z.X.X.K]
5.已知双曲线 的一个焦点与抛物线
的一个焦点与抛物线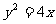 的焦点重合,且双曲线的离心率等于
的焦点重合,且双曲线的离心率等于 ,则该双曲线的方
,则该双曲线的方 程为 ( )
程为 ( )
A. B.
B.
C.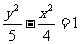 D.
D.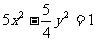
4.在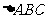 中,若
中,若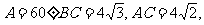 则角B的大小为 ( )
则角B的大小为 ( )
A.30° B.45° C.135°  D.45°或135°
D.45°或135°
3.等差数列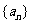 的前n项和
的前n项和 等于 ( )
等于 ( )
A.152 B.154 C.156 D.158
2.设 (i为虚数单位),则
(i为虚数单位),则 ( )
( )
A.-1-i B.-1+i C.1-i D.1+i
1.设集合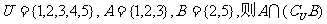 = ( )
= ( )
A.{1,3} B.{2} C.{2,3} D.{3}
30.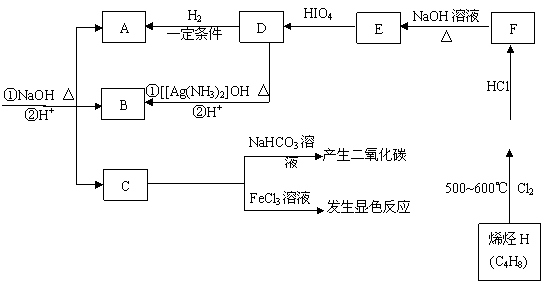 (16分).有机物X、A、B、C、D、E、F、G、H可以发生如下转化。其中C苯环上的一氯代物只有两种,烯烃H与HCl加成生成的产物有两种,D分子中所有的原子不可能均处在同一平面内。
(16分).有机物X、A、B、C、D、E、F、G、H可以发生如下转化。其中C苯环上的一氯代物只有两种,烯烃H与HCl加成生成的产物有两种,D分子中所有的原子不可能均处在同一平面内。
|
|||
|
|||
提示: +HIO4
+HIO4 R1CHO+R2CHO+HIO3+H2O
R1CHO+R2CHO+HIO3+H2O
回答下列问题:
(1)C中含氧官能团的名称____________________________;
(2)写出下列物质的结构简式:
D__________________________、X_________________________;
(3)写出下列化学反应方程式
①H G:______________________________________________________________;
G:______________________________________________________________;
②F E:______________________________________________________________;
E:______________________________________________________________;
(4)C的另一种同分异构体甲满足以下条件:
①属于芳香族化合物;②苯环上的一氯取代物只有一种;③与足量的NaOH溶液完全反应1 mol甲消耗3 mol NaOH。写出甲所有的结构简式:
。
29.(16分).A、B、C、 D、 E五种溶液分别是NaOH、 NH3·H2O、 CH3COOH 、HCl 、NH4HSO4
中一种。常温下进行下列实验:
①将1 L pH=3的A溶液分别与0.001mol·L-1 x LB溶液、0.001mol·L-1 y L D溶液充分反应后溶液呈中性,x、y大小关系为:y<x;
②浓度均为0.1mol·L-1A和E溶液,pH:A<E;
③浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是__________________溶液,判断理由是____________________________________
______________________________________________________________________。
(2)用水稀释0.1 mol·L-1B时,溶液中随着水量的增加而减小的是______________(填写序号)
① 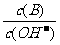 ;
②
;
② 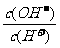 ;
;
③ c(H+)和c(OH-)的乘积 ④ OH-的物质的量
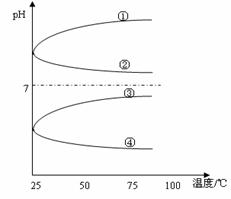 (3)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如下图中的_____________曲线(填写序号) 。
(3)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如下图中的_____________曲线(填写序号) 。
(4)OH-浓度相同的等体积的两份溶液A和E,分别和锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是________________(填写序号)
①反应所需要的时间E>A
②开始反应时的速率A>E
③参加反应的锌的物质的量A=E
④反应过程的平均速率 E>A
⑤A溶液里有锌剩余
⑥E溶液里有锌剩余
(5)室温下,向0.01mol·L-1C溶液中滴加0.01mol·L-1D溶液至中性得到的溶液中所有离子的物质的量浓度大小关系为____________________________________________。
28.(14分)aA、bB、cC、dD四种短周期元素,它们的原子序数有如下关系:c-b=b-a=1 且 b+c=d,B的最高价氧化物对应水化物为强酸。
(1)写出D的两种同素异形体的名称是 ;
(2)B与D形成的单质分别为甲、乙,下列判断正确的是 。
a.非金属性:D>B, 活泼性:甲>乙 b.非金属性:B>D,活泼性:甲>乙
c.非金属性:B>D,活泼性:乙>甲 d.非金属性:D>B,活泼性:乙>甲
(3)1993年7月,美国哈佛大学传出轰动性的科技新闻:利用激光溅射技术研制由A和B两种元素组成的新材料,而新材料硬度将超过目前世界上最硬的金刚石晶体,成为首屈一指的超硬新材料。该新材料的化学式为_______________;新材料晶体熔化时克服作用力为_____________;
(4)B的氢化物液态时可发生电离(电离方式与C的氢化物电离方式相似),加入金属钠能放出一种无色无味的可燃性气体,同时得到一种钠盐。写出常温下此钠盐与水作用的化学反应方程式 ;
(5)B和C分别形成的两种液态氢化物Q和S,且M(S)- M(Q)=2。1g Q与S恰好完全反应,产生无毒又不污染环境的物质X(g)和C的另一种液态氢化物W,放出的热量为20.1kJ,请写出该反应的热化学方程式 。
13.在2L固定密闭容器中,充入1molA气体和3molB气体,在温度为T℃下进行下列反应:
A(g) + 2B(g) 3C(g)
;△H<0,达到平衡时A转化率为50%。甲、乙两化学小组,控制温度为T℃,分别在2L固定密闭容器中充入一定量A气体和B气体。甲:2molA和6molB;乙:1molA和6molB。记录反应时容器内A的物质的量如下表所示:
3C(g)
;△H<0,达到平衡时A转化率为50%。甲、乙两化学小组,控制温度为T℃,分别在2L固定密闭容器中充入一定量A气体和B气体。甲:2molA和6molB;乙:1molA和6molB。记录反应时容器内A的物质的量如下表所示:
|
t/min |
甲组A的物质的量 |
乙组A的物质的量 |
|
0 |
2 |
1 |
|
5 |
1.0 |
0.5 |
下列说法正确的是( )
A.反应在第5min时,乙组中v(正)<v(逆)
B.反应在第5min时,甲组中3v(B正)=2v(C逆)
C.反应在第5min时,甲、乙两组均处于化学平衡状态
D.前5min中,甲组用A表示的化学反应速率为v(A)=0.2mol/(L ·min)
第II卷 (非选择题)
 27(14分).某化学小组利用浓盐酸和二氧化锰在加热条件下制取氯气,并利用氯气进行有关的探究实验,制取氯气的装置如图I和Ⅱ。
27(14分).某化学小组利用浓盐酸和二氧化锰在加热条件下制取氯气,并利用氯气进行有关的探究实验,制取氯气的装置如图I和Ⅱ。
(1)制取氯气反应的离子方程式_________________________________________;
(2)装置Ⅱ中小试管的作用为___________________________________________;
(3)装置I与装置Ⅱ比较,装置I的主要优点为:________________________________
__________________________________________________________________。
(4)将生成的氯气通入水中,可制得氯水,氯水见光易分解生成O2,请简述利用小烧瓶设计实验证明氯水见光分解有O2生成的实验方法:
________________________________ 。
(5)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能,请利用中学实验室常见试剂,设计实验,得出正确结论。
|
提出问题 |
收集资料 |
提出假设 |
验证假设 |
得出结论 |
|
氯水中何种物质能使湿润的红色布条褪色? |
①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 |
①______________ ________________。 ②________________ ________________。 ③_______________ ________________。 ④H2O使布条褪色 |
验证假设①:把红色干布条放入充满氯气的集气瓶,布条不褪色; 验证假设②:_______________________________________。 验证假设④:把红色布条放在水里,布条不褪色。 |
使红色布条褪色的物质是次氯酸。 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com