
4. 已知点P(3,2)与点Q(1,4)关于直线l对称,则直线l的方程为
A.x-y+1=0 B.x-y=0 C.x+y+1=0 D.x+y=0
3.已知向量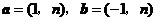 ,若
,若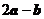 与
与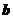 垂直,则
垂直,则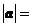
A.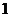 B.
B.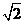 C.
C. D.4
D.4
2. 已知函数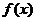 是定义在R上的奇函数,当
是定义在R上的奇函数,当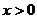 时,
时,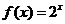 ,则
,则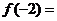
A. 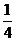 B.
B.
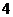 C.
C.
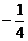 D.
D. 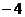
1.复平面内,复数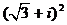 对应的点位于
对应的点位于
A.第一象限 B.第二象限 C.第三象限 D.第四象限
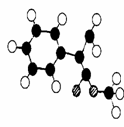
29.(18分)肉桂酸甲酯常用于调制具有草莓、葡萄、樱桃、香
子兰等香味的食用香精。它的分子中只含有1个苯环,苯环上只
有一个取代基。G为肉桂酸甲酯的一种同分异构体,其分子结构
模型如图所示(图中球与球之间的连线表示单键或双键)
用芳香烃A为原料合成G的路线如下:
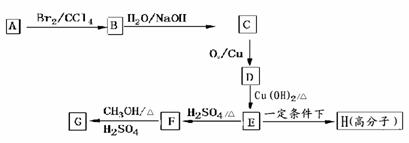
(1)写出肉桂酸的结构简式为 ;H结构简式为 。
(2)A分子中最多有 个碳原子共面。
(3)化合物E中的官能团有 (填名称)
(4)化合物D的名称是 (用系统命名法)
(5)E→F反应类型为 。
(6)书写下列化学反应方程式:
C→D
E→G
(7)其中E的同分异构体很多,其中有一类可用通式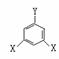 表示(其中X、Y均不为H)试写出符合上述通式且能发生银镜反应的结构简式。
表示(其中X、Y均不为H)试写出符合上述通式且能发生银镜反应的结构简式。
28.(14分)常温下用惰性电极电解200 mL 一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(以下气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
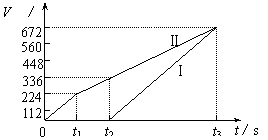 (1)0-t1时间段反应的离子方程式为 。
(1)0-t1时间段反应的离子方程式为 。
(2)t1-t2时间段阳极反应式 。
(3)通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度;
②t2时所得溶液的pH;
 (4)若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中的氯离子浓度的取值范围为 ,铜离子浓度的取值范围为
。
(4)若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中的氯离子浓度的取值范围为 ,铜离子浓度的取值范围为
。
27.(14分)某化学实验小组,通过Mg3N2固体水解生成氢氧化镁和氨气的反应制氨气,并进行氨气还原氧化铜的实验探究。如下图所示,给出了本实验可供选择的装置:
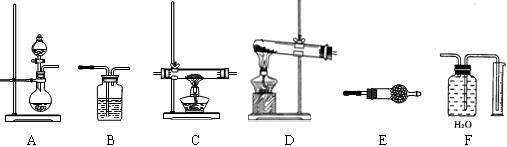
请回答下列问题:
⑴按该方法制氨气时,应选用上述装置中的 (填装置代码,下同)做氨气发生装置。
⑵为检验氨气还原氧化铜反应后生成Cu、H2O、N2,氨气发生装置后应依次连接 → C → → → (装置可重复使用)
⑶在C装置前后连接的装置中,填充的药品按前后顺序分别为 、 。
⑷有资料提出:CuO被还原时,当黑色固体完全变为红时,不一定完全转化为Cu,可能还含有Cu2O。已知查阅到一离子反应方程式:Cu2O+2H+=Cu2++Cu+H2O。依据该信息,若证明C处的红色固体中是否含有Cu2O ,请设计实验 。
⑸实验时充分加热,至C装置质量不再减轻为止。实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况)。则若用CO还原同样多CuO,理论上最少需要CO的体积为(标准状况,用含字母a的代数式表示) L。
26.(14分)现有A、B、C、D、E五瓶无色溶液,它们分别是:A1C13、BaCl2、NaHSO4、K2CO3、AgNO3溶液中的一种,已知A溶液显碱性,且A与E反应只有气体生成,B与C、C与D反应有沉淀生成,且沉淀为同一种物质,D与E反应也有沉淀生成。回答下列问题:
(1)C、D溶液中溶质的化学式分别是:C 、D 。
(2)A、E反应的离子方程式 。
(3)向B溶液中逐滴加入过量的稀氨水,用准确语言表述该反应过程的现象 。
(4)将0.1 mol/L的Ba(OH)2溶液与0.1 mol/L的E溶液按下表中甲、乙、丙三种不同体积比进行混合:
|
|
甲 |
乙 |
丙 |
|
V[Ba(OH)2]:
V(E) |
1:2 |
1:1 |
2:1 |
①按甲组比例混合,所得溶液呈 (填“酸”、“碱”、“中”)性。
②按乙组比例混合,溶液中发生反应的离子方程式为 。
③按丙组比例混合,所得溶液的pH为 。
13.M的名称是乙烯雌酚,它是一种激素类药物,结构简式如下。下列叙述不正确的是
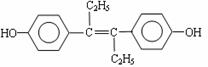 A.M的分子式为C18H20O2
A.M的分子式为C18H20O2
B.1 mol M最多能与7 mol H2发生加成反应
C.M能与NaOH溶液反应,不与NaHCO3溶液反应
D.1 mol M与饱和溴水混合,最多消耗7 mol Br2
12.一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH + 3O2 = 2 CO2 + 3H2O,电池构造如下图。下列关于该电池的说法正确的是
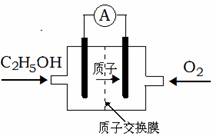
A.放电过程中,电源内部的H+从正极区向负极区迁移
B.通入乙醇的电极是负极
C.该电池的正极反应为: O2 + 4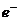 +2H2O= 4OH-
+2H2O= 4OH-
D.用该电池做电源,用惰性电极电解饱和NaCl的水溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com