
3.Ó̉ͼ·´Ó³ÁËÎ̉¹ú¹Å´úij̉»³¯´úµÄ¶¼³Ç²¼¾Ö£¬¸Ă²¼¾ÖµÄ³öÏÖÓ¦
¸Ă²»ÍíÓÚÏÂÁĐÄĸö³¯´ú£¿
¡¡ A.ºº³¯
¡¡ B.Ë峯
¡¡ C.Ëγ¯
¡¡ D.Ă÷³¯
2.ÀîԼɪ¶Ô¹Å´úÖĐ¹ú¿Æ¼¼×÷³öƠâÑùµÄÆÀ¼Û£º¡°ÔÚÖĐ¹úÍê³ÉµÄ·¢Ă÷ºÍ¼¼Êơ·¢ÏÖ£¬¸Ä±äÁËÎ÷·½ÎÄĂ÷µÄ·¢Ơ¹½ø³̀£¬²¢̣̉¶ø̉²È·¶¨¸Ä±äÁËƠû¸öÊÀ½çµÄ·¢Ơ¹½ø³̀¡£¡±̉ÔÏ¿É̉ÔÖ§³ÖƠẩ»¹ÛµăµÄÊÇ
¢Ù»đ̉©Íƶ¯ÁËÅ·Ö̃×Ú½̀¸Ä¸ï¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¢ÚÓ¡Ë¢ÊơΪÎÄ̉Ơ¸´ĐË×¼±¸ÁË̀ơ¼₫
 ¢ÛÖ¸ÄÏƠëʹµØÀí´ó·¢ÏÖ³ÉΪ¿ÉÄÜ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢ÜỐÖ½Êơ·½±ăÁËÖÇƠßѧÅɵÄÑĐ¾¿
¢ÛÖ¸ÄÏƠëʹµØÀí´ó·¢ÏÖ³ÉΪ¿ÉÄÜ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢ÜỐÖ½Êơ·½±ăÁËÖÇƠßѧÅɵÄÑĐ¾¿
 A. ¢Û¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡
B. ¢Ù¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡
C. ¢Ù¢Û¡¡¡¡¡¡¡¡¡¡
D. ¢Ú¢Û
A. ¢Û¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡
B. ¢Ù¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡
C. ¢Ù¢Û¡¡¡¡¡¡¡¡¡¡
D. ¢Ú¢Û
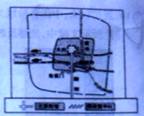
1.ÏÂͼËùʾÊÇËÄ·½¹ÅÓ¡ÎÄ£¬ÁªÏµÇس¯µÄÀúÊ·£¬Î̉ĂÇ¿É̉Եõ½µÄƠưÈ·½áÂÛÊÇ

¢ÙÇس¯´´Á¢»ÊµÛÖƶȡ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¢ÚÇس¯ÔÚÖĐÑëÉèÁ¢Ø©Ïà¡¢ÓùÊ·´ó·̣µÈÖ°¢ÛÇس¯Ôڵط½ÍÆĐĐ·Ö·âÖÆ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¢ÜÇس¯Í³̉»ÁËÎÄ×Ö
A.¢Ù¢Ú¢Û¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡B.¢Ú¢Û¢Ü
C.¢Ù¢Ú¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D.¢Ù¢Û¢Ü
15£®Ï±íÊư¾ƯÊÇÔÚij¸ßÎÂÏ£¬½đÊôĂ¾ºÍÄø·Ö±đÔÚÑơÆøÖĐ½øĐĐÑơ»¯·´Ó¦Ê±£¬ÔÚ½đÊô±íĂæÉú³ÉÑơ»¯±¡Ä¤µÄʵÑé¼Ç¼(±íÖĐaºÍb¾ùΪÓëζÈÓĐ¹ØµÄÊư¾Ư)£º
|
·´Ó¦Ê±¼ä t/h |
1 |
4 |
9 |
16 |
25 |
|
MgO²ăºñ y/nm |
0.05a |
0.20a |
o.45a |
0.80a |
1.25a |
|
NiO²ăºñy1/nm |
b |
2b |
3b |
4b |
5b |
¢Å ½đÊô¸ßÎÂÑơ»¯¸¯Ê´ËÙÂÊ¿É̉ÔÓĂ½đÊôÑơ»¯Ä¤µÄÉú³¤ËÙÂÊÀ´±íʾ£¬ÆäÀíÓÉÊÇ£º¡¡¡¡¡¡¡¡¡¡ £»
¢Æ ½đÊôÑơ»¯Ä¤µÄĤºñyºÍʱ¼ätËù³ÊÏֵĹØϵ£ºMgOÑơ»¯Ä¤ºñyÊô¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ĐÍ£¬NiOÑơ»¯Ä¤y1Êô¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ĐÍ(̀î¡°Ö±Ïß¡±£¬¡°Å×ÎïÏß¡±£¬¡°¶ÔÊư¡±»̣¡°Ë«ÇúÏß¡±µÈÀàĐÍ)¡£
¢Ç MgºÍNi±È½Ï£¬ÄÇ̉»ÖÖ½đÊô¾ßÓиüÁ¼ºĂµÄÄÍÑơ»¯¸¯Ê´ĐÔ£º¡¡¡¡ £¬ÆäÀíÓÉÊÇ£º¡¡¡¡¡¡ ¡£¡¡
14£®½«ÎïÖʵÄÁ¿ÏàµÈµÄA¡¢B»́ºÏÓÚ2LµÄĂܱƠÈƯÆ÷ÖĐ£¬·¢Éú·´Ó¦£º3A(g)+B(g)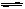 xC(g)+2D(g)£¬¾5minºó£¬²âµĂDµÄŨ¶ÈΪ0.5mol/L£¬c(A)¡Ăc(B)£½3¡Ă5£¬CµÄƽ¾ù·´Ó¦ËÙÂÊÊÇ0.1mol/(L¡¤min)£¬Ç󣺢Š´ËʱAµÄŨ¶È¼°·´Ó¦¿ªÊ¼Ç°·ÅÈëÈƯÆ÷ÖĐA¡¢BµÄÎïÖʵÄÁ¿£»¢Æ BµÄƽ¾ù·´Ó¦ËÙÂÊ£»¢Ç xµÄÖµÊǶàÉÙ£¿
xC(g)+2D(g)£¬¾5minºó£¬²âµĂDµÄŨ¶ÈΪ0.5mol/L£¬c(A)¡Ăc(B)£½3¡Ă5£¬CµÄƽ¾ù·´Ó¦ËÙÂÊÊÇ0.1mol/(L¡¤min)£¬Ç󣺢Š´ËʱAµÄŨ¶È¼°·´Ó¦¿ªÊ¼Ç°·ÅÈëÈƯÆ÷ÖĐA¡¢BµÄÎïÖʵÄÁ¿£»¢Æ BµÄƽ¾ù·´Ó¦ËÙÂÊ£»¢Ç xµÄÖµÊǶàÉÙ£¿
13£®È¡2g¸ÉÔïÂÁ·ÛºÍ3gµâ·ÛĐ¡ĐÄ»́ÔÈ£¬·ÖΪËĶѡ£Íù¸÷¶ÑÉÏ·Ö±đ¼Ó0.5gË®£¬1gĂ÷·¯£¬1gµ¨·¯£¬1gÎ̃Ë®Ạ́ËáÍ¡£¼ÓË®ÄǶѻ́ºÏÎïÊ×ÏÈĂ°»đ»¨£¬·¢Éú¾çÁ̉·´Ó¦£¬Æä´Î·¢Éú·´Ó¦µÄÊǼÓĂ÷·¯µÄÄÇ̉»¶Ñ»́ºÏÎÔٴη¢Éú·´Ó¦µÄÊǼӵ¨·¯µÄÄÇ̉»¶Ñ»́ºÏÎ¶ø¼ÓÎ̃Ë®Ạ́Ëá͵ÄÄǶÑ×îÄÑ·¢Éú·´Ó¦¡£
¢Å ÂÁºÍµâ·´Ó¦µÄ·½³̀ʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»ÂÁºÍµâ·´Ó¦»¹¿É̉Ô¿´µ½¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
¢Æ ËĶѻ́ºÏÎï·¢Éú·´Ó¦µÄÏȺó˳Đ̣˵Ă÷¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
12£®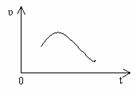 ÂÈËá¼ØºÍÑÇẠ́ËáÇâÄÆ·¢ÉúÑơ»¯»¹Ô·´Ó¦Éú³ÉCl(£1)ºÍS(+6)
ÂÈËá¼ØºÍÑÇẠ́ËáÇâÄÆ·¢ÉúÑơ»¯»¹Ô·´Ó¦Éú³ÉCl(£1)ºÍS(+6)
µÄ·´Ó¦ËÙÂÊÈçͼ4Ëùʾ£¬̉ÑÖªƠâ¸ö·´Ó¦ËÙÂÊËæ×ÅÈÜ̉ºÖĐc(H+)Ôö´ó¶ø¼Ó¿́¡£·´Ó¦¿ªÊ¼Ê±·´Ó¦ËÙÂʼӿ́µÄỘ̉ÊÇ__________________£»¡¡¡¡¡¡
·´Ó¦ºóÆÚ·´Ó¦ËÙÂÊϽµµÄỘ̉ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
11£®¶ÔÓÚ4FeS2+1O2 ==2Fe2O3+8SO2£¬ÊԻشđÓĐ¹ØµÄÎỀâ
¢Ù ³£Ñ¡ÓĂÄÄĐ©ÎïÖÊŨ¶ÈµÄ±ä»¯À´±íʾ¸Ă·´Ó¦µÄËÙÂÊ¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡ £»
¢Ú µ±Éú³ÉSO2µÄËÙÂÊΪ4mol/(L¡¤S)£¬ỘO2¼ơÉÙµÄËÙÂÊÊÇ¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡ £»
¢Û ²âµĂ4Sºó£¬O2µÄŨ¶ÈΪ2.8mol/L£¬Ộ¿ªÊ¼Ê±O2µÄŨ¶ÈΪ¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡ £»
¢Ü ΪÁË̀á¸ßÉú³ÉSO2µÄËÙÂÊ£¬¿É̉Ô²ÉÈ¡µÄ´ëÊ©ÊÇ
A£®Ôö¼ÓFeS2µÄÁ¿¡¡¡¡¡¡ B£®Ôö´óO2µÄŨ¶È¡¡¡¡ C£® Éư¸ßζȡ¡¡¡ D£®¼ơĐ¡Ñ¹Ç¿
9£®100mL6mol/LẠ́ËáÈÜ̉ºÓë¹ưÁ¿Đ¿·Û·´Ó¦£¬ÔÚ̉»¶¨Î¶ÈÏ£¬ÎªÁ˼ơ»º·´Ó¦½øĐеÄËÙÂÊ£¬µ«ÓÖ²»ÄÜÓ°ḮÉú³ÉÇâÆøµÄ×ÜÁ¿£¬¿ÉỊ̈·´Ó¦ÎïÖĐ¼ÓÈëÊÊÁ¿µÄ
A£®̀¼ËáÄÆ¡¡¡¡¡¡¡¡¡¡ B£®Ë®¡¡¡¡ ¡¡¡¡¡¡C£®Ạ́Ëá¼ØÈÜ̉º¡¡¡¡¡¡¡¡¡¡ D£®ÏơËá¼ØÈÜ̉º
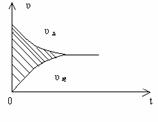 ¡¡
10£®ÈƯ»ư¹̀¶¨µÄ2LĂܱƠÈƯÆ÷ÖĐ½øĐеÄij̉»¿ÉÄæ·´Ó¦
¡¡
10£®ÈƯ»ư¹̀¶¨µÄ2LĂܱƠÈƯÆ÷ÖĐ½øĐеÄij̉»¿ÉÄæ·´Ó¦
A(g)+2B(g)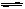 2C(g)£¬̉ÔBµÄÎïÖʵÄÁ¿Å¨¶È¸Ä±ä±íʾµÄ·´Ó¦
2C(g)£¬̉ÔBµÄÎïÖʵÄÁ¿Å¨¶È¸Ä±ä±íʾµÄ·´Ó¦
ËÙ¶Èv(Ơư)£¬v(Äæ)Óëʱ¼äµÄ¹ØϵͼÈçËùʾ¡£̉ÑÖª·´Ó¦ËÙÂÊvµÄ¡¡¡¡¡¡
µ¥Î»Îªmol¡¤L£1¡¤s£1£¬ỘͼÖĐ̉ơÓ°²¿·ÖµÄĂæ»ư¿É±íʾ
A£®AµÄÎïÖʵÄÁ¿Å¨¶ÈµÄ¼ơÉÙ¡¡ B£®BµÄÎïÖʵÄÁ¿Å¨¶ÈµÄ¼ơÉÙ
C£®CµÄÎïÖʵÄÁ¿Ôö¼Ó¡¡¡¡¡¡¡¡ D£®BµÄÎïÖʵÄÁ¿¼ơÉÙ
8£®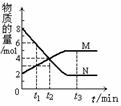 ÔÚ̉»¶¨Î¶ÈÏ£¬ÈƯÆ÷ÄÚij̉»·´Ó¦ÖĐM¡¢NµÄÎïÖʵÄÁ¿Ë淴Ӧʱ¼ä±ä»¯µÄÇúÏßÈçÏÂͼ£¬ÏÂÁбíÊöÖĐƠưÈ·µÄÊÇ
ÔÚ̉»¶¨Î¶ÈÏ£¬ÈƯÆ÷ÄÚij̉»·´Ó¦ÖĐM¡¢NµÄÎïÖʵÄÁ¿Ë淴Ӧʱ¼ä±ä»¯µÄÇúÏßÈçÏÂͼ£¬ÏÂÁбíÊöÖĐƠưÈ·µÄÊÇ
A£®·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ£º2M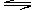 N
N
B£®t2ʱ£¬ƠưÄæ·´Ó¦ËÙÂÊÏàµÈ£¬´ïµ½Æ½ºâ
C£®t3ʱ£¬Ơư·´Ó¦ËÙÂÊ´óÓÚÄæ·´Ó¦ËÙÂÊ¡¡¡¡¡¡ D£®t1ʱ£¬NµÄŨ¶ÈÊÇMŨ¶ÈµÄ2±¶
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com