
21. 目前人们正在研究一种高能电池--钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na + xS = Na2Sx,以下说法正确的是:
A、放电时钠作正极,硫作负极;
B、充电时钠极与外电源的正极相连,硫与外电源的负极相连
C、充电时,阳极发生的反应为:Sx2- - 2e = x S D、放电时钠极发生氧化反应
20. 、某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿氏常数,下列说法中正确的是:
A、氧元素的相对原子质量为12a/b B、1mol该原子质量为aNAg
C、x g该氧原子所含的电子数为8x/a D、y g 该氧原子的中子数一定为8y/a
19. 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距离为a cm,氯化铯的式量为M,NA为阿氏常数,则氯化铯晶体的密度为
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距离为a cm,氯化铯的式量为M,NA为阿氏常数,则氯化铯晶体的密度为
|
|
|
|||||||
|
|||||||||
A、-- g/cm3 B、-- g/cm3 C、-- g/cm3 D、-- g/cm3
18.FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应生成H2S2,H2S2类似于H2O2,易分解:H2S2 = H2S + S↓。实验室制取H2S时,某学生误将FeS2颗粒当作FeS使用,当FeS2反应完后,不可能生成的物质是
A、FeS B、H2S C、S D、FeCl3
17. 下列离子方程式正确的是
A、在氢氧化钡溶液中加入过量小苏打: Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2O
B、在氢氧化钾的稀溶液中通入过量SO2: SO2 + OH- = HSO3-
C、氯化铁水解: Fe3+ +3H2O = Fe(OH)3↓+ 3H+
D、氯气通入水中:Cl2 + H2O = 2H+ + Cl- + ClO-
16、设NA为阿氏常数,下列叙述正确的是
A、在100mL0.5mol/LCH3COOH溶液中CH3COOH分子数等于0.05NA;
B、标况下,11.2LCH4中所含电子数总和为5NA;
C、在100mLpH=1的稀硫酸中,水合氢离子数为0.1NA;
D、15.6gNa2O2跟过量CO2反应时,转移电子数为0.2NA。
15、下列反应的离子反应方程式正确的是
A、过量二氧化碳通入少量漂白粉溶液中: CO2 + ClO- + H2O = HClO + HCO3-
B、氯气通入冷的氢氧化钠溶液中: 2Cl2 + 2OH- = 3Cl- + ClO- + H2O
C、硫酸亚铁溶液中加入过氧化氢溶液: Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2O
D、硫代硫酸钠溶液中滴入稀盐酸: S2O32- + 2H+ = S↓ + SO2↑+ H2O
14..NA表示阿伏加德罗常数的值,下列说法正确的是()
A.2.4g金属镁与足量的盐酸反应,转移电子数为2NA
B.1mol硫原子同足量的铜粉充分反应时,铜失去的电子数为2NA
C.3molNO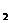 跟水充分作用,转移的电子数为3NA
跟水充分作用,转移的电子数为3NA
D.常温常压下,活泼金属从盐酸中置换出1molH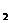 ,发生转移的电子数为2NA
,发生转移的电子数为2NA
13.已知:H2(g)+I2(g)
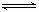 2HI(g)的平衡常数为K1
;
2HI(g)的平衡常数为K1
;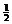 H2(g)+
H2(g)+ 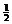 I2(g)
I2(g) 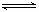 HI(g)的平衡常数为K2,则K1、K2的关系为
HI(g)的平衡常数为K2,则K1、K2的关系为
A、K1= 2K2 B、K1= K22 C、K1 = K2 D、K1= K2
12.设NA为阿伏加德罗常数。下列叙述中正确的是
A.标准状况下,22.4 LCO2和O2混合气体中含有的氧原子数约为NA
B.常温常压下,0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3 NA
C.2.3 g 钠被足量O2完全氧化时,失去电子数约为0.1×6.02×1023
D.1 L 1 mol/L的K2CO3溶液中离子总数大于3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com