
7、一个塑料文具胶带如图10所示,带宽为1cm,内径为4cm,外径为7cm,已知30层胶带厚1.5mm,则这卷胶带长 m..

6、某住宅小区6月份随机抽查了该小区6天的用水量(单位:吨),结果分别是30、34、32、37、28、31,那么,请你估计该小区6月份(30天)的总用水量约是 吨.
4、直线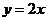 过点A,则不等式
过点A,则不等式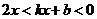 的解集为( )
的解集为( )
A.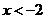 B.
B.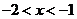
C.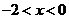 D.
D.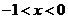
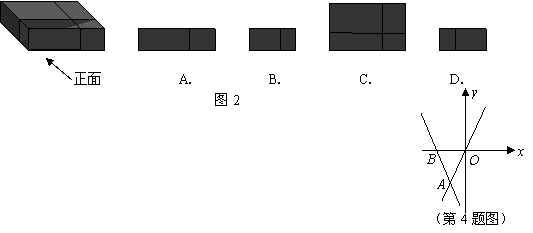
3、如图2是小玲在九月初九“重阳节”送给她外婆的礼盒,图中所示礼盒的主视图是( )
1,据统计,2008年在国际金融危机的强烈冲击下,我国国内生产总值约30 067 000 000 000元,仍比上年增长9.0%.30 067 000 000 000元用科学记数法表示为( )
A.30 067×109元 B.300.67×1011元
C.3.006 7×1013元 D.0.300 67×1014元
2、计算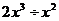 的结果是( )
的结果是( )
A.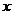 B.
B.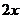 C.
C.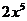 D.
D.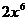
25. (1) (4分) 为测定石灰石中CaCO3的质量分数,取40.0g稀盐酸分4次加入到10.0 g石灰石样品中(石灰石中的杂质不跟稀盐酸反应),实验中测出的数据记录如下表:
|
|
加入稀盐酸的质量/g |
剩余固体的质量/g |
|
第一次 |
10.0 |
7.0 |
|
第二次 |
10.0 |
m |
|
第三次 |
10.0 |
2.0 |
|
第四次 |
10.0 |
n |
根据实验中的数据计算下列问题:
①m = __________,n = ________。②石灰石中CaCO3的质量分数为___________。
(2) (6分) 钙是维持人体正常功能所必需的元素。下图所示为某种补钙剂“钙尔奇”说明书的一部分。取1片钙尔奇,放入盛有适量稀盐酸的烧杯中,其中的碳酸钙跟盐酸完全反应(其他成分与盐酸不反应)。
反应前后的质量如下:
|
反应前 |
烧杯+1片钙尔奇+稀盐酸 |
32.00 g |
|
反应后 |
烧杯+烧杯内的物质 |
31.34g |
 请你计算:
请你计算:
①每片钙尔奇中含碳酸钙的质量。
②服用这种补钙剂,每人每天摄入钙元素的质量。
解:
24. (4分) 今天是某附属中学实验室的开放日,初三七班的同学来到实验室,实验室的桌上摆放有如图所示的仪器:
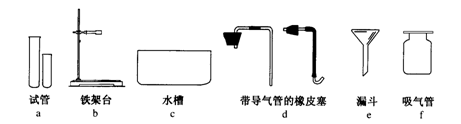
(1) 班长让同学完成的第一个任务是写出仪器的名称,同学们完成任务的情况如图所示,其中名称有错误的是__________(填序号)。
(2) 用高锰酸钾制取氧气还需要的玻璃仪器是___________________。
(3)
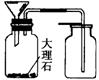 某同学想用右图所示制取CO2,班长指出这需要太多的稀盐酸才能淹没漏斗的下管口,起到液封的作用。有位同学选用了上面的一种仪器,加在右图装置上,既解决了液封的问题,又可以减少酸的用量,请把仪器画在图中应该放置的位置。
某同学想用右图所示制取CO2,班长指出这需要太多的稀盐酸才能淹没漏斗的下管口,起到液封的作用。有位同学选用了上面的一种仪器,加在右图装置上,既解决了液封的问题,又可以减少酸的用量,请把仪器画在图中应该放置的位置。
23. (11分) 实验室制取气体的装置如下图所示,根据所学的知识回答下列问题:
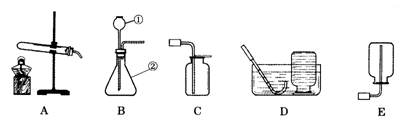
(1) 图中标有①、②的仪器名称:①_____________;②____________。
(2) 写出实验室用装置B制取氧气的反应方程式________________________________,A装置中试管略向下倾斜的原因是:
_____________________________________________________________________。
(3) 写出实验室制取二氧化碳的反应方程式:
_____________________________________________________________________。可选用图中__________和__________(填编号)组装一套制取二氧化碳的装置。检验二氧化碳的反应方程式___________________________________。
22. (8分) (1) 由碳元素和氢元素组成的化合物种类非常之多,以下是其中称为“烷烃”的一类,请你根据其化学式(分子式)的规律,写出丙烷和戊烷的化学式。
|
甲烷 |
乙烷 |
丙烷 |
丁烷 |
戊烷 |
…… |
十一烷 |
…… |
|
CH4 |
C2H6 |
_______ |
C4H10 |
_______ |
|
C11H24 |
|
(2) 丙烷和丁烷是液化石油气的主要成分,请你写出丁烷充分燃烧的化学方程式。
___________________________________________________________
丁烷在燃烧不充分时会生成一种使人中毒的气体,这种气体是_____________。
(3) 在煤气中加入少量有特殊气味的乙硫醇(化学式为C2H5SH)能及时发现煤气泄漏。乙硫醇充分燃烧生成三种氧化物,完成这一反应的化学方程式(在方框内填写化学计量数,在横线上填写化学式。)
2C2H5SH + 9O2
 □__________+□__________ +□__________
□__________+□__________ +□__________
乙硫醇燃烧时排放出的_______________气体溶于雨水会形成酸雨。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com