
8. 梁启超曾说,知有兵事而不知有民政……知有朝廷而不知有国民……以为吾中国之政教风俗无一不优于他国。这里批评的是当时某个派别主张
A、中学为体,西学为用 B、师夷长技以制夷
C、军事为主,民生为辅 D、原封不动地维护封建统治
7. 康有为曾上书光绪帝:“今则万国交通,一切趋于尚同,而吾以一国衣服独异……今为机器之世,多机器则强,少机器则弱,辫发与机器不相容也。” 这表明资产阶级维新派实质上要求
A.改革社会风尚 B.吸收世界文明
C.发展近代交通 D.主张机器生产
6.鸦片战争后,近代中国的经济发生了深刻的变化,下列说法正确的是
①家庭手工业开始与农业分离 ②农村商品开始交流到城市市场
③近代资本主义性质的企业开始出现 ④中国逐渐沦入资本主义世界市场
A.①②③ B.①②④ C.②③④ D.①③④
5.王阳明宣扬“心外无物,心外无理”,下列诗词中能体现这一意境的是
A.野旷天低树,江清月近人 B.还似旧时游上苑,车如流水马如龙
C.结庐在人境,而无车马喧 D.江流天地外,山色有无中
4. “(元)世祖皇帝建元中统以来……夫外之郡县,其朝廷远者,则镇之以行中书省。郡县又远于省,若有边徼之事者,则置宣慰司以达之。”对此材料理解正确的是
A.行省是元朝管辖边疆的唯一机构
B.中央政府加强了对地方的有效管理
C.行省是地方最高行政机关,拥有军政大权
D.行省辖区广阔,发展了前代的政治制度
3. 某历史兴趣小组在探究“宋代城市商业发展”课题的过程中,搜集到了下列素材,你认为其中最有价值的是
A.司马光主编的史学巨著《资治通鉴》
B.“南海一号”沉船打捞出的青花瓷片
C. 画家张择端《清明上河图》的摹本
D.苏轼的《洞庭春色赋》手迹拓片
2.下图分别是“仁”字小饰品和北京街头的“仁”字广告牌,这些都表明


A.商家均以仁爱作为打造品牌的工具 B.孔子思想已成为当今社会的行为准则
C.国人对社会和谐发展的真诚祈愿 D.只要弘扬传统道德就能实现社会公平
1.《孟子》中记载:“天子适诸侯曰巡狩……诸侯朝于天子曰述职……一不朝,则贬其爵;再不朝,则削其地;三不朝,则六师移之。”这主要反映了
A.西周初年周天子具有至尊权威 B.西周初年诸侯势力逐渐增强
C.诸侯有对周王朝觐述职的义务 D.西周末年周王势力日益衰微
21.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容,请选择其中一题,并在相应的答题区域作答。若两题都做,则按A题评分。
A.能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
 ⑴太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式 ▲ 。
⑴太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式 ▲ 。
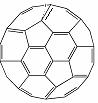
⑵富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为 ▲ ;1 mol C60分子中σ键的数目为 ▲ 。
 ⑶多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
⑶多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As ▲ Se(填“>”、“<”或“=”)。
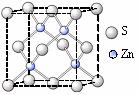
②硫化锌的晶胞中(结构如右图所示),硫离子的配位数是 ▲ 。
③二氧化硒分子的空间构型为 ▲ 。
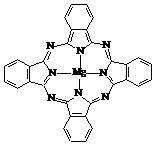
⑷金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如下图,请在下图中用箭头表示出配位键。
B.实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
|
化合物 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100g水 |
|
正丁醇 |
74 |
0.80 |
118.0 |
9 |
|
冰醋酸 |
60 |
1.045 |
118.1 |
互溶 |
|
乙酸正丁酯 |
116 |
0.882 |
126.1 |
0.7 |
请回答有关问题:
Ⅰ.乙酸正丁酯粗产品的制备
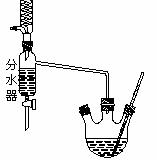 在三孔圆底烧瓶中加入沸石、18.5mL正丁醇和15.4mL冰醋酸,再加3-4滴浓硫酸。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热使之反应。
在三孔圆底烧瓶中加入沸石、18.5mL正丁醇和15.4mL冰醋酸,再加3-4滴浓硫酸。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热使之反应。
⑴有同学拟通过某种谱线鉴定所得产物中是否含有醚类物质。这种谱线为 ▲ 。
⑵反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是 ▲ 。
Ⅱ.乙酸正丁酯粗产品的精制
⑴①将圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步操作的目的是 ▲ 。
②用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是 ▲ 。
⑵将酯层进行蒸馏。蒸馏收集乙酸正丁酯产品时,应将温度控制在 ▲ 左右。
Ⅲ.计算产率
称量制得的乙酸正丁酯的质量为12.76g,则乙酸正丁酯的产率为 ▲ 。
20.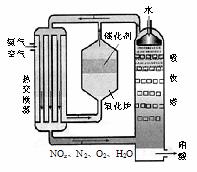 (10分)右图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有:
(10分)右图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有:
①4NH3(g)+5O2(g) 4NO(g) +6H2O(l) △H<0
4NO(g) +6H2O(l) △H<0
②2NO(g)+O2
(g) 2NO2(g) △H<0
2NO2(g) △H<0
③3NO2(g)+H2O(l) 2HNO3(l) +NO(g) △H<0
2HNO3(l) +NO(g) △H<0
⑴能使吸收塔内反应速率增大,且能提高HNO3产率的措施是 ▲ 。
A.适当升高温度
B.适当增大吸收塔内的压强
C.增大空气中O2的浓度
D.吸收塔内填充瓷环,增大气液接触面
⑵在2L密闭容器内充入0.50 mol NO和0.25 mol O2,维持反应温度为800℃,当反应达到平衡时,NO的转化率为50%。则800℃时反应2NO+O2=2NO2的平衡常数K= ▲ 。
⑶某工厂每套设备每小时可生产20 t 63%的硝酸(密度为1.4 g/cm3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。
回答下列问题:
①该工厂设备所生产硝酸的物质的量浓度是 ▲ 。
②每小时从吸收塔淋下的水的质量应是多少吨?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com