
3. doubt
A. young B. soul C. mountain D. would
2. bicycle
A. precious B. musical C. officer D. especially
第一节 语音知识 (共5小题;每小题1分;满分5分)
从A、B、C、D四个选项中,找出其划线部分与所给单词的划线部分读音相同的选项,并在答题卡上将该项涂黑。
例:have
A. gave B. save C. hat D. made
答案是C。
1. strong
A. comb B. obvious C. freedom D. front
28. (14分) 次氯酸钠和高铁酸钾(
(14分) 次氯酸钠和高铁酸钾(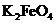 )是两种重要的化工产品,在生产和生活中有广泛的应用。
)是两种重要的化工产品,在生产和生活中有广泛的应用。
(1)工业上用氯气和烧碱溶液可以制取次氯酸钠,反应的离子方程式是 。
(2)工业上有多种方法制备高铁酸钾。
①电解法:原理如右图所示。阴极的电极反应是 。
②湿法氧化:在溶液中用次氯酸钠、氢氧化铁和氢氧化钾制高铁酸钾,参加反应的氧化剂和还原剂的物质的量之比是 。
(3)已知:



①配制高铁酸钾溶液时,应将其溶于一定浓度的KOH溶液中,原因是 。
②用如图所示装置测定高铁酸钾溶液中溶质的物质的量浓度,需要测定的两个实验数据是
。
(4)用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,已知该电池的总反应是: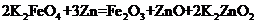 ,则负极的电极反应是
。
,则负极的电极反应是
。
27. (14分)工业以浓缩海水为原料提取溴的部分过程如下:

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

(1)A装置中通入a气体的目的是(用离子方程式表示) 。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是
。
(3)反应过程中,B装置中有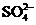 生成。检验
生成。检验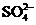 的方法是
。
的方法是
。
(4)C装置的作用是 。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用 方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是 。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是:取出少量溶液,先加入新制氯水,再加入淀粉KI溶液。该方法是否合理并简述理由 。
26. (16分)有A、B、C、D、E、F六瓶不同物质的溶液,它们各是NaOH、(NH4)2CO3、BaCl2、AgNO3、HCl和MgSO4溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。其中“↓”表示生成沉淀或微溶化合物,“↑”表示生成气体或受热挥发出碱性气体的化合物,“-”表示观察不到明显变化。试回答下列问题。
|
|
A |
B |
C |
D |
E |
F |
|
A |
- |
- |
↓ |
↑ |
- |
- |
|
B |
- |
- |
↓ |
↓ |
↓ |
↓ |
|
C |
↓ |
↓ |
- |
↓ |
↓ |
↓ |
|
D |
↑ |
↓ |
↓ |
- |
↓ |
↑ |
|
E |
- |
↓ |
↓ |
↓ |
- |
- |
|
F |
- |
↓ |
↓ |
↑ |
- |
- |
(1)写出A~F物质的化学式。
A: ,B: ,C:
D: ,E: ,F:
(2)写出下列反应的离子方程式。
A与D反应:
B与F反应:
25. (14分)有机化合物D常用于香料工业和电镀工业。D的合成过程如图所示。

(1)①A中含氧官能团的名称是 。
②A可以发生的反应是 (填字母)。
a.还原反应 b.消去反应 c.水解反应 d.取代反应
(2)B是由碳、氢、氧三种元素组成的化合物,经质谱分析相对分子质量为58;分子中含有碳氧双键和2个甲基。B的结构简式是 。
(3)D的结构简式是 。
(4)已知B能和H2发生加成反应;E与C互为同分异构体。A氧化后的产物与B和H2加成后的产物在
一定条件下反应制得E。该反应的化学方程式是 。
(5)F可作塑料的热稳定剂,由苯酚和B反应制得:

F能与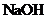 反应,F分子苯环上的一氯取代物只有两种,核磁共振氢谱显示其分子中含有4种不同类型的氢原子。F的结构简式是
。
反应,F分子苯环上的一氯取代物只有两种,核磁共振氢谱显示其分子中含有4种不同类型的氢原子。F的结构简式是
。
13. 早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔) =4Na + O2↑+
2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔) =4Na + O2↑+
2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
3Fe+4NaOH  Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:2OH--2e-=H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
第II卷
12.下述实验不能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将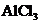 溶液蒸干灼烧 溶液蒸干灼烧 |
制备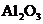 |
|
B |
向沸水中滴加几滴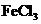 饱和溶液,继续加热至红褐色 饱和溶液,继续加热至红褐色 |
制备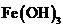 胶体 胶体 |
|
C |
向某溶液中加入稀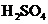 ,将产生的气体通入澄清石灰水 ,将产生的气体通入澄清石灰水 |
检验溶液中是否含有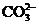 |
|
D |
相同温度下,测定浓度分别为0.1mol·L-1的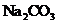 和 和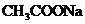 溶液的pH 溶液的pH |
比较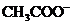 和 和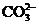 结合 结合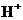 的能力强弱 的能力强弱 |
11. 常温下,将体积为V1、物质的量浓度为c1的氨水滴加到体积为V2、物质的量浓度为c2的盐酸中,下列结论正确的是
A.若V1=V2,且溶液的pH<7,则一定有c1<c2
B.若c1=c2,V1=V2,则混合液中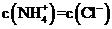
C.若混合液的pH=7,则混合液中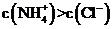
D.若混合液的pH=7, 则原溶液中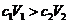
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com