
20£®Î¶ȡ¢´ß»¯¼Á²»±ä£¬Ïòijһ¹Ì¶¨Ìå»ýµÄÃܱÕÈÝÆ÷ÄÚ°´ÏÂÁи÷×éÎïÖʵÄÁ¿¼ÓÈëH2¡¢N2¡¢NH3£¬·´Ó¦´ïµ½Æ½ºâʱNH3Ũ¶È×î´óµÄÒ»×éÊÇ
|
¡¡ |
A |
B |
C |
D |
|
H2 |
6 |
1 |
3.5 |
5 |
|
N2 |
2 |
0 |
1 |
1.5 |
|
NH3 |
0 |
4 |
2 |
1 |
19£®ÊÒÎÂʱ£¬ÏÂÁи÷ÖÖ˵·¨ÖÐÕýÈ·µÄÊÇ
¡¡ A£®pH = 2µÄ´×ËáÈÜÒº£¬ÔÙ¼ÓˮϡÊÍÖÁÔÀ´µÄ100±¶£¬ÈÜÒºµÄpH = 4
¡¡ B£®pH = 2µÄij¶þԪǿËáºÍpH = 12ijһԪǿ¼îµÈÌå»ý»ìºÏ£¬ËùµÃÈÜÒºµÄpHÒ»¶¨µÈÓÚ7
¡¡ C£®ÏòFeCl3ÈÜÒºÖмÓÈëKSCN¿ÉʹÈÜÒºµÄÑÕÉ«±ädz
¡¡ D£®ÈôHA¡¢H2BÁ½ÖÖËáÈÜÒºµÄŨ¶È¶¼ÊÇ0.1 mol/L£¬pHÒÀ´ÎΪ1.5ºÍ1.8£¬µ±NaAºÍNa2BµÄŨ¶È¶¼ÊÇ0.1 mol/Lʱ£¬Na2BÈÜÒºµÄpH×îС
18£®³£ÎÂÏ£¬½«1 molµÄÏÂÁÐÎïÖÊͶÈëµ½1 LË®ÖУ¬ÈÜÒºÖÐÒõÀë×ÓÊýÄ¿´Ó´óµ½Ð¡µÄÅÅÁÐ˳ÐòÕýÈ·µÄÊÇ
¢ÙNa2O2¡¡¡¡ ¢ÚCa3(PO4)2¡¡¡¡ ¢ÛNa2S¡¡¡¡ ¢ÜNaClO¡¡¡¡ ¢ÝAlCl3
¡¡ A£®¢Ý¢Ù¢Û¢Ü¢Ú¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®¢Ý¢Ú¢Ù¢Û¢Ü
¡¡ C£®¢Ù¢Ý¢Û¢Ú¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¢Ú¢Ý¢Ù¢Û¢Ü
17£®ÔÚÒ»¶¨Î¶ÈÏ£¬½«CO(g) ºÍH2O(g)·Ö±ðΪ1 mol¡¢3 molÔÚÃܱÕÈÝÆ÷Öз´Ó¦£º
CO(g) + H2O(g) 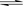 ¡¡CO2(g) + H2(g)
¡¡CO2(g) + H2(g)
´ïµ½Æ½ºâºó²âµÃCO2Ϊ0.75 mol£¬ÔÙͨÈë6 mol H2O(g)£¬´ïµ½ÐµÄƽºâºó£¬CO2ºÍH2µÄÎïÖʵÄÁ¿Ö®ºÍ¿ÉÄÜΪ
¡¡ A£®1.0 mol¡¡¡¡¡¡ B£®1.5 mol¡¡¡¡¡¡ C£®1.8 mol¡¡¡¡¡¡ D£®2.0 mol
16£®ÊÒÎÂÏ£¬Ä³ÈÜÒºÖÐÓÉË®µçÀë³öÀ´µÄc(H+)Ϊ1¡Á10£12 mol/L£¬Ôò¸ÃÈÜÒºÖÐÒ»¶¨²»¿ÉÄÜ´óÁ¿´æÔÚµÄÀë×Ó×éÊÇ
¡¡ A£®Cu2+¡¢SO42£¡¢Cl£¡¢Na+¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ca2+¡¢Cl£¡¢HCO3£¡¢K+
¡¡ C£®NH4+¡¢NO3£¡¢SO42£¡¢Mg2+¡¡ ¡¡¡¡¡¡¡¡D£®Cl£¡¢SO42£¡¢K+¡¢Na+
15£®Ò»¶¨Î¶ÈÏ£¬ÔÚÈÝ»ýºã¶¨µÄÃܱÕÈÝÆ÷ÖУ¬·¢ÉúÈçÏ·´Ó¦£º
¡¡¡¡ A(s) + 2B(g) 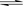 ¡¡C(g) + D(g)
¡¡C(g) + D(g)
µ±ÏÂÁÐÎïÀíÁ¿²»·¢Éú±ä»¯Ê±£¬ÄܱíÃ÷¸Ã·´Ó¦ÒѴﵽƽºâ״̬µÄÊÇ
¢ÙÈÝÆ÷ÄÚÆøÌåµÄѹǿ¡¡¡¡¡¡¡¡¡¡ ¢Ú»ìºÏÆøÌåµÄÃܶÈ
¢ÛBÎïÖʵÄÎïÖʵÄÁ¿Å¨¶È¡¡¡¡¡¡ ¢Ü»ìºÏÆøÌåµÄ×ܵÄÎïÖʵÄÁ¿
¡¡ A£®¢Ù¢Ü¡¡¡¡¡¡ B£®¢Ú¢Û¡¡¡¡¡¡ C£®¢Ú¢Û¢Ü¡¡¡¡¡¡ D£®Ö»ÓТÛ
14£®ÓÃpH´óС±íʾÈÜÒºµÄËá¼îÐÔÏà¶ÔÇ¿ÈõÓÐÐí¶à²»×ãÖ®´¦¡£Òò´Ë£¬ºÉÀ¼¿Æѧ¼ÒHenk VanLubeckÒýÈëÁËËá¶È(AG)µÄ¸ÅÄ¼´°ÑËá¶È¶¨ÒåΪc(H+)Óëc(OH£)±ÈÖµµÄ¶ÔÊý£¬Óù«Ê½±íʾΪ£ºAG = lg{c(H+)/c(OH£)}¡£ÏÂÁÐÓйØÐðÊöÖУ¬ÕýÈ·µÄÊÇ
¡¡ A£®ÔÚ25¡æʱ£¬ÈÜÒºµÄpHÓëAGµÄ»»Ë㹫ʽΪ£ºAG = 2(7 - pH)
¡¡ B£®ÔÚ25¡æʱ£¬AG = 10µÄÈÜÒº³Ê¼îÐÔ
¡¡ C£®ÔÚ25¡æʱ£¬0.01 mol/L NaOHÈÜÒºµÄAG = 0
¡¡ D£®ÔÚ25¡æʱ£¬ÈôÈÜÒº³ÊÖÐÐÔ£¬ÔòpH = 7£¬AG = 1
13£®ÏÂÁÐʽ×ÓÖУ¬ÊôÓÚË®½â·´Ó¦ÇÒÈÜÒº³ÊËáÐÔµÄÊÇ
¡¡ A£®HS£+ H2O
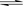 ¡¡H3O+ + S2£
¡¡H3O+ + S2£
¡¡ B£®HCO3£+ H2O
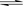 ¡¡H2CO3 + OH£
¡¡H2CO3 + OH£
¡¡ C£®NH4+
+ H2O 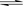 ¡¡NH3¡¤H2O
+ H+
¡¡NH3¡¤H2O
+ H+
¡¡ D£®HCO3£ + H2O
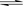 ¡¡H3O+ + CO32£
¡¡H3O+ + CO32£
12£®ÔÚÒ»¶¨Î¶ÈÏ£¬ÓÐa£®ÑÎËá¡¡ b£®´×ËáÁ½ÖÖËᣬÏÂÁÐÐðÊöÖв»ÕýÈ·µÄÊÇ
¡¡ A£®µ±c(H+)Ïàͬ¡¢Ìå»ýÏàͬʱ£¬·Ö±ð·ÅÈëµÈÖÊÁ¿µÄп£¬Èô²úÉúµÈÁ¿µÄH2£¬Ôò·´Ó¦ËùÐèʱ¼ä£ºa > b
¡¡ B£®ÏàͬÌå»ý¡¢ÏàͬÎïÖʵÄÁ¿Å¨¶ÈµÄÁ½ÖÖËᣬÓëNaOH¹ÌÌå·´Ó¦£¬ÖкÍNaOHµÄÄÜÁ¦£ºb>a
¡¡ C£®ÏàͬÌå»ý¡¢ÏàͬÎïÖʵÄÁ¿Å¨¶ÈµÄÁ½ÖÖËáÖÐË®µÄµçÀë³Ì¶È£ºb > a
¡¡ D£®µ±c(H+)Ïàͬ¡¢Ìå»ýÏàͬʱ£¬·Ö±ð·ÅÈë×ãÁ¿µÄп£¬Ïàͬ״¿öϲúÉúÆøÌåµÄÌå»ý£ºb > a
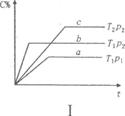
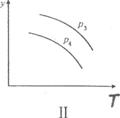
11£®ÔÚijÃܱÕÈÝÆ÷ÖУ¬¿ÉÄæ·´Ó¦£ºA(g) + B(g) 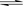 ¡¡xC(g)£¬·ûºÏÏÂÁÐͼÏñ(¢ñ)Ëùʾ¹Øϵ¡£ÓÉ´ËÍƶ϶ÔͼÏñ(¢ò)µÄÕýȷ˵·¨ÊÇ
¡¡xC(g)£¬·ûºÏÏÂÁÐͼÏñ(¢ñ)Ëùʾ¹Øϵ¡£ÓÉ´ËÍƶ϶ÔͼÏñ(¢ò)µÄÕýȷ˵·¨ÊÇ
 ¡¡
¡¡
A£®p3 > p4£¬yÖá±íʾAµÄ°Ù·Öº¬Á¿
¡¡ B£®p3 > p4£¬yÖá±íʾBµÄ°Ù·Öº¬Á¿
¡¡ C£®p3£¼ p4£¬yÖá±íʾ»ìºÏÆøÌåµÄÃܶÈ
¡¡ D£®p3 > p4£¬yÖá±íʾ»ìºÏÆøÌåµÄƽ¾ùÏà¶Ô·Ö×ÓÖÊÁ¿
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com