
1.下列词语中,没有错别字的一组是( )
A.屏弃 气慨 流水账 兵来将挡水来土淹
B.祛除 内敛 哈蜜瓜 复巢之下安有完卵
C.狼籍 谛造 白炽灯 万变不离其中
D.砥砺 会晤 跆拳道 文武之道一张一弛
30.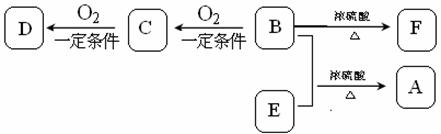 (15分)有机物A(C13H18O2)具有香味,可用作香皂、洗发香波的芳香剂。A可通过下图所示的转化关系而制得。
(15分)有机物A(C13H18O2)具有香味,可用作香皂、洗发香波的芳香剂。A可通过下图所示的转化关系而制得。
已知:
①B属于芳香族化合物,相对分子质量大于100,小于130,其中含氧质量分数为0.131;
②D、E具有相同官能团。E分子烃基k@s^5*u上的一氯取代物只有一种;
③F可以使溴的四氯化碳溶液褪色。
请回答下列问题:
(1)B的分子式为 ;B在k@s^5*u上图转化中所发生的反应类型有 。
(2)F的名称是 ,C发生银镜反应的化学方程式是 。
(3)D的同分异构体有多种,写出符合下列条件的所有物质的结构简式
a.属于芳香族化合物且苯环k@s^5*u上的一氯代物有两种;b.含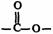 基团。
基团。
(4)B和E反应生成A的化学方程式为 。
29. (15分)某实验小组欲测定KMnO4的分解率α,但加热前忘记称量KMnO4的质量。面对此情况,甲同学采用下述方法:在加热时,利用浓盐酸与KMnO4受热部分分解后所得的固体混合物反应产生的Cl2被碱石灰吸收,通过碱石灰增重来计算KMnO4的分解率α。(与热的浓盐酸反应时,固体混合物中的Mn元素均被还原成Mn2+)
(15分)某实验小组欲测定KMnO4的分解率α,但加热前忘记称量KMnO4的质量。面对此情况,甲同学采用下述方法:在加热时,利用浓盐酸与KMnO4受热部分分解后所得的固体混合物反应产生的Cl2被碱石灰吸收,通过碱石灰增重来计算KMnO4的分解率α。(与热的浓盐酸反应时,固体混合物中的Mn元素均被还原成Mn2+)
取KMnO4受热部分分解后所得的固体混合物mg进行实验,请从k@s^5*u上图中选用所需的仪器(可重复选用)组成一套反应装置,其它固、液试剂自选。(其中某些连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置、打气筒等均略去)
(1)在反应发生前,为了消除装置内空气中酸性气体的影响,须用打气筒向装置内鼓入一定量的空气。请你在下表中填写完成本实验时各装置的连接次序及药品。
|
各装置连接次序 |
|
A |
|
|
C |
C |
|
对应的药品 |
|
d:浓盐酸 e:固体混合物 |
|
|
碱石灰 |
碱石灰 |
(2)k@s^5*u上述高锰酸钾受热部分分解后所得固体混合物中K2MnO4与MnO2物质的量之比是 。
(3)当A装置内反应结束后,关闭分液漏斗活塞,打开止水夹k,再一次用打气筒向装置内鼓入一定量空气,其目的是 。
(4)若测得碱石灰增重ng。为了计算KMnO4的分解率α,该同学采用方法如下:设原mg的固体混合物中KMnO4及MnO2的物质的量分别为x、y,依据实验数据m及n,可列出三个含x、y、α的等式,请你写出这三个等式。(注意:等式中不用带单位)
仅含m、x、y的等式①:m= 。
仅含 n、x、y的等式②:n= 。
仅含α、x、y的等式③:α= 。
(5)另一同学设计更为简单的方法(无须化学反应)也可测定KMnO4的分解率α。
该同学的方法是:称取一定量KMnO4受热部分分解后所得的固体混合物,置于盛有适量蒸馏水的烧杯中,充分搅拌,再进行“一系列实验操作”并记录实验数据,最后经计算,即可得出KMnO4的分解率α。该同学的“一系列实验操作”是指 。
28.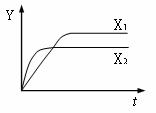 (15分)已知在某密闭容器中进行的反应a A
(g)
(15分)已知在某密闭容器中进行的反应a A
(g) 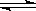 b B
(g)+ c C (g),(其中a、
b、c分别为方程式中的物质计量数),某物理量Y随时间(t)变化的情况如右图所示(X1、X2表示不同温度或压强),请回答下列问题:
b B
(g)+ c C (g),(其中a、
b、c分别为方程式中的物质计量数),某物理量Y随时间(t)变化的情况如右图所示(X1、X2表示不同温度或压强),请回答下列问题:
(1)当X1、X2分别表示不同的温度状况时,Y可代表生成物C在平衡时混合物中的质量分数, 则该反应的正反应是 反应(填“放热”或“吸热”);
(2)当X1、X2分别表示不同的压强状况时,Y可代表反应物A的转化率,则X1 X2(选填“>”或“<”或“=”);a、 b 、c三者之间的关系为 a (b+c)(填“>”或“<”或“=”)
(3)将 4mol A、3mol B、2mol C充入该反应容器中,在温度为T,压强为P的条件下达平衡后,测得A、B、C的物质的量分别是2mol A、5mol B、3mol C,则a、b、c的最简整数比为 ;此时A的转化率为 。若将最初充入该反应容器中的各物质的物质的量变为5mol A、2mol B、1.5mol C,也在温度为T,压强为P的条件下建立平衡,此时容器中的C在混合气体中的体积分数为30%,则此时A的转化率为 。
(4)将 4mol A、3mol B、2mol C充入该反应容器中并达平衡,下列措施能提高物质B在平衡混合气体中体积分数的是 (填写序号)
①增加B的物质的量 ②加入合适的催化剂
③增加A的物质的量 ④降低温度
27.(15分)已知X、Y、Z为三种由短周期元素构成的粒子,每摩粒子都有10mol电子,其结构特点如下:
|
|
X |
Y |
Z |
|
原子核数 |
单核 |
四核 |
双核 |
|
粒子的电荷数 |
1个单位正电荷 |
0 |
1个单位负电荷 |
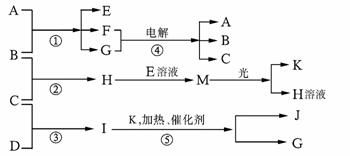 现有A、B、C、D、E、F、G、H、I、J、K等物质,它们之间的相互反应转化关系如下图所示:
现有A、B、C、D、E、F、G、H、I、J、K等物质,它们之间的相互反应转化关系如下图所示:
已知物质A由X、Z构成, B、C、D、K都是单质,G为无色液体,I的水溶液呈碱性,反应①-⑤都是用于工业生产的反应,请回答下列问题:
(1) A的电子式为 ;D的结构式为 。
(2)物质B的组成元素在元素周期表中的位置是 。
(3)反应①的化学方程式为 。
反应④离子方程式为 。
(4)H和I反应的生成物的水溶液呈酸性,其原因是 (用一个离子反应方程式表示)
(5)已知每生成1mol I放出46.0kJ的热量,则反应③的热化学方程式为 。
13.有一铁的氧化物样品,用140mL5mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56L氯气,使其中的Fe2+全部转化为Fe3+。该样品可能的化学式为
A.Fe4O5
B.Fe5O7 C.Fe2O3  Fe3O4
Fe3O4
12.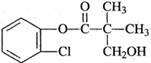 某有机物A是农药生产中一种中间体,其结构简式如下图所示,关于A的叙述不正确的是
某有机物A是农药生产中一种中间体,其结构简式如下图所示,关于A的叙述不正确的是
A.属于芳香族化合物
B.分子中至少有12个原子处于同一平面内
C.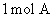 可以与4molNaOH反应
可以与4molNaOH反应
 一定条件下可发生加成反应、消去反应、水解反应
一定条件下可发生加成反应、消去反应、水解反应
11.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在短周期元素中,满足k@s^5*u上述关系的元素共有
A.3对 B.4对
C.5对
 6对
6对
10.中和相同体积相同pH的Ba(OH)2、NaOH和NH3·H2O三种稀溶液,所用相同浓度盐酸的体积分别为V1、V2和V3,则
A.V3>V1=V2
B.V3>V2>V1
C.V1>V2>V3  V3<V1=V2
V3<V1=V2
9.甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,片刻沉淀由白色变为灰绿色又变为红褐色,丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是
A.Al2(SO4)3 B.NaOH
C.BaCl2  FeSO4
FeSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com