
|
|
|
铁 |
铜 |
|
与非金属单质的反应 |
与O2 反应 |
|
|
|
与Cl2反应 |
|
|
|
|
与非氧化性酸(盐酸、稀硫酸)的反应 |
|
|
|
|
与某些盐溶液(如Cu2+、Ag+)的反应(置换) |
|
|
3. 铜的冶炼:
工业上用高温冶炼黄铜矿得到铜。次冶炼得到的铜,其含量达到99.5%-99.7%。通过 法精炼铜,同等含量可以达到99.95%-99.98%。
2. 铁的冶炼:
工业上铁的冶炼是在 中进行的。原料有 、 、 和 等。在冶炼过程中,铁元素被还原,还原剂是 ,产生还原剂的化学方程式
、 。由于矿石中有杂质,需除去,所加造渣剂为 ,反应方程式为 、 。
用这种方法炼出的铁是含碳2%-4.5%的 ,将生铁进一步冶炼,就可以得到用途广泛的钢。
1. 常见的铁矿:磁铁矿(主要成分为 _ )、赤铁矿(主要成分为 _____ )
常见的铜矿:黄铜矿(主要成分为 )、孔雀石(主要成分为 )
4、下列五个图中,横坐标为某溶液中加入某物质的量,纵坐标为生成沉淀的量,请从A-E中选择符合各题要求的序号填在表中。

|
|
某溶液 |
加入的物质 |
答案 |
|
① |
饱和石灰水 |
通过量的CO2 |
|
|
② |
AlCl3溶液 |
通过量的NH3 |
|
|
③ |
含少量NaOH的NaAlO2溶液 |
通过量的CO2 |
|
|
④ |
含少量NaOH的NaAlO2溶液 |
逐滴加稀盐酸 |
|
|
⑤ |
MgCl2、AlCl3混合溶液 |
逐滴加NaOH溶液至过量 |
|
3、下列为铝或铝合金的各种用途,在后面横线上写出所根据的性质:
⑴制造飞机或汽车外壳 ;
⑵作为储存浓硫酸的容器 ;
⑶制造各种日用炊具 ;
⑷铝热法冶炼金属 ;
⑸造电线电缆 ;
⑹制造包装用的铝箔 。
2、将一块镁铝合金先溶解在盐酸中,恰好反应完全,再加入过量的NaOH溶液,发生反应的离子方程式依次是⑴ _ ;
⑵ _ ; ⑶ _ ;
⑷ _ ;⑸ _ ;
方程式:_______________________________________________________
[归纳]铝三角的转换关系
Al3+ Al
Al AlO2-
AlO2-
Al3+ Al2O3
Al2O3 AlO2-
AlO2-
Al3+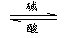 Al(OH)3
Al(OH)3 AlO2-
AlO2-
[练习]
1、①相同物质的量的钠、镁、铝与足量的稀盐酸反应时放出的氢气的体积比为_________。
②相同质量的钠、镁、铝与足量的稀盐酸反应时放出的氢气的体积比为____________。
③分别将0.3mol的钠、镁、铝投入100mL 1mol/l的硫酸溶液中,产生的氢气的体积比为____________。
3、不稳定性(受热易分解): ______
2、与强碱(如氢氧化钠)的反应:
注意:氢氧化铝不能溶解在氨水中。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com