
33.[物理-选修3-5模块](15分)
(1)下列说法正确的是
A.卢瑟福的 粒子散射实验揭示了原子核有复杂的结构
粒子散射实验揭示了原子核有复杂的结构
B.天然放射现象的发现揭示了原子核有复杂的结构
C.玻尔的原子结构理论是在卢瑟福的核式结构说学基础上引进了量子理论
D. 射线、
射线、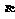 射线、
射线、 射线本质上都是电磁波,且
射线本质上都是电磁波,且 射线的波长最短
射线的波长最短
(2)从静止的镭核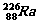 中射出的
中射出的 粒子垂直进入正交的匀强电场E和匀强磁场B,在电磁复合场中做直线运动,已知E=3.72×104N/C,B=2.0×10-3T
粒子垂直进入正交的匀强电场E和匀强磁场B,在电磁复合场中做直线运动,已知E=3.72×104N/C,B=2.0×10-3T
①写出核反应方程式;
②放出 粒子后,反冲核的速度多大?
粒子后,反冲核的速度多大?
③若静止的镭核放出 粒子是在匀强磁场中进行的,而且衰变后它们的速度垂直于匀强磁场B。求
粒子是在匀强磁场中进行的,而且衰变后它们的速度垂直于匀强磁场B。求 粒子与反冲核做圆周运动的半径之比,并定性地画出
粒子与反冲核做圆周运动的半径之比,并定性地画出 粒子和反冲核运动的完整轨迹。
粒子和反冲核运动的完整轨迹。
32. [物理-选修3-4模块](15分)
[物理-选修3-4模块](15分)
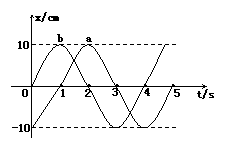
(1)如图所示,一列简谐横波沿直线由a向b传播,相
距10.5m的a、b两处质点的振动图象如图中的a、
b所示。则
A.该波的振幅可能是20cm
B.该波的波长可能是8.4m
 C.该波的波速可能是10.5m/s
C.该波的波速可能是10.5m/s
D.该波由a传播到b可能历时7s
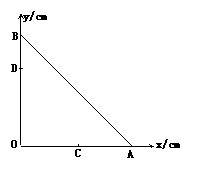
(2)将直角坐标和等腰直角棱镜ABO如图所示放置,腰长
为16cm。为了测量棱镜的折射率,从OB边的D点注视
A棱,发现A棱的视觉位置在C点。在D、C两点插上
大头针取走棱镜,若D、C两点的位置坐标分别为(0,12)
和(9,0),由此可求得棱镜的折射率为多少?
31.(10分)红外线CO2分析仪可用于测定混合气体中CO2的浓度及其变化量。将水稻的成熟绿叶组织放在密封透明的叶室内给以适宜光照,在不同CO2浓度下测定光合作用速率。右图示光合作用增长率随CO2浓度变化的情况,A-E是曲线上的点,
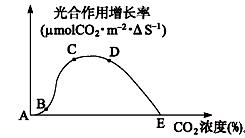
请分析完成下列问题:
(1)图中光合作用增长率最大的是 段,光合速率最快且CO2浓度最低的是 点对应的值。
(2)大棚生产上,可通过 措施保证CO2的供应。
(3)若用该装置和无色纱布测定叶片净光合速率与光强的关系,则主要实验设计思路是: 。
选考题(每科选做1题)
考生从给出的2道物理题、2道化学题中任选1题解答,2道生物题中任选1题解答并用2B铅笔在答题卡上把所选题目的对应题号涂黑。注意所做题目必须与所涂题目一致,在答题卡选答区域指定位置答题。
30.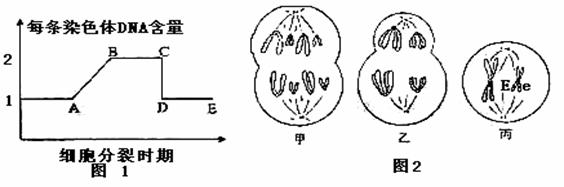 (9分)下图1表示某高等动物(基因型为EeFf)细胞分裂的不同时期每条染色体上DNA含量的变化;图2表示该生物细胞分裂不同时期的细胞图像(字母E、e代表染色体上的基因),请据图回答问题:
(9分)下图1表示某高等动物(基因型为EeFf)细胞分裂的不同时期每条染色体上DNA含量的变化;图2表示该生物细胞分裂不同时期的细胞图像(字母E、e代表染色体上的基因),请据图回答问题:
(1)图1中AB段形成的原因是 ,CD段变化发生在 期。
(2)图2中,甲细胞含有 个染色体组,乙细胞处于图1中的 段,丙细胞的名称是 。
(3)仔细观图2中 察丙细胞内染色体上的基因,分析产生这种情况的原因是 。
察丙细胞内染色体上的基因,分析产生这种情况的原因是 。
(4)请在图3坐标中的A、B、C处用直方图分别表示图2中甲、乙、丙细胞分裂过程中染色体数和染色体中DNA分子数目。
29.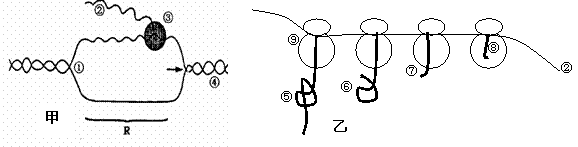 (12分)下图为真核细胞中的转录和多聚核糖体合成蛋白质的示意图,据图回答下列问题:
(12分)下图为真核细胞中的转录和多聚核糖体合成蛋白质的示意图,据图回答下列问题:
(1)正常情况下构成图中①和②的碱基有 种,核苷酸有 种,R所示的节段①的形成需要 。
(2)乙图中多聚核糖体上合成⑤⑥⑦⑧的原料是 ,该过程可以说明蛋白质合成的特点 。
(3)甲图中若R节段中有一个碱基发生替换,则合成的多肽链的结构一定会发生改变吗?
。说明原因 ;如果R节段的中部缺失了1个核苷酸对,可能的后果是(答出一种即可) 。
(4)甲图所示的过程发生的场所是 。
28.(8分)请分析下表,回答有关实验的问题。
|
组
别 |
材 料 |
实
验 条
件 |
观察内容 |
|
|
A |
A1 |
|
染液 |
线粒体 |
|
A2 |
0.9%NaCl溶液、8%盐酸.吡罗红甲基绿染色剂 |
DNA和RNA在细胞中的分布 |
||
|
B |
浸泡过的花生种子 |
清水、苏丹Ⅳ染液、 50%酒精溶液 |
细胞中着 色的小颗粒 |
|
|
D |
紫色洋葱鳞片叶外表皮 |
解离液、0.3g/mL蔗糖溶液、清水 |
|
(1)请在上表的 填补适当的内容。
(2)A1组实验中,在显微镜下观察到的线粒体呈 色。A2组实验中,盐酸的作用是 ,加速染色剂进入细胞,同时使 ,有利于DNA与染色剂结合。
(3)D组实验中,如果在显微镜下观察不到任何变化,原因可能是 。
27.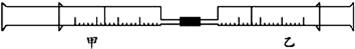 (15分)如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
(15分)如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
|
实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
|
1 |
10mL FeSO4溶液 |
10mL NH3 |
生成白色沉淀,后变色 |
|
2 |
20mL H2S |
10mL SO2 |
|
|
3 |
30mL NO2(主要) |
10mL H2O(l) |
剩有无色气体,活塞自动向内压缩 |
|
4 |
9mL Cl2 |
24mL NH3 |
|
试回答下列问题:
(1)实验1中,沉淀最终变为_______色,写出沉淀变色的化学方程式_______________。
(2)实验2甲针筒内的现象是:有_______生成,活塞___________移动(填“向外”“向内”或“不”)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入________溶液中。
(3)实验3中,甲中的30mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是__________,写出NO2与H2O反应的化学方程式_____________________。
(4)实验4中,已知:3Cl2+2NH3 N2+6HCl。甲针筒除活塞有移动、针筒内有白烟产生外,气体的颜色变化为________,最后针筒内剩余气体的体积约为________mL。
N2+6HCl。甲针筒除活塞有移动、针筒内有白烟产生外,气体的颜色变化为________,最后针筒内剩余气体的体积约为________mL。
26.(14分)物质之间的转化关系如下图,其中A、D、E、F、H为常见单质,其余为化合物,且单质E和单质F在点燃或加热的条件下生成淡黄色的固体,A易被磁性物质吸引,B常温下为液态化合物。
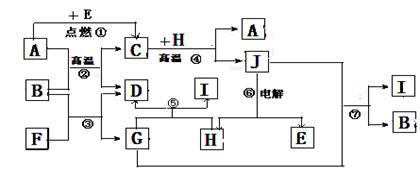
试回答下列有关问题:
(1)A在元素周期表的位置 周期 族
(2)单质E和单质F在点燃或加热的条件下生成的淡黄色固体是 (填化学式);其电子式 。
(3)写出反应②的化学方程式: ,
(4)写出引发反应④的实验操作 ,
写出该反应一种重要的工业用途 ,
(5)写出反应⑤的离子方程式: 。
(6)写出用A与H作电极材料插入G溶液形成闭合电路后的正极反应是 。
25.(14分)下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
⑥ |
⑦ |
⑧ |
|
⑨ |
⑩ |
|
(1)②、⑤、⑦的原子半径由小到大的顺序为_________________________。
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是______________________。
(3)①、④、⑤、⑩中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见微粒情况如下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
①用化学符号表示下列4种微粒:
A: B: C: D:
②写出A、B、E三种微粒反应的离子方程式:
24.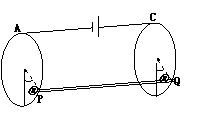 (17分)有两个相同的全长电阻为9Ω的均匀光滑圆环,固定于一个绝缘的水平台面上。两环分别在两个相互平行的、相距为20cm的竖直平面内,两环的连心线恰好与环面垂直,两环间有方向竖直向下的磁感应强度B=
(17分)有两个相同的全长电阻为9Ω的均匀光滑圆环,固定于一个绝缘的水平台面上。两环分别在两个相互平行的、相距为20cm的竖直平面内,两环的连心线恰好与环面垂直,两环间有方向竖直向下的磁感应强度B=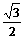 T的匀强磁场。两环的最高点A和C间接有一内阻r=0.5Ω的电源,连接导线的电阻不计。今有一根质量为10克,电阻为R0=1.5Ω的导体棒置于两环内侧,通电后导体棒恰好静止于如图所示的水平位置。它与圆弧的两接触点P、Q和圆弧最低点间所夹的弧对应的圆心角均为
T的匀强磁场。两环的最高点A和C间接有一内阻r=0.5Ω的电源,连接导线的电阻不计。今有一根质量为10克,电阻为R0=1.5Ω的导体棒置于两环内侧,通电后导体棒恰好静止于如图所示的水平位置。它与圆弧的两接触点P、Q和圆弧最低点间所夹的弧对应的圆心角均为 =60°,取重力加速度g=10m/s2。试求:
=60°,取重力加速度g=10m/s2。试求:
(1)平衡时,导体棒受到的安培力的大小;
(2)电路中的电流强度;
(3)电路中的总电阻;
(4)电源的电动势。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com