
2.[ҪвОц]өҘЦК·ЦЧУ¶јКЗ·Зј«РФјь№№іЙөД·Зј«РФ·ЦЧУЈ»ФЪ»ҜәПОп·ЦЧУЦРЈ¬ҝЙУЙј«РФјьРОіЙ·Зј«РФ·ЦЧУЈ¬ТІҝЙРОіЙј«РФ·ЦЧУЈ»п§СОКЗАлЧУ»ҜәПОпЈ¬¶јҝЙУЙ·ЗҪрКфФӘЛШРОіЙЎЈ
[ҙр°ё] (1)NH3ЎўH2OЎЎ (2)O2ЎўN2ЎЎ (3)SiCl4ЎўCO2ЎЎ (4)(NH4)2SO4
[ҝјМвФЩПЦ]
1.[ҪвОц]ёщҫЭ(CN)2·ЦЧУөД¶ФіЖРФәН180¶ИөДјьҪЗХвБҪёцТСЦӘМхјюЈ¬јҙҝЙНЖЦӘЖдөзЧУКҪЈ¬ІўЦӘЖдОӘ·Зј«РФ·ЦЧУЈ¬ФЩҫЭЖдУлВИЖшөДРФЦКПаЛЖЈ¬ҝЙРҙіцУлјо·ҙУҰөД·ҪіМКҪЎЈ
[ҙр°ё] 15.(1)(CN)2+2OH-ЈҪCN-+CNO-+H2OЎЎ (2) 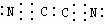 ЎЎ
ЎЎ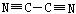 ЎЎ·Зј«РФЎЎ
(3)14ЎЎ
ЎЎ·Зј«РФЎЎ
(3)14ЎЎ 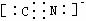
19.әЛҙЕ№ІХс(NMR)јјКхТС№г·әУҰУГУЪёҙФУ·ЦЧУҪб№№өДІв¶ЁәНТҪС§ВЫ¶ПөИёЯҝЖјјБмУтЎЈТСЦӘЦ»УРЦКЧУКэ»тЦРЧУКэОӘЖжКэөДФӯЧУәЛУРNMRПЦПуЎЈКФЕР¶ППВБРДДЧйФӯЧУҫщҝЙІъЙъNMRПЦПу(ЎЎЎЎ )
ЎЎ A. 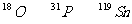
ЎЎ B. 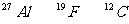
ЎЎ C. ФӘЛШЦЬЖЪұнЦРVAЧеЛщУРФӘЛШөДФӯЧУ
ЎЎ D. ФӘЛШЦЬЖЪұнЦРөЪ1ЦЬЖЪЛщУРФӘЛШөДФӯЧУ
өЪЛДҝОКұЎЎ ·Зј«РФ·ЦЧУәНј«РФ·ЦЧУ
[АэМвҪвОц]
18.ДіФӘЛШAДЬРОіЙЖшМ¬Зв»ҜОпHxAЈ¬ЛьөДЛ®ИЬТәДЬәНCaCO3·ҙУҰ·ЕіцК№іОЗеКҜ»ТЛ®ұд»лЧЗөДЖшМеЈ¬·ҙУҰЦРHxAәНCaCO3өДОпЦКөДБҝЦ®ұИОӘ2ЎГ1Ј¬ІвөГHxAЖшМеФЪұкЧјЧҙҝцПВөДГЬ¶ИОӘ1.629g/LЎЈКФИ·¶ЁЈә
(1)xЦөЈ»
(2)AөДПа¶ФФӯЧУЦКБҝәНГыіЖЈ»
(3)H-AјьКЗ·сКЗј«РФјь?HxAКЗ·сКЗј«РФ·ЦЧУ?
DЈ®°ВИьТ»Жі
17.ТСЦӘДіФӘЛШRөДЧоёЯјЫСх»ҜОпөДЛ®»ҜОп0.49gУлRөДЖшМ¬Зв»ҜОп0.17gЈ¬·ЦұрДЬәН100ml,0.1mol/2өДNaOHИЬТәНкИ«·ҙУҰЈ¬RФӘЛШөДФӯЧУЦРЈ¬ЦКЧУКэУлЦРЧУКэПаөИЈ¬ФЪЦЬЖЪұнЦРФӘЛШAЎўBУлRН¬ЦЬЖЪЧуУТПаБЪЈ¬ФӘЛШCЎўDУлRН¬ЦчЧеЙППВПаБЪЈ¬КФИ·¶ЁЈә
(1)RЎўAЎўBЎўCЎўDёчОӘәОФӘЛШ?
(2)ұИҪПRЎўCЎўDИэЦЦФӘЛШЖшМ¬Зв»ҜОпөДОИ¶ЁРФҙуРЎ?
(3)УЙRәНCБҪФӘЛШРОіЙөДБҪЦЦ»ҜәПОп·ЦЧУЦРЈ¬ЦёіцЛьГЗёчКфУЪәОЦЦ·ЦЧУ?
16.ПЦУР¶МЦЬЖЪAЎўBЎўCИэЦЦФӘЛШЈ¬ФӯЧУРтКэТАҙОФцҙуЈ¬AФӘЛШөДөҘЦККЗГЬ¶ИЧоРЎөДЖшМеЈ¬B»сөГ2ёцөзЧУҝЙҙпөҪОИ¶ЁҪб№№Ј¬CУлAН¬ЦчЧеЎЈ
(1)ЕР¶ПAЎўBЎўCёчОӘәОЦЦФӘЛШЎЈ
A______________ЎЎ B______________ЎЎ C______________
(2)УГөзЧУКҪұнКҫИэЦЦФӘЛШФӯЧУЦ®јдҝЙДЬ№№іЙөД»ҜәПОпөДРОіЙ№эіМЈ¬ІўЦёКҫёчЧФ»ҜС§јьөДАаРНЈә
ўЩAУлB______________Ўў______________
ўЪAУлC______________
ўЫBУлC______________Ўў______________
ўЬAЎўBЎўC______________
15.AЎўBЎўCЎўDЎўEЎўFЎўGОӘЖЯЦЦУЙ¶МЦЬЖЪФӘЛШ№№іЙөДОўБЈЈ¬ЛьГЗ¶јУР10ёцөзЧУЈ¬ЖдҪб№№МШөгИзПВЈә
|
ОўБЈҙъВл |
A |
B |
C |
D |
E |
F |
G |
|
ФӯЧУәЛКэ |
өҘәЛ |
өҘәЛ |
Л«әЛ |
¶аәЛ |
өҘәЛ |
¶аәЛ |
¶аәЛ |
|
өзәЙКэ(өҘО»өзәЙ) |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
ЖдЦРЈәBөДАлЧУ°лҫ¶ҙуУЪEөДАлЧУ°лҫ¶Ј»DКЗУЙј«РФјь№№іЙөД4ФӯЧУј«РФ·ЦЧУЈ»CУлFҝЙРОіЙDәНG·ЦЧУЎЈ
(1)AОўБЈөДҪб№№КҫТвНјКЗ______________ЎЈ
(2)ұИҪПBәНEПаУҰФӘЛШөДЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпөДјоРФЗҝИхЈ¬ОӘ______________Јҫ______________(УГ»ҜС§КҪұнКҫ)ЎЈ
(3)DәНGОўБЈКЗ·сОӘј«РФ·ЦЧУ?ҙрЈә______________ЎЈ
(4)CОўБЈКЗ______________Ј¬FОўБЈКЗ______________(УГөзЧУКҪұнКҫ)ЎЈ
14.ТСЦӘБЧЛб·ЦЧУ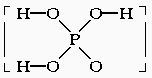 ЦРөДИэёцЗвФӯЧУ¶јҝЙТФёъЦШЛ®·ЦЧУ(D2O)ЦРөДDФӯЧУ·ўЙъЗвҪ»»»Ј¬УЦЦӘҙОБЧЛб(H3PO2)ТІҝЙёъD2OҪшРРЗвҪ»»»Ј¬ө«ҙОБЧЛбДЖ(NaH2PO2)ИҙІ»ФЩДЬёъD2O·ўЙъЗвҪ»»»Ј¬УЙҙЛҝЙНЖ¶ПіцH3PO2өД·ЦЧУҪб№№КЗ(ЎЎЎЎ
)
ЦРөДИэёцЗвФӯЧУ¶јҝЙТФёъЦШЛ®·ЦЧУ(D2O)ЦРөДDФӯЧУ·ўЙъЗвҪ»»»Ј¬УЦЦӘҙОБЧЛб(H3PO2)ТІҝЙёъD2OҪшРРЗвҪ»»»Ј¬ө«ҙОБЧЛбДЖ(NaH2PO2)ИҙІ»ФЩДЬёъD2O·ўЙъЗвҪ»»»Ј¬УЙҙЛҝЙНЖ¶ПіцH3PO2өД·ЦЧУҪб№№КЗ(ЎЎЎЎ
)

13.¶ФұИТФПВјёёц·ҙУҰКҪ:Cl+ClЎъCl2+247KJ;O+OЎъO2+493KJ;N+NЎъN2+946JЈ¬ҝЙөГіцөДҪбВЫКЗ(ЎЎЎЎ )
A.ФЪіЈОВПВN2ұИO2ЎўCl2ОИ¶ЁЎЎЎЎЎЎЎЎ B.өӘЎўСхЎўВИөД·ЦЧУ¶јКЗ·Зј«РФ·ЦЧУ
C.өӘЎўСхЎўВИ¶јКЗЛ«ФӯЧУ·ЦЧУЎЎЎЎЎЎЎЎ D.өӘЖшЎўСхЖшәНВИЖшөДГЬ¶ИІ»Н¬
CЈ®ДЬБҰСөБ·
12.AЎўBЎўCЎўDЛДЦЦФӘЛШЈ¬AB2·ЦЧУЦРУР22ёцөзЧУЈ¬CАлЧУЦРЦКЧУКэұИЦРЧУКэЙЩТ»ёцЈ¬11.5gCУлЧгБҝЛ®ҝЙ·ЕіцH25.6L(ұкҝцПВ)Ј»DУлCН¬ЦЬЖЪЈ¬ОЮСУХ№РФЈ¬ө«УРТ»¶ЁөДөјөзРФЈ¬ЗТФЪ»ҜәПОпЦРЦчТӘКЗ№ІјЫјьҪбәПЈ¬ПВГжРрКцХэИ·өДКЗ(ЎЎЎЎ )
A.DB2өДИЫөгәЬөНЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ B.C2B2УР·Зј«РФјь
C.ҫ§МеAТ»¶ЁКЗФӯЧУҫ§МеЎЎЎЎЎЎЎЎЎЎЎЎЎЎ D.ХвЛДЦЦФӘЛШФӯЧУРтКэЦ»УРТ»ёцЖжКэ
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com