
1. 解空气的成分、污染与防治
⑴干燥的空气的成分按体积分数计算,大约是氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%。
⑵排放到空气中的有害物质,大致可分为粉尘和有害气体(主要指二氧化硫、一氧化碳、氮氧化物等)
17.⑴这些汽油完全燃烧产生的热量为:
Q汽油=4.6×107J/kg×15kg=6.9×108J
⑵根据题意知,氢气与汽油完全燃烧产生德热量相同,即
Q氢气=Q汽油 ,需要电解水的质量44.1Kg
16.设a mL水样中含溶解O2的质量为xg,根据有关反应方程式,已知物质与注物质的关系为:
O2 - 2MnO(OH)2 - 2I2 - 4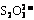 (4分)
(4分)
32g 4mol
xg 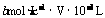
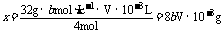 则溶解氧的计算式为:
则溶解氧的计算式为: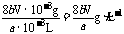
15.(1)2Na2O2+2CO2=2Na2CO3+O2
(2)③ 其一 条件简单,无需加热或通电
其二 该反应能吸收人呼出的CO2产生氧气
14. Cl2与H2O反应生成HClO,HClO具有杀菌和漂白作用,同时Fe2+被Cl2氧化成Fe3+水解生成具有吸附性的Fe(OH)3胶体,吸附水中悬浮杂质而达净水的目的。
Cl2+H2O H++Cl-+HClO 2Fe2++Cl2=2Fe3++2Cl-
H++Cl-+HClO 2Fe2++Cl2=2Fe3++2Cl-
Fe3++3H2O Fe(OH)3(
胶体)+3H+
Fe(OH)3(
胶体)+3H+
13.(1)乙学生 因为甲学生设计的装置,小试管套在大试管中,小试管中的空气不易排出,且氢气易从两试管空隙逸出(2)将大试管漫漫向上移动
(3)废干电池的锌皮和白醋 。
12.(1)10%-70% (2)这种说法只能表明收集德H2体积分数大于70%,而不是纯H2
讲析:(1)由表中可知:H2的体积分数为90%、80%时,能安静的燃烧, H2的体积分数小于10%时,不燃烧,其它含量均爆炸,因此混合气的爆炸可确定
11.D
1.B 2.C 3.D 4.B 5.C 6.B 7.D 8.D 9.A 10.C
2.(1)C6H10O5+6O2→6CO2+5H2O
(2)BOD为0.0112 g·L-1(3)鱼类不能正常保持生命
讲析:本题所述的内容在课内并未学过,而其涉及内容则并不复杂。
(1)配平方程式,此方程式可以看做为含氧有机物C6H10O5的“燃烧”方程式,因分子中H:O原子比符合2:1,则C→CO2所耗氧量即为完全氧化C6H10O5时的耗氧量:
C6H10O5+6O2→6CO2+5H2O
(2)计算BOD,将河水的密度近似看作1g·cm-3,则1L河水的C6H10O5的质量为:
m(C6H10O5)=10×10-5g/cm3=1×10-2g
根据化学方程式进行计算:
设1×10-2g有机物转化为无机物质需O2质量为m(O2)
m(O2)=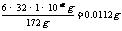
(3)与正常溶氧量比较:0.0112g·L-1>0.0092 g·L-1,即BOD大于水中的正常氧气量,故鱼类不能保持生命。
检测提高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com