
13.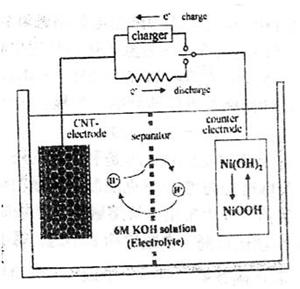 [江苏省前黄高级中学国际分校09届第一学期期末综合练习二]一种碳纳米管(氢气)二次电池原理如右图,该电池的电解质为6mol/LKOH溶液,下
[江苏省前黄高级中学国际分校09届第一学期期末综合练习二]一种碳纳米管(氢气)二次电池原理如右图,该电池的电解质为6mol/LKOH溶液,下
列说法正确的是 [BC] ( )
A.储存H2的碳纳米管作电池正极
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:
NiO(OH)+H2O+e-==Ni(OH)2+OH-
D.放电时,电池反应为2H2+O2→2H2O
w.w.w.k.s.5.u. c.o.m
12. [江苏省前黄高级中学国际分校09届第一学期期末综合练习二]下列离子反应方程式正确的是[D] ( )
[江苏省前黄高级中学国际分校09届第一学期期末综合练习二]下列离子反应方程式正确的是[D] ( )
A.用两个铜电极电解食盐水:2Cl-+2H2O 2HO-+H2↑+Cl2↑
B.李永刚腐蚀法制作印刷线路板:Fe3++Cu====Fe2++Cu2+
C.Ca(HCO3)2溶液中假如过量KOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
 D.AlCl3溶液呈酸性的原因:Al3++3H2O Al(OH)3+3H+
D.AlCl3溶液呈酸性的原因:Al3++3H2O Al(OH)3+3H+
11.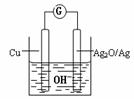 [江苏省前黄高级中学国际分校09届第一学期期末综合练习二]普通水泥在固化过程中自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是[C]
[江苏省前黄高级中学国际分校09届第一学期期末综合练习二]普通水泥在固化过程中自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是[C]
A.工业上以黏土、石灰石和石英为主要原料来制造普通水泥
B.负极的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O
C.测量原理示意图中,电流方向从Cu→Ag2O
D.电池工作时,OH-向正极移动
10.[江苏省前黄高级中学国际分校09届第一学期期末综合练习二]下列有关金属腐蚀与防护的说法正确的是 [AC]
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
9、[江苏省前黄高级中学国际分校09届上学期综合练习一] LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 负极 Li-e-== Li+
下列说法中不正确的是[ D ]
A.充电时电池反应为:LiFePO4= FePO4+Li
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时,Li+向正极移动
|
 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m8.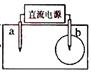 [江苏省前中国际分校2009届高三第一学期第一次调研试卷]取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是 [ D]
[江苏省前中国际分校2009届高三第一学期第一次调研试卷]取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是 [ D]
A.b电极是阴极 B.a电极与电源的正极相连
C.b电极附近溶液的pH变大 D.电解过程中水是还原剂
7.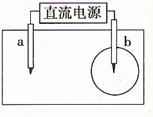 [江苏省前黄高级中学国际分校09姐上学期综合练习三]取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现b电极与试纸接触处出现一个双色同心圆,内圆为白色,外圆呈浅红色。则下列说法错误的是
[江苏省前黄高级中学国际分校09姐上学期综合练习三]取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现b电极与试纸接触处出现一个双色同心圆,内圆为白色,外圆呈浅红色。则下列说法错误的是
A.a电极是阴极 B.b电极与电源的正极相连接
C.电解过程中,水是氧化剂 D.a电极附近溶液的pH变小
6.[09届江苏省前黄高级中学国际分校期末化学综合练习四](10分)工业合成氨与制备硝酸一般可连续生产,流程如下:
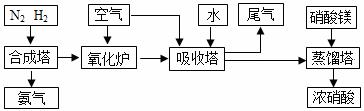
(1)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式 。
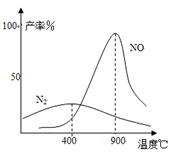 (2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图所示):
(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图所示):
4NH3+5O2 4NO+6H2O K1=1×1053(900℃)
4NO+6H2O K1=1×1053(900℃)
4NH3+3O2 2N2+6H2O K2=1×1067(900℃)
2N2+6H2O K2=1×1067(900℃)
温度较低时以生成 为主,温度高于900℃时,
NO产率下降的原因 。
吸收塔中需要补充空气的原因 。
(3)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收
剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NO和NO2的去除率高达99.95%。其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2 和N2请写出有关反应化学方程式:
, 。
答案.(1) N2+6e-+6H+=2NH3 (2分)
(2) N2 (1分) 生成NO的反应为放热反应,升高温度转化率下降 (2分)
进一步与NO反应生成硝酸(2分)
(3) NO+NO2+H2O=2HNO2;(1分) CO(NH2)2+2HNO2=CO2+2N2+3H2O(2分)
5.[09届江苏省前黄高级中学国际分校期末化学综合练习四]甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电源正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙。则下列叙述正确的是 ( )
A.甲、丙中是化学能转变为电能,乙中是电能转变为化学能
B.C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应
C.C1和C3放出的气体相同,铜片和铁片放出的气体也相同
D.甲、乙中溶液的PH值逐渐升高,丙中溶液的PH值逐渐减小
4. [ 江苏省泗阳致远中学2009届高三化学综合模拟试卷二]肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃
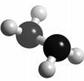 电池。已知肼的球棍模型如右图所示,下列有关说法正确的是
电池。已知肼的球棍模型如右图所示,下列有关说法正确的是
A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为: N2H4(g)+O2(g) = N2(g) +2H2O(g);△H=-642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com