
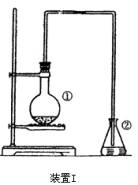

将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3-5分钟后发现滴有AgNO3的锥形瓶中有浅黄色沉淀生成,即证明苯与溴发生了取代反应。
(A)装置I中①的化学方程式为_________________________________。
②中离子方程式为_______________________________________。
(B)①中长导管的作用是____________________________________。
(C)烧瓶中生成的红褐色油状液滴的成分是____________________,要想得到纯净的产物,可用_________试剂洗涤。洗涤分离粗产品应使用的最主要仪器是_______________。检验产物已纯净的方法是_________。
(D)甲做实验时,乙观察到烧瓶中液体沸腾并有红棕色气体从导管口逸出,提出必须先除去红棕色气体,才能验证锥形瓶中的产物。产生红棕色气体的原因是___________。
该红棕色气体会干扰反应产物的验证,请说明干扰的原因并用相关的化学方程式表示:______________
____。
(E)乙同学设计右图所示装置Ⅱ,并用下列某些试剂完成该实验。可选用的试剂是:苯、液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。
a的作用是_____________________________。
b中的试剂是___________________________。
比较两套装置,装置Ⅱ的主要优点是________________。
第十四章 糖类 蛋白质
第一课时 糖类
【考纲要求】
3.为探究苯与溴的取代反应,甲用右图装置I进行如下实验:
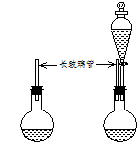 |
|||||
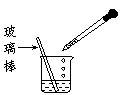 |
 |
||||
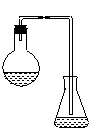
A B C D
(B)步骤②中如何判断“反应完全”______________________。
(C)步骤③中补充少量四氢化萘的目的是__________________。
(D)步骤③中过滤后得到的固体物质是___________________。
(E)已知在实验条件下,饱和氢溴酸水溶液中氢溴酸的质量分数是66%,如果溴化反应进行完全,则步骤①中四氢化萘和水的质量比约是1:______________(保留小数点后1位。)
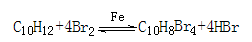 液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:
液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:
生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液;实验步骤如下:
①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉
②慢慢滴入液溴,不断搅拌,直到反应完全。
③取下反应容器,补充少量四氢化萘直到溶液颜色消失。过滤,将滤液倒入分液漏斗静置。
④分液,得到的“水层”即氢溴酸溶液。
回答下列问题:
(A)下列示意图中的装置,适合步骤①和②操作的是________________。
2. 1,2,3,4-四氢化萘的结构简式是 分子式是C10H12。常温下为无色
1.昆虫能分泌信息素。下列是一种信息素的结构简式:CH3(CH2)5CH=CH(CH2)9CHO
指出该物质中的任意一种官能团,为该官能团提供一种简单的鉴别方法并简述实验现象,写出与鉴别方法有关反应的化学方程式并指出反应类别,完成下表。
官能团
鉴别方法及实验现象
有关反应的化学方程式
反应类别
5.实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中。
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀。
③在50-60℃下发生反应,直至反应结束。
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤。
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
填写下列空白:
(A)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是:_______。
(B)步骤③中,为了使反应在50-60℃下进行,常用的方法是_________。
(C)步骤④中洗涤、分离粗硝基苯应使用的仪器是_____ __________。
(D)步骤④中粗产品用5%NaOH溶液洗涤的目的是________________。
(E)纯硝基苯是无色,密度比水_____(填“小”或“大”),具有_______气味的油状液体。
课外作业
4.(03年江苏高考题)无水乙酸又称冰醋酸(熔点16.6℃)。在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。答:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com