
7、各取三种未知液少许,分别滴入2滴酚酞试液,溶液显红色的原溶液为NaOH溶液,另取余下的两种未知液,分别向其中加入含有酚酞试液的NaOH溶液,可使溶液褪色的原溶液是盐酸,余下的原溶液为食盐溶液。
1.C 2.C 3.D 4.D 5.C 6.B
10.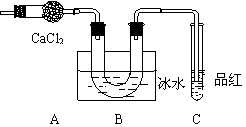 某学生设计如下实验,用于检验硫酸亚铁晶体(FeSO4·nH2O)分解产物并测定其结晶水的n值,步骤如下:
某学生设计如下实验,用于检验硫酸亚铁晶体(FeSO4·nH2O)分解产物并测定其结晶水的n值,步骤如下:
① 在质量为m1g的某容器中放入适量的
已研碎的硫酸亚铁晶体,再称量为m2g;
① 在隔绝空气的条件下,将晶体强热,
并将气态产物通过如下装置(设每步吸收均
是完全的),直至晶体全部变为红棕色粉末
为止,发现U形管底部有无色晶体析出,
品红溶液褪色。
③ 将红色粉末冷却至温室,称量(连容器)为m3g
④ 重复加热、冷却、称量、直至合格为止
回答下列问题:
(1) 第①步实验中盛放晶体的容器是(从下列选出)
A.坩埚 B. 蒸发皿 C. 烧瓶 D. 石英试管
(2) 第③步实验应如何冷却? ;
(3) 第④步实验称量合格的标准是 ;
(4) 求n值的计算式是 ;
(5) U形管中的晶体可能是什么物质?如何检验? ;
(6) 根据实验结果,写出FeSO4·nH2O分解化学方程式(化学计量数可用n表示)
第4讲 物质的检验、分离和提纯
例1、(1)pH试纸 (2)NaOH (3)HCl (4)蒸馏水
例2、D
例3从浓硫酸中取出铜片,用水洗干净后,放入稀硫酸中,如溶液呈蓝色,说明铜发生了钝化,否则没有钝化
例4(1)合理
(2)用磁铁吸引,若能吸附,说明有铁生成
(3)NaOH溶液 取少量样品放入试管,加入NaOH溶液, 有气泡产生,说明该熔融物中有铝。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
例5(1)Br2;Fe3+
(2)乙
|
实验方案 |
选用试剂(填代号) |
实验现象 |
|
方案一 |
C |
有机层无色 |
|
方案二 |
D |
溶液变红 |
(3)Fe2+;不可以,因为Br2和Fe3+都能把I-氧化成I2
课堂练习
9.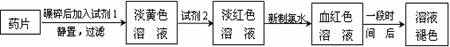 铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
⑴ 试剂1是 ,试剂2是 ,加入新制氯水后溶液中发生的离子反应方程式是
,
⑵ 加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为
写出+2价Fe在空气中转化为+3价Fe的化学方程式
;
⑶ 该同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗? 。
若你认为合理,请说明理由(若你认为不合理,该空不要作答)
若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不要作答) 。
8.设计一个用BaCl2溶液及试管鉴别Na2SO3溶液和稀H2SO4的实验,简要写出鉴别过程和实验结论。
7.如何用最简便的实验方法,只用酚酞试液就能鉴别出浓度均为0.1mol·L-1的食盐,盐酸和NaOH溶液,简述其实验方法和步骤。
6.蛇纹石由MgO、A12O3、Si02、Fe203组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是
A.沉淀X的成分是Si02
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3,
C.在溶液Y中加入过量的NaOH溶液,过滤,得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
5.下列有关实验所选用的试剂能达到目的的是 ( )
A.证明NaHCO3溶液中混有苏打用澄清石灰水 B.证明SO2中混有CO2用澄清石灰水 C.证明AgNO3溶液中混有Al(NO3)3用氨水 D.除掉C2H6中的C2H4用酸性KMnO4溶液
4.下列各组物质,不能用一种试剂区别开的是 ( )
A.二氧化锰、氧化铜、铁粉、炭粉 B.硫酸铵、氯化铵、氯化钠、硫酸钠
C.乙醇、四氯化碳、苯、已烯 D.苯、水、甲苯、二甲苯
3.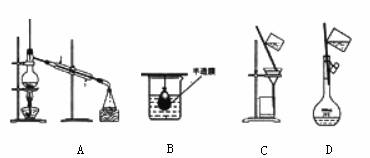 以下实验装置一般不用于分离物质的是
( )
以下实验装置一般不用于分离物质的是
( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com