
3.影响:只与 有关,
 [例6])将1.00molSO2(g)和1.00molO2(g)放入容积为1L的密闭容器中,在1000K达到平衡:2SO2(g) + O2(g) 2SO3(g),测得c(SO3)=0.925mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
[例6])将1.00molSO2(g)和1.00molO2(g)放入容积为1L的密闭容器中,在1000K达到平衡:2SO2(g) + O2(g) 2SO3(g),测得c(SO3)=0.925mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
[例7]在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应: H2(g)+I2(g)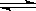 2HI(g),△H<0
2HI(g),△H<0
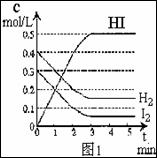
反应中各物质的浓度随时间变化情况如图1:
(1)该反应的化学平衡常数表达式为 ;
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为 ;
(3)反应达到平衡后,第8分钟时:①若升高温度,化学平衡常数K (填写增大、减小或不变)
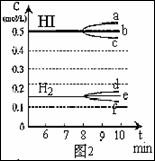
HI浓度的变化正确 ;(用图2中a-c的编号回答)
②若加入I2,H2浓度的变化正确的是 。(用图2中d-f的编号回答)
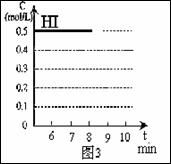
(4)反应达到平衡后,第8分钟时,若反容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。
 1.表达式:aA +bB c cC+dD K=
1.表达式:aA +bB c cC+dD K=
2. 意义:K的大小说明反应进行的程度(限度),K越大反应越
3.速率与平衡的关系
⑴υ正>υ逆,平衡向_____ 移动 ⑵υ正=υ逆,平衡_________移动
⑶υ正<υ逆, 平衡向_______移动
 [例5]在一定条件下,可逆反应:N2 + 3H2
2NH3;△H<0,达到平衡,当单独改变下列条件后,有关叙述错误的是( )
[例5]在一定条件下,可逆反应:N2 + 3H2
2NH3;△H<0,达到平衡,当单独改变下列条件后,有关叙述错误的是( )
A.加催化剂,正反应和逆反应速率都发生变化,且变化倍数相等。
B.加压,正反应和逆反应速率都增大,且正反应速率增大倍数大于逆反应速率增大的倍数
C.降温,正反应和逆反应速率都减小,且正反应速率减小倍数大于逆反应速率减小的倍数
D.恒容下充入Ar气,正反应和逆反应速率都增大,且正反应速率增大的倍数大于逆反应
2.化学平衡状态
⑴概念:
。
⑵特征:
⑶可逆反应达到平衡状态的标志:
[例3]哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生。下列有关说法正确的是 ( )
A 达到化学平衡时,N2将完全转化为NH3
B 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D 达到化学平衡时,正反应和逆反应的速率都为零
 [例4]下列方法中可以证明2HI H2
+ I2(g)已达到平衡状态的是
[例4]下列方法中可以证明2HI H2
+ I2(g)已达到平衡状态的是
①单位时间内生成了nmolH2的同时生成了nmolHI
②一个H-H键断裂的同时有两个H-I断裂 ③百分组成HI%=I2%
④反应速率υH2=υI2=1/2υHI时 ⑤温度和体积一定时,某一生成物浓度不变的状态
⑥c(HI)∶c(H2)∶c(I2)=2∶1∶1 ⑦温度和体积一定时,容器内压强不再变化的状态
⑧条件一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
 ⑩温度和压强一定时,混合气体密度不再变化
⑩温度和压强一定时,混合气体密度不再变化
[思考]在上述⑦-⑩的说法中,能说明2NO2 N2O4达到平衡状态的是____ _____。
1.可逆反应:在 条件下,既能向 又能向 方向进行的反应。
1. 能量判据(ΔH<0):多数自发进行的化学反应是放热反应
2. 熵判据(ΔS>0):熵增有利于自发,同一物质熵值:S(固) S(液) S(气)
3. 复合判据(△G = △H - T△S 0)
[思考]请填写下列表格(用自发反应,非自发反应,不一定)
|
|
ΔS >0 |
ΔS <0 |
|
ΔH >0 |
|
|
|
ΔH <0 |
|
|
[例1]下列变化过程中,ΔS<0的是( )
A.氯化钠溶于水中 B.NH3和HCl反应生成NH4Cl(固)
C.干冰的升华 D.碳酸钙分解为CaO和C02
[例2]以下自发反应可用能量判据来解释的是( )
A.硝酸铵自发地溶于水; B.2N2O5(g) = 4NO2(g)+ O2(g) △H=+56.7kJ/mol;
C.(NH4 )2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9 kJ/mol; D.2H2(g)+ O2(g)=2H2O(l) △H=-571.6 kJ/mol。
教学过程动态化
教学过程动态化的研究,主要是要处理好课堂教学中预设与生成的问题。“课程标准”指出:“教学是预设与生成、封闭与开放的矛盾统一体”。现在人们普遍认为:一堂成功、有效的课堂既离不开预设,也不能没有生成。完全按照预设进行教学,就会导致忽视学生学习的主动性,影响学生的思维发展;但如果一味追求课堂上的即时“生成”,也许课堂会热热闹闹,但可能会因为缺乏目标,而出现“随波逐流”的现象。
华东师范大学叶澜教授就什么是理想课堂,曾经做过这样精辟的论述:“课堂应是向未知方向挺进的旅程,随时都有可能发现意外的通道和美丽的图景,而不是一切都必须遵循固定线路而没有激情的行程”。
课堂教学是师生在特定情景中的交流和对话,是动态的、即时的。备课再仔细,预设再充分,教师也无法预计课堂中可能会发生的一切。在整个教学过程中,随着教学活动的展开,教师、学生的思想和教学文本不断碰撞,精神、情感不断交流,创造火花不断迸发,新的学习需求、方向不断产生,认识和体验不断加深,随时都可能出现教师预料不到的情况和问题,这些预料不到的情况和问题就是必须关注的生成性内容。教师要在课堂教学过程中善于把这种生成性内容看作新的教学资源,及时调整教学预设,形成新的教学方案。下面是一个典型的课堂“生成”教学案例。
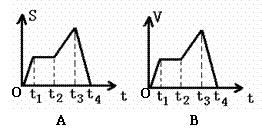 在今年的“运动图像”习题课上,我设计如图所示的两个曲线图形,希望通过分析讲解,帮助学生区别 “匀变速直线运动的速度--时间图像和位移--时间图像”的物理意义。然而在讲完本题后,并没有达到期望的效果,仍然有一部分同学表示不能理解。我本想用准备好的多媒体课件展示它们的区别,此时有一位同学示意他可以用走动的方法表示它们的区别,我请他说出方法,他走到讲台中间,向同学们介绍他的做法,接着他先按图A的图像走动(边走边讲解):向教室门口方向走去(0-t1时段),停了几秒钟(t1-t2时段),又向门口走去(t2-t3时段),再接着又转身走回开始的位置(t3-t4时段);又按图B的图像走动:先加速小跑几步(0-t1时段),接着匀速走几步(t1-t2时段),又加速跑几步(t2-t3时段),然后还是向前越来越慢的走几步(t3-t4时段),直至停下。他的这种表示方法,同学们用热烈的掌声表示赞赏,好多同学产生了浓厚的兴趣,纷纷举手要求上台走动。我深受启发,立即改变原来的设计,同意让几个同学上台表演,大部分同学都能正确表示,也有几个在t3-t4时段出现错误,经过下面同学大声的指正,最后都表示能理解这两个图像的区别。由于本节课学生独特的表示方法,引起了其他同学极大的兴趣,课堂气氛相当活跃,学生不仅理解了两种图像的物理意义,大大增强了他们的参与热情,效果比多做几道习题好得多。
在今年的“运动图像”习题课上,我设计如图所示的两个曲线图形,希望通过分析讲解,帮助学生区别 “匀变速直线运动的速度--时间图像和位移--时间图像”的物理意义。然而在讲完本题后,并没有达到期望的效果,仍然有一部分同学表示不能理解。我本想用准备好的多媒体课件展示它们的区别,此时有一位同学示意他可以用走动的方法表示它们的区别,我请他说出方法,他走到讲台中间,向同学们介绍他的做法,接着他先按图A的图像走动(边走边讲解):向教室门口方向走去(0-t1时段),停了几秒钟(t1-t2时段),又向门口走去(t2-t3时段),再接着又转身走回开始的位置(t3-t4时段);又按图B的图像走动:先加速小跑几步(0-t1时段),接着匀速走几步(t1-t2时段),又加速跑几步(t2-t3时段),然后还是向前越来越慢的走几步(t3-t4时段),直至停下。他的这种表示方法,同学们用热烈的掌声表示赞赏,好多同学产生了浓厚的兴趣,纷纷举手要求上台走动。我深受启发,立即改变原来的设计,同意让几个同学上台表演,大部分同学都能正确表示,也有几个在t3-t4时段出现错误,经过下面同学大声的指正,最后都表示能理解这两个图像的区别。由于本节课学生独特的表示方法,引起了其他同学极大的兴趣,课堂气氛相当活跃,学生不仅理解了两种图像的物理意义,大大增强了他们的参与热情,效果比多做几道习题好得多。
信息传输多样化
课堂教学是师生在特定情景中的信息传输、交流和反馈的过程。组成教学过程的基本因素包括教师、学生、教学内容、教学媒体,它形成了一个相互联系和相互作用的课堂教学信息系统。从信息论上说,课堂教学是由师生共同创设的一个动态的、开放的信息传递系统。传统教学中教师在课堂上是信息发布者,信息源单一,课堂信息交流是以教师讲和学生听的单向、线性信息传输方式为主,学生处于被动接受信息,抑制了学生思维的发展,阻碍了学生主体性的发挥;随着高中新课程改革的进行,特别是随着信息技术的发展,现在的课堂里,教师的作用不再是信息发布者,而是为课堂教学提供一个信息平台,教学过程就是通过师--生、生--生、人--机等的互动、对话和交流,实现信息的多向、非线性传输,这种多向、非线性传输方式,使学生个体自我反馈、学生群体间信息碰撞、师生间信息反馈、交流及时普遍地联系起来,使学生通过探究学习、合作学习,相互启发、互相帮助、相互补充,达到共识、共享、共进,使课堂教学成为学生主体活动展开与整合的过程。
实现课堂信息传输多样化,首先要建立平等、民主、和谐的师生关系,创设合适的问题情境,提供宽松的课堂平台。在这样的环境中,师生都可充分展示其个性特长,观点能自由表达,信息可以彼此交流,思维发生碰撞,从而产生新的思想,形成新的知识结构,达到共同提高。
实现课堂内信息传输多样化,需要科学合理的运用现代化教育技术手段。信息技术的飞速发展,为课堂信息非线性、多向交流提供了强大的技术支撑。一方面师生能及时从互联网中获取大量有用的最新信息,丰富师生的知识面,为课堂信息交流提供很多信息源;另一方面,多媒体教学平台和多媒体网络系统,又为课堂信息交流和反馈提供新的方式,使信息交流、传输和反馈更直接,更及时、更能引起新信息的产生和新思想的形成。
实现课堂内信息传输的多样化,要求教师善于引导和调控课堂信息传输与反馈的方向,避免与教学内容无关的信息影响有用信息的效度,使信息的传输和反馈有利用思维的碰撞和新信息的产生,有利于教学目标的实现。
目标实施个性化
新课标提出:“促进满足每个学生的个性差异,促进每个学生全面而有个性的发展,是普通高中课程改革的根本价值尺度。”《教育--财富蕴藏之中》中也指出:“使人日臻完善,使他的性格丰富多彩,表达方式复杂多样;使他作为一个人,作为一个家庭和社会的成员,作为一个公民和生产者、技术发明者和有创造性的理想家,来承担各种不同的责任。”这都说明在课堂教学中,要充分关注学生的个体差异,使教学目标实施满足学生的个性发展。
“多元智力理论”表明:学生与学生之间存在着差异,每个学生都有独特的心理特点。在教学中,教师要善于发现和尊重学生的个体差异,培养和张扬学生的个性特长,把学生的个体差异作为一种教育资源加以开发和利用,通过学生的个性发展来实现学生的全面发展。
目标实施个性化首先要求教师能为学生提供施展个性的空间。教师要给学生营造一个积极向上、崇尚创新、张扬个性的良好课堂环境,让学生有广阔的心理空间和心灵自由,使他们的个性得到充分的发展。教师可根据教学目标需要和教学内容特点,结合自己的教学风格,少一些满堂灌,多一些指导,多设计一些能为学生个性发挥的问题情境,引起学生产生各种不同疑问,提出不同的问题,再在教师的引导下,学生根据自己生活经验、原有基础,采用不同的思维方法,寻找不同的解决问题途径。
目标实施个性化需要教师采用各种不同的教学方式,为学生提供更多主动学习的机会,如采用自主探究学习方式、协作学习方式、讨论式学习方式等等。在这些不同学习方式中,学生能扬长避短,发挥优势,用最适合自己发展的方式学习,使自己处在主动求知过程中,真正实现知识建构、经历过程和情感体验的全方位提高。
目标实施个性化还需要教师采用个性化的评价方式。新课标提倡对学生采用发展性的评价方式,通过评价促进学生全面而有个性的发展。发展性学生评价内容不仅是学生的学业成绩,还包括学生的心理素质、学习兴趣、情感体验、创新精神、实践能力、道德品质、学习风格、心理优势、人际关系、自我评价等。课堂上通过适当的评价方法,对学生的发展进行价值判断,使学生不断展示自己独特的个性特点,发挥个性特长;使学生认识自我、发展自我、完善自我,促进自己全面而有个性的发展。
高中新课程改革还刚刚处于初级阶段,很多新的教育理念还需要一定的时间,通过一定的手段才能转化为教育行动。对我们来说,落实新课标的课堂教学研究也才刚刚开始,以上所研究的内容还需要进一步深入研究,同时课堂教学的生活化、课堂互动的有效性、教学评价的激励性等问题也将成为我们以后课堂教学研究的重点。我们希望通过课堂教学改革,使每一个学生都能全面而有个性地发展,为学生的终身学习打下坚实的基础。
6.(2009安徽卷26)
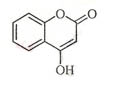 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
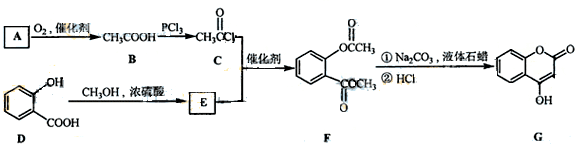
(1)A与银氨溶液反应有银镜生成,则A的结构简式是 。
(2)B→C的反应类型是 。
(3)E的结构简式是 。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
。
(5)下列关于G的说法正确的是 。
a.能与溴单质反应 b.能与金属钠反应
c.1molG最多能和3mol氢气反应 d.分子式是C9H6O3
[答案](1)CH3CHO (2)取代反应
 (3)
(3)


(4) +3NaOH → +CH3COONa +CH3OH +H2O
(5)a、b、d
 [解析](1)A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知,A与氧气反应可以生成乙酸,则A为CH3CHO;
[解析](1)A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知,A与氧气反应可以生成乙酸,则A为CH3CHO;
(2)由B和C的结构简式可以看出,乙酸分子中的羟基被氯原子取代,发生了取代反应;
(3)D与甲醇在浓硫酸条件下发生酯化反应生成E,E的结构为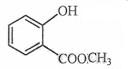 ;
;
(4)由F的结构简式可知,C和E 在催化剂条件下脱去一个HCl分子得到F,F中存在酯基,在碱液中可以发生水解反应,方程式为: 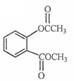 +3NaOH→
+3NaOH→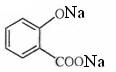 +CH3COONa+CH3OH+H2O;
+CH3COONa+CH3OH+H2O;
(5)G分子的结构中存在苯环、酯基、羟基、碳碳双键,所以能够与溴单质发生加成反应或者取代反应,能够与金属钠反应产生氢气,A和B选项正确;1molG中1mol碳碳双键和1mol苯环,所以需要4mol氢气,C选项错误;G的分子式为C9H6O3,D选项正确。
21世纪教育网
5.请用合成反应流程图表示出由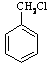 和其他无机物合成
和其他无机物合成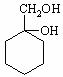 最合理的方案(不超过4步),请在答题纸的方框中表示。
最合理的方案(不超过4步),请在答题纸的方框中表示。
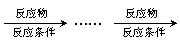 例:
例: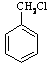

[答案]
 [解析]分析目标产物的结构可知,相邻碳上各引入一个羟基要引入碳碳双键。而
[解析]分析目标产物的结构可知,相邻碳上各引入一个羟基要引入碳碳双键。而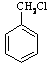 不能直接消去,必须先与氢气加成,再在氢氧化钠醇溶液中发生消去,要注意反应条件,再加成,再水解即可。
不能直接消去,必须先与氢气加成,再在氢氧化钠醇溶液中发生消去,要注意反应条件,再加成,再水解即可。
4.(2008徐州质检)已知:
现有只含碳、氢、氧的化合物A-F,有关它们的某些信息,已注明在下面的方框内。
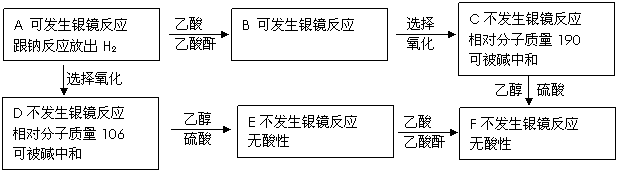
(1)在化合物A-F中有酯的结构的化合物是 。
(2)写出化合物A和F的结构简式。
[答案](1)B、C、E、F
(2)A:CH2(OH)CH(OH)CHO F:CH3COOCH-CH(OOCCH3)-COOC2H5
[解析]解答本题可从下面几方面入手:(1)弄懂题给信息 (2)能发生银镜反应说明分子内含有醛基,醛基易被氧化;能和乙酸、乙酸酐发生酯化反应说明分子内含有羟基(羟基也能和钠反应产生H2);可被碱中和、能和乙醇在浓硫酸存在的条件下发生酯化反应说明分子内含有羧基。这样可大致确定各物质所含有的官能团。(3)利用题中的数据,已知-CHO氧化为-COOH式量增加16,若A物质中只有1个醛基(若1个醛基不合理再讨论多个醛基),采用逆向思维方式从C→B,从D→A,推测A、B的相对分子质量为:M(A)=90、M(B)=174,A、B的相对分子质量之差等于84,表示A醇羟基形成乙酸酯时相对分子质量的增加,而信息说明每个醇羟基形成乙酸酯时相对分子质量增加42,由此推出A中含2个醇羟基。经过上述的推论再经综合分析可以得出结果。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com