
| A. | 加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,SO42- | |
| B. | 含有NaClO的溶液中:K+,Al3+,Br-,S2- | |
| C. | 澄清透明溶液:Cu2+、SO42-、HCO3-、H+ | |
| D. | 使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42- |
分析 A.加入Mg能放出H2的溶液为酸性溶液,四种离子之间不反应,都不与氢离子反应;
B.次氯酸根离子能够氧化溴离子、硫离子,硫离子与铝离子发生双水解反应;
C.铁离子、氢离子与碳酸氢根离子反应;
D.使甲基橙变红的溶液中为酸性溶液,酸性条件下高锰酸根离子能够氧化亚铁离子.
解答 解:A.加入Mg能放出H2的溶液中存在大量氢离子,Mg2+,NH4+,Cl-,SO42-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.Al3+、S2-之间发生双水解反应,具有还原性,Br-,S2-能够被次氯酸钠氧化,在溶液中一定不能大量共存,故B错误;
C.HCO3-与Cu2+、H+发生反应,在溶液中不能大量共存,故C错误;
D.使甲基橙变红的溶液中存在大量氢离子,Fe2+、MnO4-在酸性条件下能够发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 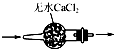 干燥SO2气体 | |
| B. | 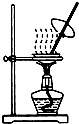 蒸发CH3COONa溶液得醋酸钠晶体 | |
| C. | 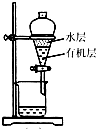 分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 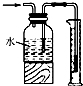 测量氯气的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L甲烷中含有的氢原子数为2NA | |
| B. | 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3NA | |
| C. | 常温常压下,2 g H2的分子数为NA | |
| D. | 常温常压下,1 mol/L MgCl2溶液中含Cl-数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用KSCN溶液检验${\;}_{26}^{45}$FeCl3和${\;}_{26}^{56}$FeCl3 | |
| B. | H2O与D2O互称同素异形体 | |
| C. | 副族元素中没有非金属元素,所以又称过渡金属 | |
| D. | F-与K两种微粒之间可以形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2NH3→2NaNH2+H2↑ | B. | NH3+HNO3→NH4NO3 | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| C. | 氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,与铜发生置换反应 | |
| D. | 晶体硅具有半导体的性质,所以可以制作光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:Na2CO3>NaHCO3>H2CO3 | B. | 溶解度:Na2CO3<NaHCO3 | ||
| C. | 熔点:Rb>K>Na>Li | D. | 还原性:Rb<K<Na<Li |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入HNO3酸化的Ba(NO3)2溶液 | |
| B. | 先加入HNO3酸化,再加Ba(NO3)2 | |
| C. | 加入盐酸酸化的BaCl2 | |
| D. | 先用盐酸酸化,若有沉淀,则过滤,滤液中再加BaCl2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com