
| A、可以用NaOH溶液来检验FeCl3溶液中混有的Fe2+ |
| B、受NH4+检验方法的启发,可以通过将NO3-转化成NO的方式来检验 |
| C、取待测液于试管中,先加稀硝酸酸化,再加Ba(NO3)2溶液,若产生白色沉淀,则待测液中一定有SO42- |
| D、取待测液于试管中,加入足量的稀盐酸,若产生使澄清石灰水变混浊的无色无味气体,则待测液中一定有大量CO32- |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
| A、150mL 1mol/L的NaCl |
| B、75mL 1mol/L的FeCl3 |
| C、150mL 3mol/L的KCl |
| D、75mL 2mol/L的CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、②④⑤ |
| C、①②⑤ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加入KSCN溶液 | 固体物质中有FeCl3 | |
| 在酸性KMnO4溶液中加入少量A | KMnO4溶液颜色无明显变化 | 固体物质中不含 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
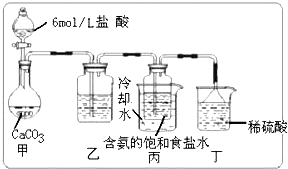
查看答案和解析>>
科目:高中化学 来源: 题型:
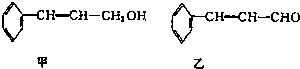
| 分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl2褪色能在稀硫酸中水解 |
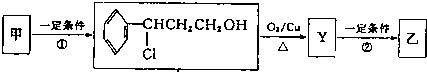
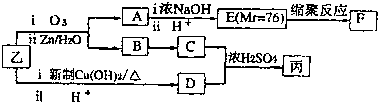
| ⅰO2 |
| ⅱZn/H2O |
| ⅰ浓NaOH |
| ⅱH+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na在Cl2中燃烧制NaCl |
| B、氯气溶于水制盐酸 |
| C、Cl2与石灰乳作用制漂白粉 |
| D、H2和Cl2混合光照制HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.40 | 19.95 |
| 醋酸浓度(mol?L-1) | 0.0010 | 0.01000 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.83 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com