
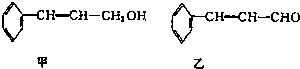
| 分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl2褪色能在稀硫酸中水解 |
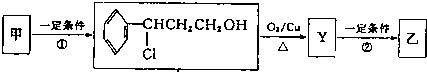
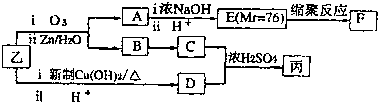
| ⅰO2 |
| ⅱZn/H2O |
| ⅰ浓NaOH |
| ⅱH+ |
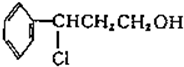 ,
, 发生氧化反应生成Y,Y发生消去反应生成乙;
发生氧化反应生成Y,Y发生消去反应生成乙; ,A结构简式为OHCCHO;
,A结构简式为OHCCHO;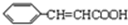 ,
,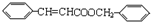 ,据此分析解答.
,据此分析解答. ,
, 发生氧化反应生成Y,Y发生消去反应生成乙,
发生氧化反应生成Y,Y发生消去反应生成乙, ,A结构简式为OHCCHO;
,A结构简式为OHCCHO;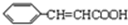 ,
,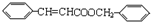 ,
, ,故答案为:
,故答案为: ;
;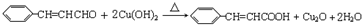 ,
,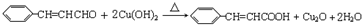 ;
;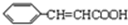 ,其同分异构体符合下列条件,
,其同分异构体符合下列条件,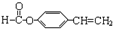 ,
, ;
;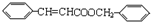 ,故答案为:
,故答案为: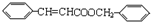 .
.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可以用NaOH溶液来检验FeCl3溶液中混有的Fe2+ |
| B、受NH4+检验方法的启发,可以通过将NO3-转化成NO的方式来检验 |
| C、取待测液于试管中,先加稀硝酸酸化,再加Ba(NO3)2溶液,若产生白色沉淀,则待测液中一定有SO42- |
| D、取待测液于试管中,加入足量的稀盐酸,若产生使澄清石灰水变混浊的无色无味气体,则待测液中一定有大量CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 检测次数 | 溶液中检测出的溶质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2CO3、K2CO3 |
| 第三次 | Na2CO3、KCl、K2SO4、NaCl |
2- 4 |
2- 3 |
| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 | ||
| 第一步 | 向溶液中滴加过量的HNO3溶液 | 检验 | |||
| 第二步 | 继续滴加过量的 | 检验SO
| |||
| 第三步 | 过滤、再向滤液中滴加 | 检验 | Ag++Cl-=AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
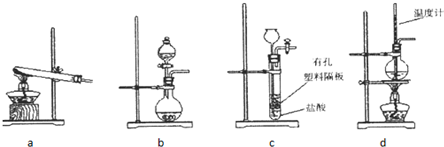
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com