
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p1${\;}^{2{2}^{3}}$③1s22s22p2④1s22s22p63s23p4 原子半径最大的是① | |
| B. | 具有下列价电子排布式的原子中,①3s23p1 ②3s23p 2 ③3s23p3 ④33s23p 4第一电离能最大是③ | |
| C. | ①Na、K、Rb ②N、P、Si ③Na、P、Cl,元素的电负性随原子序数增大而递增的是③ | |
| D. | 某主族元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+ |
分析 A.同周期,自左而右原子半径减小,同主族,自上而下原子半径增大;
B.同周期,随原子序数增大第一电离能呈增大趋势,ⅤA族3p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素;
C.同周期,自左而右电负性增大,同主族,自上而下电负性减小;
D.该元素第三电离能剧增,最外层应有2个电子,表现+2价.
解答 解:A.核外电子排布:①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,则①为Si、②为N、③为C、④为S,同周期,自左而右原子半径减小,同主族,自上而下原子半径增大,故原子半径:Si>C>N,Si>S,故Si原子半径最大,即①的原子半径最大,故A正确;
B.同周期,随原子序数增大第一电离能呈增大趋势,ⅤA族3p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能,③>④>②>①,故B正确;
C.同周期自左而右电负性增大,同主族自上而下电负性减小,故①Na、K、Rb电负性依次减小,②N、P、Si的电负性依次减小,③Na、P、Cl的电负性依次增大,故C正确;
D.该元素第三电离能剧增,最外层应有2个电子,表现+2价,当它与氯气反应时最可能生成的阳离子是X2+,故D错误;
故选D.
点评 本题考查核外电子排布、微粒半径比较、电离能与电负性等,难度中等,注意理解电离能与元素化合价关系、同周期第一电离能发生突跃原理.


科目:高中化学 来源: 题型:选择题
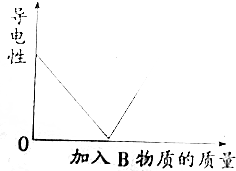 向某A溶液中加入一种物质B,其导电能力变化与加入B物质的质量关系符合如图曲线的是( )
向某A溶液中加入一种物质B,其导电能力变化与加入B物质的质量关系符合如图曲线的是( )| A. | 盐酸中滴加Ba(OH)2溶液至过量 | |
| B. | CaCl2溶液中滴加浓Na2CO3溶液至过量 | |
| C. | AgNO3溶液中滴加NaCl溶液至过量 | |
| D. | 稀硫酸中滴加Ba(OH)2溶液至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
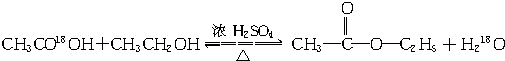 .
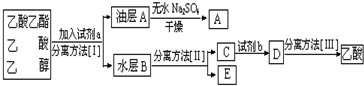
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
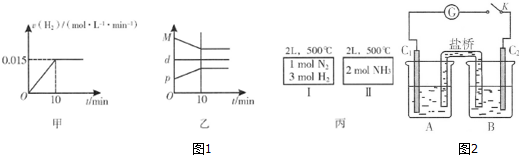
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
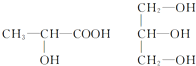 按要求完成下列问题.
按要求完成下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、101KPa条件下,1摩尔任何气体的体积都是22.4升 | |
| B. | 同质量的O2和O3所含的氧原子数不相同 | |
| C. | 同温同压下两种气体,只要分子数相同,所占体积相同,质量也相同 | |
| D. | 标准状况下,体积是22.4升的物质,其物质的量可能是1摩尔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com