
 �黯��Ϊ�������뵼����ϣ������ṹ��ͼ��ʾ��
�黯��Ϊ�������뵼����ϣ������ṹ��ͼ��ʾ��| m |
| V |
| 700�� |
| 700�� |
 ������������ı߳�Ϊx��CE�ij�Ϊ0.5x��BE=
������������ı߳�Ϊx��CE�ij�Ϊ0.5x��BE=| x2-(0.5x)2 |
| ||
| 2 |
| ||
| 2 |
| 2 |
| 3 |
| ||
| 3 |
x2-(
|
| ||
| 3 |
| ||
| 3 |
a2-(
|
| 2 |
| 3 |
| 6 |
| ||
| 2 |
| 2 |
| 4 |
| 3 |
| 3 |
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
| ||||
(
|
3
| ||
| 16a3NA |
3
| ||
| 16a3NA |


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH-����С |
| B��CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ� |
| C��������Һ������Ũ�ȵĹ�ϵ���㣺c��H+��=c��OH-��+c��CH3COO-�� |
| D��������pH=2��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ���Һ��pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ | B��������þ |
| C��̼���� | D��̼��þ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
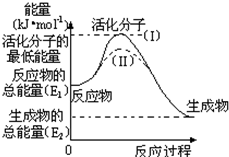 �ڻ�ѧ��Ӧ�У���������ѧ��Ӧ�ķ��Ӽ���ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ����������л�ܣ��䵥λ��kJ?mol-1��ʾ��������۲�ͼ��Ȼ��ش����⣮
�ڻ�ѧ��Ӧ�У���������ѧ��Ӧ�ķ��Ӽ���ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ����������л�ܣ��䵥λ��kJ?mol-1��ʾ��������۲�ͼ��Ȼ��ش����⣮| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
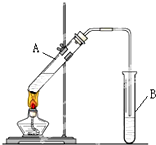 ��ϩ��������������ʯ�ͺ�ú�Ļ�������ԭ�ϣ��Ҵ������������������г������л������
��ϩ��������������ʯ�ͺ�ú�Ļ�������ԭ�ϣ��Ҵ������������������г������л�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ӳɷ�Ӧ | B���ֽⷴӦ |
| C��������Ӧ | D��ȡ����Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com