
Ⅰ(本题9分)乙酸乙酯是重要的工业原料和溶剂,通常混有少许乙醇和乙酸。某学习小组利用图1装置制取乙酸乙酯粗产品,再分析乙酸乙酯的含量。

| 乙酸乙酯 | 乙醇 | 乙酸 |
沸点 | 77.1℃ | 78.5℃ | 117.9℃ |
操作步骤如下:
(I)准确称量20.0g乙酸乙酯粗品于锥形瓶中,用0.50mol/LNaOH滴定(酚酞做指示剂)。终点时消耗NaOH溶液的体积为40.0mL
(II)另取20.0g乙酸乙酯粗产品于250mL锥形瓶中,加入100mL 2.1mol/LNaOH溶液混合均匀后,装上冷凝箱,在水浴上加热回流约1小时,装置如图2所示。待冷却后,用0.50mol/LHCl滴定过量的NaOH。终点时消耗盐酸的体积为20.0mL。
回答下列问题:
(1)实验(II)中冷水从冷水凝管的 (填a或b)管口通入。
(2)利用实验(I)、(II)测量的数据计算粗产物中乙酸乙酯的质量分数为 。
(3)实验结束后,同学们对粗产品中乙酸乙酯的含量不高进行讨论。
①有人认为是实验(II)带来的误差。建议将图2中的锥形瓶改为三颈瓶,装置如图3,在三颈瓶的c、d口装配相关的仪器并进行恰当的操作,可以提高测定的精确度。你认为在三颈瓶的c、d口装配相关的仪器或操作是: (填字母);
A.装上温度计,严格控制反应温度
B.实验中经常打开瓶口,用玻璃进行搅拌
C.在反应后期,用事先安装的分液漏斗添加一定量的NaOH溶液
②还有同学认为改进乙酸乙酯的制取装置(图1)才能提高产率。拟出你的一条改进建议
Ⅱ(本题6分)如图是配制50 mL酸性KMnO4标准溶液的过程示意图。

(1)请你观察图示判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是____________________________________(填名称)。
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将________(填“偏大”或“偏小”)。
Ⅰ.(1)b;(2)79.2﹪;(3)①A、C;②用圆底烧瓶替代试管并加装温度计控制反应温度或加装水冷凝管,提高冷却效果。Ⅱ.(1)②⑤;(2)50mL容量瓶;(3)偏大。
【解析】
试题分析:(1)为了增强冷凝效果,在实验(II)中冷水从冷水凝管的下口b管口通入。(2)n(NaOH)=0.50mol/L×0.04L=0.02mol;所以n(CH3COOH)= 0.02mol,其质量是1.2g;在(II)中可知乙酸与乙酸乙酯的物质的量的和为:0.100L× 2.1mol/L-0.50mol/L×0.02L=0.2mol,所以n(乙酸乙酯)= 0.2mol -0.02mol=0.18mol,m(乙酸乙酯)=0.18mol×88g/mol=15.84g。所以测量的数据计算粗产物中乙酸乙酯的质量分数为(15.84g÷20.00g) ×100﹪=79.2﹪;(3)装上温度计,严格控制反应温度 ;在反应后期,用事先安装的分液漏斗添加一定量的NaOH溶液,所以选项是A、C;②改进乙酸乙酯的制取装置的建议是用圆底烧瓶替代试管并加装温度计控制反应温度或加装水冷凝管,提高冷却效果等。Ⅱ(1)图示判断不正确的操作有②在量筒中溶解物质和⑤仰视读数;(2)其中确定50 mL溶液体积的容器是50mL的容量瓶;(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,由于溶液的体积偏小,所以所测得的实验结果将偏大。
考点:考查仪器的所用、物质纯度的计算、装置的设计与改进、误差分析等化学实验基本操作的知识。


科目:高中化学 来源:2015届辽宁省鞍山市高二下学期期末考试化学(B卷)试卷(解析版) 题型:选择题
某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原HNO3的物质的量之比为2∶1时,还原产物可能是
A.N2O B.NO C.NO2 D.N2
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省鞍山市高二下学期期末考试化学(A卷)试卷(解析版) 题型:选择题
在预防SARS时,医学专家告诉我们对公共场所要进行消毒,毛巾、口罩要经常用开水蒸煮,被褥要放在太阳光下直射,其目的是
A.使多糖水解B.使油脂水解C.使氨基酸变性D.使蛋白质变性
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高三上学期期初检测化学试卷(解析版) 题型:选择题
铁是一种应用广泛的金属。下列有关铁的说法正确的是
A.铁与盐酸反应生成氯化铁和氢气 B.常温下铁在浓硫酸中钝化
C.铁在氧气中燃烧生成物为三氧化二铁 D.纯铁(块状)是黑色金属
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高三上学期期初检测化学试卷(解析版) 题型:选择题
以下化学用语正确的是
A.甲醛的结构式: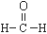 B.乙醇的分子式: CH3CH2OH
B.乙醇的分子式: CH3CH2OH
C.乙烯的结构简式: CH2CH2 D.苯的实验式: C6H6
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省抚顺市六校联合体高二下学期期末考试化学试卷(解析版) 题型:选择题
分析下表中各项的排布规律。有机物X是按此规律排布的第19项,下列有关X的组成、性质的说法中肯定错误的是( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
①是戊酸 ②是戊醇 ③是丁酸甲酯 ④在稀硫酸中易变质 ⑤一定能与钠反应
A.②⑤ B.①③④ C.③④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三8月月考理综化学试卷(解析版) 题型:填空题
(14分)有A、B、C、D四种物质,B的焰色反应为黄色。C是酸式盐,C加入硝酸酸化的Ba(NO3)2溶液中有白色沉淀生成。D和G相遇有大量白烟生成,D通入硝酸酸化的AgNO3溶液有白色沉淀生成。对A、B、C、D四种物质的水溶液进行下列实验,过程和现象如下图所示(图中部分产物未列出),请回答下列问题:

(1)B的电子式为____________________。
(2)H生成I的化学方程式为 。
(3)G在同主族同类物质中稳定性最强____,也是沸点最高的 。(判断正误填“是”或“否”)
(4)A溶液中加入D,A溶液的颜色由浅绿色变黄,则A的化学式为__________ 。
(5)写出C与过量B反应(加热)的离子方程式 。
(6)C与D溶液恰好反应,假设生成气体全部逸出,所得溶液中离子浓度从大到小的顺序 。
(7)25℃时pH=9的B溶液和pH=9的G溶液中,水的电离程度B___________G(填>,<或=)。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:选择题
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2===LiNH2+LiH,下列有关说法正确的是( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com