
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
29£®(22·Ö)ĻÖÓŠ×čÖµRĪŖ10.0¦øµÄ¶ØÖµµē×č2øö”¢æŖ¹Ų2øö”¢ČōøÉøłµ¼ĻßŗĶ1øöµēĮ÷±ķ£¬øƵēĮ÷±ķ±ķĆęÉĻÓŠæĢ¶Čµ«ĪŽæĢ¶ČÖµ£¬ŅŖĒóÉč¼ĘŅ»øöÄܲā¶ØijµēŌ“ÄŚ×čµÄŹµŃé·½°ø(ŅŃÖŖ
”” µēĮ÷±ķµÄÄŚ×čæÉŗöĀŌ²»¼Ę£¬µēĮ÷±ķĮæ³ĢæÉŅŌĀś×ć²āĮæµÄŅŖĒ󣬵ēŌ“ÄŚ×čŌ¼ĪŖ¼øÅ·).
”” (1)ŌŚÓŅĆęµÄ·½æņÄŚ»³öŹµŃéµēĀ·Ķ¼£»
”” (2)¼ņŅŖŠ“³öĶź³É½ÓĻßŗóµÄŹµŃé²½Öč£»
”” (3)Ķʵ¼ÓĆ²āµĆµÄĮæ¼°¶ØÖµµē×čR¼ĘĖć
µēŌ“ÄŚ×čµÄ±ķ“ļŹ½.
28£®(16·Ö)ŹµŃéŹŅĮŁŹ±ŠčŅŖÓĆNaOHČÜŅŗŗĶCO2Ą“ÖĘČ”“æNa2CO3ČÜŅŗ”£ŅŃÖŖCO2ĘųĢåŌŚĶØČėNaOHČÜŅŗŹ±¼«Ņ×ŅņĘä¹żĮæ¶ųÉś³ÉNaHCO3£¬ĒŅĪŽĆ÷ĻŌĻÖĻó”£ŹµŃ鏱æɹ©Ń”ŌńµÄŹŌ¼ĮÓŠ£ŗ¢ŁĪ“ÖŖÅØ¶ČµÄNaOHČÜŅŗ£»¢Ś37%ŃĪĖį£»¢Ū40%ĮņĖį£»¢Ü14%ŃĪĖį£»¢Ż“óĄķŹÆ£»¢ŽK2CO3¹ĢĢ壻¢ßCu2(OH)2CO3·ŪÄ©”£
ŹµŃéŹŅĻÖÓŠČēĻĀŅĒĘ÷£ŗĢś¼ÜĢØ”¢ĘōĘÕ·¢ÉśĘ÷”¢ĮæĶ²”¢ÉÕ±”¢Čé½ŗ¹Ü”¢²£Į§µ¼¹Ü”¢·ÖŅŗĀ©¶·”£ĻĀ±ķĖłĮŠĪŖÓŠ¹ŲĪļÖŹŌŚ³£ĪĀŹ±µÄČܽā¶Č(g/100gĖ®)£ŗ
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15.9 |
8.40 |
35.8 |
35.5 |
20.0 |
40.0 |
(1)±¾ŹµŃéӦєÓƵÄŅĒĘ÷£¬³żĘōĘÕ·¢ÉśĘ÷”¢Čé½ŗ¹Ü”¢²£Į§µ¼¹ÜĶā£¬»¹Ó¦ÓŠ”””””””” ”£
”” (2)ĪŖ±£Ö¤ÖʵƵÄNa2CO3ČÜŅŗ¾”Įæ“æ£¬Ó¦Ń”ÓƵÄŅ©Ę·³ż¢ŁĶā£¬»¹Ó¦ŠčŅŖ”””””””””” ”£
”” (3)¼ņŅŖŠšŹöŹµŃé²½Öč£¬Ö±µ½ÖʵƓæNa2CO3ČÜŅŗ(ŅĒĘ÷°²×°²»±ŲŠšŹö)”£
”””””””” ¢ŁĮæČ”Į½·ŻĻąĶ¬Ģå»żµÄNaOHČÜŅŗ£»¢Ś”””””””””””””””””””””””””””””””””””” £»
¢Ū”””””””””””””””””””””””””””””””””””” ”£
”” (4)øł¾Żøų³öµÄČܽā¶ČŹż¾Ż£¬Čō±£Ö¤ŌŚÅäÖĘ¹ż³ĢÖŠ²»Īö³ö¾§Ģ壬ĖłÓĆNaOHČÜŅŗÖŠŗ¬NaOHµÄÖŹĮæ·ÖŹżµÄ×ī“óÖµŹĒ¶ąÉŁ(Š“³ö¼ĘĖć²½ÖčŗĶ±ŲŅŖµÄĪÄ×ÖĖµĆ÷)£æ
”””””””” a””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”””””””” b””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”””””””” c””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”””” ÄćµÄa½į¹ūĖµĆ÷ĮĖ””””””””””””””””””””””””””””””””””””””””””””””””””””””
26£®(18·Ö)×é³Éµ°°×ÖŹµÄ°±»łĖįŌ¼ÓŠ20ÖÖ”£°±»łĖį¼ČÄÜÓėĖį·“Ó¦ÓÖÄÜÓė¼ī·“Ó¦£¬Ņņ“Ė°±»łĖįµÄ»ÆѧŠŌÖŹ±ķĻÖĪŖ”””””””””””””””””””” ”£
”” (1)Č”ĻĀŹöČżÖÖ°±»łĖį»ģŗĶĪļ¹²0.28mol£¬æÉÓė156mL 2.5mol”¤L£1µÄNaOHČÜŅŗ»ņ175mL 2.0mol”¤L£1µÄŃĪĖįĒ”ŗĆ·“Ó¦£¬ŌņŌ»ģŗĻĪļÖŠĢģĆŶ¬°±Ėį”¢Ąµ°±Ėį”¢Ėæ°±ĖįµÄĪļÖŹµÄĮæÖ®±ČĪŖ”””””””””””””””””””” ”£
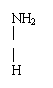
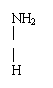 ””
””
HOOC-CH2-C-COOH”””” ””””””””H2N-CH2-CH2-CH2-CH2-C-COOH
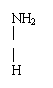 ””””””
ĢģĆŶ¬°±Ėį””””””””””””””””””””””””””””””””””
Ąµ°±Ėį
””””””
ĢģĆŶ¬°±Ėį””””””””””””””””””””””””””””””””””
Ąµ°±Ėį
HO-CH2-C-COOH
”””” Ėæ°±Ėį
”” (2)°±»łĖįŹĒŅŌ”””””””””” µÄ·½Ź½ŠĪ³Éµ°°×ÖŹ£¬°±»łĖįÖ®¼äµÄ»Æѧ¼ü³ĘĪŖ”””””””””” ”£
”” (3)µ°°×ÖŹŌŚĻø°ūÖŹÖŠŹĒÓÉ”””””””””” Ö±½ÓæŲÖĘŗĻ³ÉµÄ”£Čē¹ūŌŚµ°°×ÖŹµÄŗĻ³É¹ż³ĢÖŠ³öĻÖ×ŖĀ¼²ī“ķ£¬¾ĶæÉÄܱķĻÖ³öŅģ³£µÄŠŌד£¬ÓÉÓŚ°±»łĖįµÄ±ä»ÆÓĆĻŌĪ¢¾µŹĒ擲»µ½µÄ£¬Ņņ“Ė³öĻֵIJ”Ö¢ŹōÓŚ”””””””””” Ė®Ę½¼²²””£
 ””
””
(4)øßĪĀĆš¾śŗĶ¾Ę¾«Ćš¾ś¶¼ŹĒĄūÓƵ°°×ÖŹµÄ””””””””””””””
×÷ÓĆ£¬ÕāŅ»×÷ÓĆµÄ½į¹ūŹĒĘä””””””””””””””””””
½į¹¹±»ĘĘ»µ”£
””
””
(4)øßĪĀĆš¾śŗĶ¾Ę¾«Ćš¾ś¶¼ŹĒĄūÓƵ°°×ÖŹµÄ””””””””””””””
×÷ÓĆ£¬ÕāŅ»×÷ÓĆµÄ½į¹ūŹĒĘä””””””””””””””””””
½į¹¹±»ĘĘ»µ”£
 ””
””
””
””
 ””
””
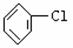 ””
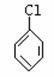
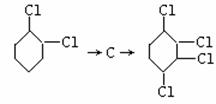
27£®(24·Ö)(1)ĻÖĶعżŅŌĻĀ²½ÖčÓÉ””””””””””
ÖĘČ”””””””””””””
£ŗ ”””””””””śA”śB
””
27£®(24·Ö)(1)ĻÖĶعżŅŌĻĀ²½ÖčÓÉ””””””””””
ÖĘČ”””””””””””””
£ŗ ”””””””””śA”śB
”ś
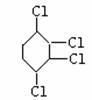
¢Ł“Ó×óµ½ÓŅŅĄ“ĪĢīŠ“Ćæ²½ĖłŹōµÄ·“Ó¦ĄąŠĶŹĒ(a£®Č”“ś·“Ó¦£¬b£®¼Ó³É·“Ó¦£¬c£®ĻūČ„·“Ó¦£¬Ö»Ģī×ÖÄø)”””””””””””””””” ”£
 ””
¢ŚŠ“³öA”śB·“Ó¦ĖłŠčµÄŹŌ¼ĮŗĶĢõ¼žŹĒ””””””””””””””””
ӣ
””
¢ŚŠ“³öA”śB·“Ó¦ĖłŠčµÄŹŌ¼ĮŗĶĢõ¼žŹĒ””””””””””””””””
ӣ
¢ŪŠ“³ö”””””””””””””””””””””””””” µÄ»Æѧ·“Ó¦·½³ĢŹ½”£
”” (2)ĻąĶ¬ĪļÖŹµÄĮæÅØ¶ČµÄĻĀĮŠĪåÖÖČÜŅŗ£ŗ¢Ł(NH4)2CO3£¬¢ŚNa2CO3£¬¢ŪNH4HCO3£¬
¢ÜNaHCO3£¬¢ŻH2CO3£¬°“c(CO32£)ÓÉŠ”µ½“óµÄĖ³ŠņÅÅĮŠµÄŹĒ(ĢīŠņŗÅ)”” ”””””””””””£
”” (3)ŌŚ101KPaŹ±£¬1.00gĮņ·ŪŌŚŃõĘųÖŠĶźČ«Č¼ÉÕ£¬·Å³ö9.25KJµÄČČĮ棬SµÄČ¼ÉÕČČĪŖ”””””””””””” £¬±ķŹ¾SČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ”””””””””””””””””””””””””” ”£
36.(9·Ö)ÉśĆüŹĒŅ»ÖÖ×īĪŖĘęĆī×īø»÷ČĮ¦µÄ×ŌČ»ĻÖĻó.¹ŲÓŚÉśĆüµÄĘšŌ“£¬ĄśŹ·ÉĻŌų¾ÓŠ¹żÖÖÖÖ¼ŁĖµ£¬ÓŠŅ»ÖÖ”°ÓīÖęÅßÖÖĖµ”±ČĻĪŖ£¬Ōģ³É»Æѧ·“Ó¦²¢µ¼ÖĀÉśĆü²śÉśµÄÓŠ»śĪļ£¬ŹĒÓėµŲĒņÅöײµÄåēŠĒ“ųĄ“µÄ.¾”¹ÜÖīČē“ĖĄąµÄ¹ŪµćČŌŹĒŅ»Š©ŠčŅŖ½ųŅ»²½Ö¤Ć÷µÄĪŹĢā£¬µ«Ķعż¶ŌŌÉŹÆ”¢åēŠĒ”¢ŠĒ¼ŹĪļÖŹŅŌ¼°ĘäĖūŠŠŠĒÉĻµÄÓŠ»ś·Ö×ÓµÄĢ½Ė÷ÓėŃŠ¾æ£¬ĮĖ½āÕāŠ©ÓŠ»ś·Ö×ÓŠĪ³ÉÓė·¢Õ¹µÄ¹ęĀÉ£¬¶¼½«ĪŖµŲĒņÉĻÉśĆüĘšŌ“µÄŃŠ¾æĢį¹©øü¶ąµÄ׏ĮĻ.
(1)×ŌČ»½ēÖŠ£¬ÉśĪļÓė·ĒÉśĪļ“ęŌŚÖī¶ąĒų±š£ŗ×÷ĪŖÉśĪļ£¬±ŲŠė¾ß±øµÄ×ī»ł±¾ĢŲÕ÷ŹĒ
(2)µ°°×ÖŹŹĒÉśĆüµÄ»ł“”ĪļÖŹ£¬ĻĀĮŠ¹ŲÓŚµ°°×ÖŹµÄĖµ·ØÕżČ·µÄŹĒ
A.µ°°×ÖŹµÄÖÖĄąŗܶą£¬ĖüĆĒ¶¼ÄÜČܽāÓŚĖ®
B.µ°°×ÖŹĖ®½āµÄ×īÖÕ²śĪļŹĒ°±»łĖį
C.µ°°×ÖŹČÜŅŗÖŠ¼ÓČėÅØŃĪĖį£¬ŃÕÉ«±ä»Ę
D.µ°°×ÖŹČÜŅŗÖŠ¼ÓČė±„ŗĶĮņĖįļ§ČÜŅŗ£¬µ°°×ÖŹ½«±äŠŌ
”””” (3)ĪŖĮĖĢ½²āijŠŠŠĒ±ķĆęÓŠĪŽÉśĆüĻÖĻó£¬ĻņøĆŠŠŠĒ·¢ÉäŅ»æÅĢ½²āĪĄŠĒ£¬ĪĄŠĒČĘŠŠŠĒ×öŌČĖŁŌ²ÖÜŌĖ¶ÆµÄ°ė¾¶ĪŖR£¬ĪĄŠĒÖŹĮæĪŖm£¬øĆŠŠŠĒÖŹĮæĪŖM£¬ŅżĮ¦³£ĮæĪŖG.ŌņĪĄŠĒĖłŹÜĻņŠÄĮ¦FĻņ__________£»ĪĄŠĒČĘŠŠŠĒ×öŌ²ÖÜŌĖ¶ÆµÄĻßĖŁ¶Čv=__________
35.(9·Ö)ČēĶ¼ĖłŹ¾ĪŖ³µÕ¾Ź¹ÓƵÄĖ®Ę½“«ĖĶ“ų×°ÖƵď¾ŅāĶ¼.±Į½ōµÄ“«ĖĶ“ųŹ¼ÖÕ±£³Ö3.Om£ÆsµÄŗć¶ØĖŁĀŹŌĖŠŠ£¬“«ĖĶ“ųµÄĖ®Ę½²æ·ÖAB¾ąĖ®Ę½µŲĆęµÄø߶ČĪŖA=0.45m.ĻÖÓŠŅ»ŠŠĄī°ü(æÉŹÓĪŖÖŹµć)ÓÉA¶Ė±»“«ĖĶµ½B¶Ė£¬ĒŅ“«ĖĶµ½ŌĀ¶ĖŹ±Ć»ÓŠ±»¼°Ź±Č”ĻĀ£¬ŠŠĄī°ü“ÓB¶ĖĖ®Ę½Å׳ö£¬²»¼ĘæÕĘų×čĮ¦£¬gČ”lOm£Æs2
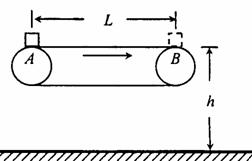
”” (1)ČōŠŠĄī°ü“ÓB¶ĖĖ®Ę½Å׳öµÄ³õĖŁv£½3.Om£Æs£¬ĒóĖüŌŚæÕÖŠŌĖ¶ÆµÄŹ±¼äŗĶ·É³öµÄĖ®Ę½¾ąĄė£»
”””” (2)ČōŠŠĄī°üŅŌv”££½1.Om£ÆsµÄ³õĖŁ“ÓA¶ĖĻņÓŅ»¬ŠŠ£¬ŠŠĄī°üÓė“«ĖĶ“ų¼äµÄ¶ÆĦ²ĮŅņŹż¦Ģ£½0.20£¬ŅŖŹ¹Ėü“ÓB¶Ė·É³öµÄĖ®Ę½¾ąĄėµČÓŚ(1)ÖŠĖłĒóµÄĖ®Ę½¾ąĄė£¬Ēó“«ĖĶ“ųµÄ³¤¶ČLÓ¦Āś×ćµÄĢõ¼ž.
34.(7·Ö)ČēĶ¼ĖłŹ¾£¬Ė®Ę½ĆęÉĻÓŠĮ½øłĻą¾ą0.5mµÄ×ć¹»³¤µÄĘ½ŠŠ½šŹōµ¼¹ģMNŗĶPQ£¬ĖüĆĒµÄµē×čæÉŗöĀŌ²»¼Ę£¬ŌŚMŗĶ PÖ®¼ä½ÓÓŠ×čÖµĪŖRµÄ¶ØÖµµē×č£¬µ¼Ģå°ōab³¤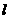 £½0.5m£¬Ęäµē×čĪŖr£¬Óėµ¼¹ģ½Ó“„Į¼ŗĆ.Õūøö×°ÖĆ“¦ÓŚ·½ĻņŹśÖ±ĻņÉĻµÄŌČĒæ“ų”ÖŠ£¬“ÅøŠÓ¦Ēæ¶ČB£½0.4T.ĻÖŹ¹abŅŌ
£½0.5m£¬Ęäµē×čĪŖr£¬Óėµ¼¹ģ½Ó“„Į¼ŗĆ.Õūøö×°ÖĆ“¦ÓŚ·½ĻņŹśÖ±ĻņÉĻµÄŌČĒæ“ų”ÖŠ£¬“ÅøŠÓ¦Ēæ¶ČB£½0.4T.ĻÖŹ¹abŅŌ £½10m£ÆsµÄĖŁ¶ČĻņÓŅ×öŌČĖŁŌĖ¶Æ.
£½10m£ÆsµÄĖŁ¶ČĻņÓŅ×öŌČĖŁŌĖ¶Æ.
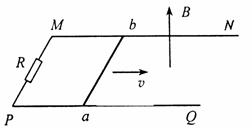
(1)abÖŠµÄøŠÓ¦µē¶ÆŹĘ¶ą“ó?
(2)abÖŠµēĮ÷µÄ·½ĻņČēŗĪ?
(3)Čō¶ØÖµµē×čR£½3£¬O¦ø,µ¼Ģå°ōµÄµē×čr£½1.O¦ø,£¬ŌņµēĀ·ÖŠµÄµēĮ÷¶ą“ó?
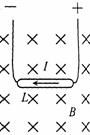
33.(4·Ö)°Ń³¤L£½0.15mµÄµ¼Ģå°ōÖĆÓŚ“ÅøŠÓ¦Ēæ¶ČB=1.0”Į10-2TµÄŌČĒæ“ų”ÖŠ£¬Ź¹µ¼Ģå°ōŗĶ“ų”·½Ļņ“¹Ö±£¬ČēĶ¼ĖłŹ¾
Čōµ¼Ģå°ōÖŠµÄµēĮ÷I£½2.0A£¬·½ĻņĻņ×ó£¬Ōņµ¼Ģå°ōŹÜµ½µÄ°²ÅąĮ¦“óŠ”F=__________N£¬°²ÅąĮ¦µÄ·½ĻņĪŖŹśÖ±Ļņ__________£¬(Ń”Ģī”°ÉĻ”±»ņ”°ĻĀ”±)
32.(4·Ö)Ņ»øöµ„°Ś×ö¼ņŠ³ŌĖ¶Æ£¬ĘäÕń¶ÆĶ¼ĻóČēĶ¼ĖłŹ¾£¬
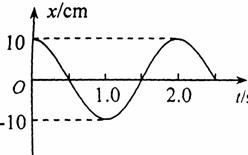
 øƵ„°ŚµÄÖÜĘŚT£½__________s£»ŌŚ2.0sÄ©£¬°ŚĒņ¶ŌÓŚĘ½ŗāĪ»ÖƵÄĪ»ŅĘx£½__________cm.””
øƵ„°ŚµÄÖÜĘŚT£½__________s£»ŌŚ2.0sÄ©£¬°ŚĒņ¶ŌÓŚĘ½ŗāĪ»ÖƵÄĪ»ŅĘx£½__________cm.””
30.(9·Ö)ĻĀĶ¼ĖłÉę¼°µÄĪļÖŹ¾łĪŖ֊ѧ»Æѧ֊µÄ³£¼ūĪļÖŹ£¬ĘäÖŠCĪŖ02”¢DĪŖC12”¢EĪŖFeµ„ÖŹ£¬ĘäÓąĪŖ»ÆŗĻĪļ£¬ĖüĆĒ“ęŌŚČēĻĀ×Ŗ»Æ¹ŲĻµ£¬·“Ó¦ÖŠÉś³ÉµÄĖ®¼°“ĪŅŖ²śĪļ¾łŅŃĀŌČ„£¬
 ””
””
(1)Š“³öÓŠ¹ŲĪļÖŹµÄĆū³Ę»ņ»ÆѧŹ½£ŗ
B ____________________ £¬F____________________£¬ H____________________””””
”” (2)Öø³öMn02ŌŚĻą¹Ų·“Ó¦ÖŠµÄ×÷ÓĆ£ŗ·“Ó¦¢ŁÖŠŹĒ__________¼Į£¬·“Ó¦¢ŚÖŠŹĒ__________¼Į
(3)Čō·“Ó¦¢ŁŹĒŌŚ¼ÓČČĢõ¼žĻĀ½ųŠŠ£¬ŌņAŹĒ__________£»Čō·“Ó¦¢ŁŹĒŌŚ³£ĪĀĢõ¼žĻĀ½ųŠŠ£¬ŌņAŹĒ__________
(4)Š“³öBÓėMn02¹²ČČ»ńµĆDµÄ»Æѧ·½³ĢŹ½£ŗ ______________________________
3l.(5·Ö)ÓŠ»śĪļAÓÉĢ¼”¢Ēā”¢ŃõČżÖÖŌŖĖŲ×é³É£¬ĻÖČ”3gAÓė 4.48LŃõĘų(±ź×¼×“æö)ŌŚĆܱÕČŻĘ÷ÖŠČ¼ÉÕ£¬Č¼ÉÕŗóÉś³É¶žŃõ»ÆĢ¼”¢Ņ»Ńõ»ÆĢ¼ŗĶĖ®ÕōĘų(¼ŁÉč·“Ó¦ĪļƻӊŹ£Óą)£¬½«·“Ӧɜ³ÉµÄĘųĢåŅĄ“ĪĶعżÅØĮņĖįŗĶ¼īŹÆ»Ņ£¬ÅØĮņĖįŌöÖŲ3.6g£¬¼īŹÆ»ŅŌöÖŲ4.4g£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
”””” (1)3gAÖŠĖłŗ¬ĒāŌ×Ó”¢Ģ¼Ō×ÓµÄĪļÖŹµÄĮæø÷ŹĒ¶ąÉŁ?
(2)Ķعż¼ĘĖćČ·¶ØøĆÓŠ»śĪļµÄ·Ö×ÓŹ½.
29.(8·Ö)ijĶ¬Ń§ÄāÓĆĀČ»ÆøĘ¹ĢĢ唢Ģ¼ĖįÄĘČÜŅŗŗĶĻ”ĻõĖįµČŹŌ¼Į£¬ĻČÖʵĆĢ¼ĖįøĘ£¬×īÖÕÖĘµĆ“æ¾»µÄĻõĖįøĘ¾§Ģ唣
(1)Š“³öÖĘČ”¹ż³ĢÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½:
__________________________ ______________________________
(2)Ēė°ļÖśøĆĶ¬Ń§Ķź³ÉĻĀĮŠŹµŃé²Ł×÷²½Öč(²»ŅŖĒó»Ų“šŹ¹ÓƵÄŅĒĘ÷)
¢ŁÓĆÕōĮóĖ®ĶźČ«ČܽāCaCl2ŗ󣬼Ó____________________
¢Ś½«·“Ó¦ŗóµÄ»ģŗĻĪļ¹żĀĖ£¬²¢ÓĆŹŹĮæÕōĮóĖ®Ļ“µÓ³ĮµķÖĮĪŽCl-.
¢Ū¼ÓČė____________________£¬Ź¹³ĮµķĶźČ«Čܽā”£
¢Ü ____________________£¬µĆµ½“æ¾»µÄĻõĖįøĘ¾§Ģå.
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com