
题目列表(包括答案和解析)
1.下列表示运用气体测压技术进行气体测定,前者是密闭装置中放入的生物材料,中间是试剂,后者是数值变化的意义。不正确的是
A.浸泡的花生种子一KOH溶液一O2消耗量
B.煮死的大豆种子一蒸馏水一CO2释放量与O2消耗量的差值
C.新鲜的小麦叶片一CO2缓冲液一净光合作用O2释放量
D.新鲜的玉米叶片一NaOH溶液一光下呼吸消耗的O2量
31.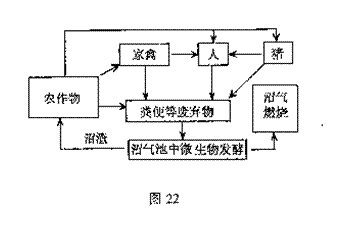 (18分)图22是某生态农业的结构模式图,请据图分析回答:
(18分)图22是某生态农业的结构模式图,请据图分析回答:
(1)该生态系统的主要成分是图中的 ,它是生态系统的基石。
(2)从生态系统的组成成分看,图中未标出的是 。
(3)生态系统的主要功能是 和 ,从生态学角度分析,人们建立图示的农业生态系统的主要目的是 (从下列选项中选择,填字母代号)
A.实现物质和能量的多级利用
B.减少环境污染
C.提高农产品的产量
D.延长食物链,使系统总能量利用效率降低
(4)一般地说,农田生态系统的 稳定性较低,若此生态系统遭到酸雨危害,首先受到影响的是 ,从而影响生态系统的稳定性。
(5)该图中的食物链
条。如果一个人的食物有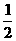 来自农作物,
来自农作物,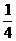 来自家禽,
来自家禽,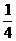 来自猪肉,假如能量传递效率为10%,那么此人每增加1千克体重,约消耗蔬菜
千克。
来自猪肉,假如能量传递效率为10%,那么此人每增加1千克体重,约消耗蔬菜
千克。
30.(18分)纳豆是以蒸煮的大豆经纳豆芽孢杆菌发酵制得的食品,营养非常丰富。纳豆芽孢杆菌能产生一种丝氨酸蛋白酶,又称为纳豆激酶,具有一定的溶纤作用,可用于血栓性疾病的预防和治疗,有广阔的发展前景。
(1)纳豆芽孢杆菌是细菌的一种,它主要以 的方式进行繁殖,大量培养时培养基中含有的营养物质包括 。
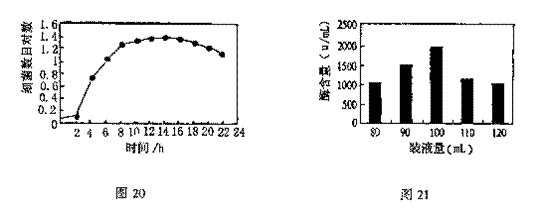
(2)图20是纳豆孢杆菌在人工培养条件下测得的生长曲线,由图可知,0-2h为
期,2-10h为 期。图21是在500mL的三角瓶中分别装入不同量的培养基,接种相同数量的菌种后测定的纳豆激酶的含量,由图可以看出,最佳的装液量为 ,装液量如果太多,培养基中的
减少,从而使纳豆激酶的产量降低,由此推测,纳豆芽孢杆菌的异化作用类型是 。
(3)血栓的主要成分之一是纤维蛋白,在纳豆激酶的作用下,可将纤维蛋白水解成短肽和氨基酸,从而达到溶解血栓的作用。水解生成的氨基酸,在人体内除了能用来合成各种组织蛋白,还可以合成一些具有一定生理功能的特殊蛋白质,如:
等激素,或者通过脱氨基作用,含氮部分转变成 而排出体外。
29.(12分)将休眠状态的糖槭种子与湿砂分层堆积的低温(0-5℃)的地方1-2个月,可解除种子的休眠状态从而开始萌发,这种催芽技术称为层积处理。图19示在层积处理过程中,糖槭种子内的各种激素含量随着处理时间的变化情况,请据图回答:
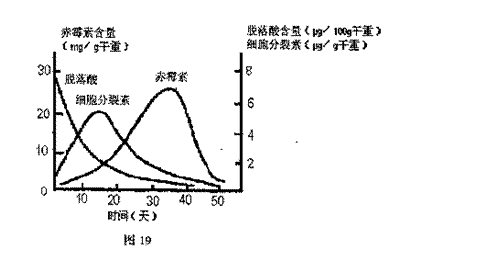
(1)对种子萌发起抑制作用的激素是 ,起促进作用的激素是 和 。由此可知,脱落酸与赤霉素这两种激素在种子破除休眠的过程中表面为 作用。
(2)在层积处理过程中,各种激素变化的根本原因是在不同时间和空间条件下细胞内的 的结果。
(3)在层积处理过程中,各种激素含量的变化说明了植物的生命活动不只受单一激素的调节,而是多种激素 的结果。
28.(16分)
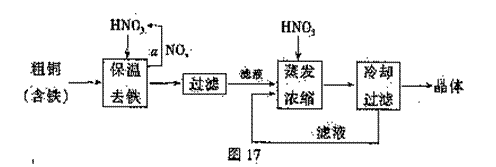 (1)工业上以粗铜为原料采取如图17所示流程制备硝酸铜晶体。
(1)工业上以粗铜为原料采取如图17所示流程制备硝酸铜晶体。
①步骤a中,还需要通入氧气和水,其目的是 。
②根据下表数据,在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
|
|
氢氧化开始沉淀时pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Cu2+ |
1.9 4.7 |
3.2 6.7 |
不用加水的方法调节溶液pH的主要原因是 。
 ③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其原因是(结合离子方程式说明)
。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其原因是(结合离子方程式说明)
。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时
阴极反应式是 。
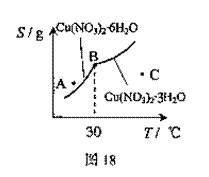
(3)图18是某小组同学查阅资料所绘出的硝酸
铜晶体[Cu(NO3)2·nH2O]的溶解度曲线
(温度在30℃前后对应不同的晶体),下
列说法正确的是 (填字母)。
a.A点时溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程终得到晶体是Cu(NO3)2·3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
(4)某些共价化合物(如H2O、NH3、N2O4等)在液态时有微弱的导电性,主要是因为发生了电离,如:2NH3 NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是
;Cu与液态N2O4反应制得无水硝酸的化学方程式是
。
NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是
;Cu与液态N2O4反应制得无水硝酸的化学方程式是
。
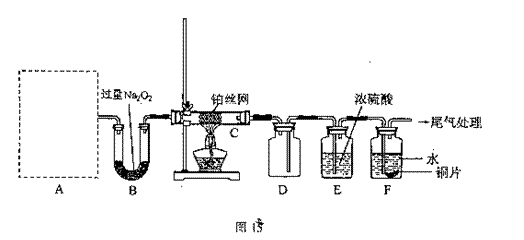
27.(14分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如图15所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:
 a.NH4HCO3 b.NH4C1 c.Ca(OH)2 d.NaOH
a.NH4HCO3 b.NH4C1 c.Ca(OH)2 d.NaOH
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验精通制取A中气体时若只用一种试剂,该试剂是 (填代表备选试剂的字母);此时A中主要的玻璃仪器有 (填名称)。
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B装置中发生反应的化学方程式: 。
(3)对于C中发生的可逆反应,下列说法正确的是 。
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
d.使用铂丝网可以使正反应速率增大,同时也增大逆反应速率
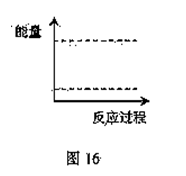 (4)请在图16坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式。
(4)请在图16坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式。
(5)待实验结束后,将B中固定混合物溶于
500mL 1 mol·L-1的盐酸中,产生无色
混合气体甲,溶液呈中性,则实验前B
中原有Na2O2的物质的量 mol。
甲在标准状况下是 L
(忽略气体溶解)。
26.(16分)中学常见反应的化学方程式是:A+B→X+Y+H2O(未配平,反应条件略去),其中,A、B的物质的量之比为1:4。请回答:
(1)若Y是黄绿色气体,则Y的电子式是 ,该反应的化学方程式是 。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在周期表中的位置是 (填所在周期和族);Y的化学式是 。
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是 mol。
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中离子浓度从大到小的顺序是 。
25.(14分)若芳香族化合物A的结构简式是 (其中R为饱和烃基),
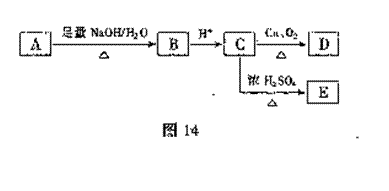 A在一定条件下有如图14所示的转化关系。已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2。
A在一定条件下有如图14所示的转化关系。已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2。
(1)E的分子式是 。
(2)关于上述各步转化中,下列说法正确的是 。
a.以上各步没有涉及加成反应
b.E比C的相对分子质量小18
c.A、B、C、D中都含有-COOH
d.A与C发生酯化反应后得到的有机物分子式可能是C18H18O4C1
(3)写出所有符合下列要求的E的同分异构体的结构简式: 、
(①分子中苯环上有三个取代基,且苯环上的一氯代物有两种
②1mol该有机物与足量银氨溶液反应能产生4molAg)。
(4)针对以下不同情况分析回答:
①若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F;D能发生银镜反应。则D的结构简式是 。欲由A通过一步反应得到F,该反应的化学方程式是 。
②若E中除苯环外,还含有一个六元环,则C→E的化学方程式是 。
24.(20分)如图13甲所示,一边长L=2.5m、质量m=0.5kg的正方形金属线框,放在光滑绝缘的水平面上,整个装置放在方向竖直向上、磁感应强度B=0.8T的匀强磁场中,它的一边与磁场的边界MN重合。在水平力F作用下由静止开始向左运动,经过5s线框被拉出磁场。测得金属线框中的电流随时间变化的图像如乙图所示,在金属线框被拉出的过程中。
(1)求通过线框导线截面的电量及线框的电阻;
(2)写出水平力F随时间变化的表达式;
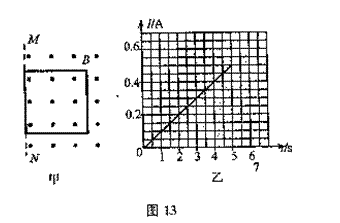 (3)已知在这5s内力F做功1.92J,那么在此过程中,线框产生的焦耳热是多少?
(3)已知在这5s内力F做功1.92J,那么在此过程中,线框产生的焦耳热是多少?
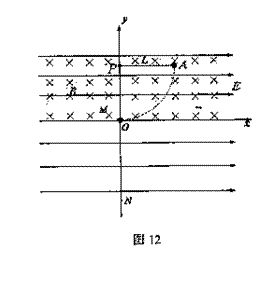
23.(18分)如图12所示,竖直平面xOy内存在水平向右的匀强电场,场强大小E=10N/c,在y≥0的区域内还存在垂直于坐标平面向里的匀强磁场,磁感应强度大小B=0.5T。一带电量q=+0.2C、质量m=0.4kg的小球由长L=0.4m的细线悬挂于P点小球可视为质点,现将小球拉至水平位置A无初速度释放,小球运动到悬点P正下方的坐标原点O时,悬线突然断裂,此后小球又恰好能通过O点正下方的N点。(g=10m/s2),求:
 (1)小球运动到O点时的速度大小;
(1)小球运动到O点时的速度大小;
(2)悬线断裂前瞬间拉力的大小;
(3)ON间的距离。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com