
题目列表(包括答案和解析)
5.下列实验的目的、材料的选择和所用试剂正确的一组是 ( )
A.利用甘蔗组织样液进行还原性糖的鉴定,加入斐林试剂并加热会出现砖红色沉淀
B.用高倍显微镜观察人口腔上皮细胞中的线粒体时,在洁净的载玻片中央滴一滴用0.5g健那绿和50mL蒸馏水配制的染液
C.观察渗透现象时,在长颈漏斗口外封上一层玻璃纸,往漏斗内注入蔗糖溶液,然后将漏斗浸入盛有清水的烧杯中
D.探究温度对酶少性的影响,向3%过氧化氢溶液中加入过氧化氢酶溶液
4.在农业生产中,人们常利用生物学原理来培育新品种以提高作物产量。下列有关叙述错误的是 ( )
A.使用一定浓度的生长素类似物处理未授粉的番茄雌蕊柱头而获得无籽番茄,该无籽番茄的变异状属于不可遗传变异
B.将不能稳定遗传的高杆抗病小麦杂交得到稳定遗传的矮秆抗病小麦,其原理是基因重组
C.诱变育种可发提高突变率,在较短时间内获得更多的变异类型
D.将二倍体番茄的花药离体培养并经秋水仙素处理,得到的番茄植株每对同源染色体上成对的基因都是纯合的,自交产生的后代不发生性状分离
3.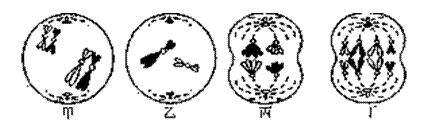 在哺乳动物的某一器官中,发现了如下细胞分裂图像,下列有关叙述错误的是 ( )
在哺乳动物的某一器官中,发现了如下细胞分裂图像,下列有关叙述错误的是 ( )
A.甲图处于减数分裂第一次分裂过程中,含有两个染色体组
B.在乙图所示的细胞中,含有1对同源染色体,4个姐妹染色单体
C.丙细胞产生的基因突变通常能遗传到子代个体中
D.该器官一定是动物的睾丸
2.运用“人工膜技术”制作的携有单克隆抗体的磷脂微球体药
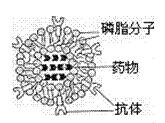 物如图所示。当药物被注射到实验鼠血液中一段时间后,首
物如图所示。当药物被注射到实验鼠血液中一段时间后,首
先在某种癌细胞内检测到药物已进入。据此认为,药物进入
细胞的方式最可能是 ( )
A.药物分子透过微球体与细胞膜的自由扩散
B.抗体与细胞识别后诱发膜融合或细胞内吞
C.药物分子通过识别细胞膜载体的主动运输
D.抗体与细胞识别后诱发微球体的主动侵染
1.“三鹿奶粉事件”是不法分子在奶粉中添加了三聚氰胺。三聚氰胺的分子式为C3N6H6,含氮量约66%,用凯氏定氨法测定饲料或食品中蛋白质含量时,根本区分不出真伪蛋白质。长期食用含三聚氰胺的奶粉会损害泌尿系统,形成膀胱肾部结石。下列相关说法正确的是 ( )
A.蛋白质所含的氮元素主要存在于R基中
B.三聚氰胺与氨基酸组成元素相同,食品中添加三聚氰胺,可提高含氮率,使劣质食品通过质检机构的检测。
C.用双缩脲试剂鉴定牛奶和三聚氰胺,后者不会生成紫色复合物
D.三聚氰胺在细胞内脱去氨基酸后可氧化分解最终生成CO2和H2O
1.请考生务必将自己所选做题目的答案写在专用的答题纸上;
30.(14分)某课外小组利用H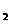 还原黄色的
还原黄色的 粉末测定W的相对原子质量,下图是测
粉末测定W的相对原子质量,下图是测
定装置的示意图,A中的试剂是盐酸。
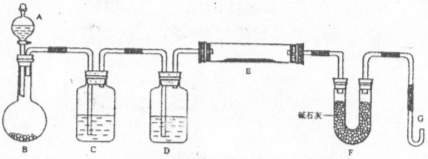
请同答F列问题。
(1)仪器中装入的试剂:B________、C________、D________:
(2)连接好装置后应首先________________________,其方法是________________
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是
________________。在这两步之间还应进行的操作是________________________ .
(4)反应过程中G管逸出的气体是________________,其处理方法是________________
(5)从实验中测得了下列数据
①空E管的质量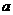 ;②E管和
;②E管和 的总质量
的总质量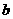 :③反应后E管和W粉的总质量c(冷却到室温称量);④反应前F管及内盛物的总质量d;⑤反应后F管及内盛物的总质量e由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其匏涉及的元素的相对原子质量均为已知):
:③反应后E管和W粉的总质量c(冷却到室温称量);④反应前F管及内盛物的总质量d;⑤反应后F管及内盛物的总质量e由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其匏涉及的元素的相对原子质量均为已知):
计算式1:A (W)= ________:计算式2:A
(W)= ________:计算式2:A (W):________。
(W):________。
选做题部分
(包括9小题,每小题8分。考生从中选2个物理、1个化学、1个生物题目作答,满
分32分,多选多做不计入成绩)
提示:
1.x是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
(1)若X为氧化物.X的化学式为_____________。
(2)若X为单质,X用于焊接钢轨时,发生反应的化学方程式为_____________。
(3)若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气
体B。等物质的量的A和B在水溶液中反应又生成X。
常温下X与足量稀氢氧化钠溶液反应的离子方程式为_____________。
II.铜既能与稀硝酸反应.也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为: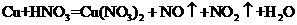 (未配平)
(未配平)
(1)硝酸在该反应中的作用是_____,该反应的还原产物是_____。
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是_____,如果得到的N0和
NO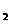 物质的量相同,则参加反应的硝酸的物质的量是_____,若用捧水法收集
物质的量相同,则参加反应的硝酸的物质的量是_____,若用捧水法收集
这些气体,可得标准状况下的气体体积_____。
(3)如果参加反应的Cu平 的物质的量之比是5:14,写出并配平该反应的离子
的物质的量之比是5:14,写出并配平该反应的离子
方程式________________________________________。
29.(14分)
28.(14分)
(1)已知::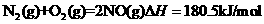
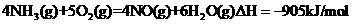
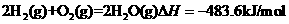
则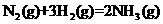 的
的 =__________________________。
=__________________________。
(2)工业合成氮的反应为 。在一定温度下,将一定量的N
。在一定温度下,将一定量的N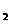 和H
和H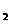 通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是___________________。
通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是___________________。
①增大压强 ②增大反应物的浓度
③使用催化荆 ④降低温度
(3) 工业合成氨的反应为 。设在容积为2.0L的密闭容器中充入
。设在容积为2.0L的密闭容器中充入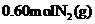 和
和 .反应在一定条件下达到平衡时,NH
.反应在一定条件下达到平衡时,NH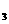 的物质的量分数(NH
的物质的量分数(NH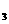 的物质的量与反应体系中总的物质的量之比)为
的物质的量与反应体系中总的物质的量之比)为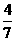 。计算
。计算
①该条件下N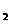 的平衡转化率为______________;
的平衡转化率为______________;
②该条下反应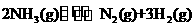 的平衡常数为_____________。
的平衡常数为_____________。
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行右图所示实验:(其中c、d均为碳棒。NaCI溶液的体积为500m1)
①a极为________极,电极反应式__________________________;
c极为________极,电极反应式__________________________
②右图装置中,当b极上消耗的O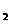 在标准状况下的体积为280ml时,则NaCl溶液
在标准状况下的体积为280ml时,则NaCl溶液
的PH为_________ (假设反应前后溶液体积不变,且NaCl溶液足量)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com