
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
2”¢ĻĀĮŠ¹ŲÓŚĻõ»ÆĻø¾śµÄĖµ·ØÕżČ·µÄŹĒ
A£®ĻßĮ£ĢåŹĒĻõ»ÆĻø¾ś½ųŠŠÓŠŃõŗōĪüµÄÖ÷ŅŖ³”Ėł
B£®Ņ¶ĀĢĢåŹĒĻõ»ÆĻø¾ś½ųŠŠĶ¬»Æ×÷ÓƵÄÖ÷ŅŖ³”Ėł
C£®Ļõ»ÆĻø¾śæÉŅŌ½«°±×Ŗ±äĪŖŃĒĻõĖįŃĪŗĶĻõĖįŃĪ
D£®Ļõ»ÆĻø¾śµÄĻø°ūÖŹÖŠµÄŅÅ“«ĪļÖŹŹĒRNA
1”¢ĻĀĆę¼×”¢ŅŅĮ½Ķ¼·Ö±š±ķŹ¾Ö²ĪļµÄ¹āŗĻĖŁĀŹÓė¹āÕÕĒæ¶Č”¢CO2ŗ¬ĮæµÄ¹ŲĻµ”£¶ŌĮ½Ķ¼¶ųŃŌ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£ŗ
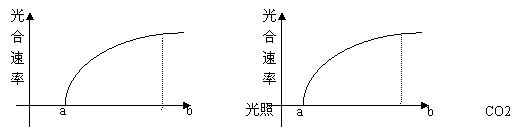
¼×”””””””””””””””””””””””””””””””” ŅŅ
A£®ČōĶĮČĄÖŠN”¢P”¢Mgŗ¬Įæ³ÖŠųĻĀ½µ£¬²»æÉÄܵ¼ÖĀĮ½Ķ¼ÖŠa,bµćøıä
B£®Čō»·¾³ĪĀ¶Č·¢Éś±ä»Æ£¬»įµ¼ÖĀĮ½Ķ¼ÖŠa,bµćĪ»ÖĆøıä
C£®ČōĶ¼ÖŠ±ķŹ¾µÄŹĒŃōÉśÖ²Īļ£¬Ōņ¶ŌŅõÉśÖ²Īļ¶ųŃŌ¼×Ķ¼ÖŠaµćÓ¦ĻņÓŅŅʶÆ
D£®ČōĶ¼ÖŠ±ķŹ¾µÄŹĒC3Ö²Īļ£¬Ōņ¶ŌC4Ö²Īļ¶ųŃŌŅŅĶ¼ÖŠaµćÓ¦ĻņÓŅŅʶÆ
31£®ŌŚĖ®µ¾ÖŠ£¬ÓŠĆ¢(A)¶ŌĪŽĆ¢(a)ĪŖĻŌŠŌ£¬æ¹²”(R)¶Ō²»æ¹²”(r)ĪŖĻŌŠŌ£¬Į½¶ŌŠŌדµÄŅÅ“«·ūŗĻ×ŌÓÉ×éŗĻ¶ØĀÉ”£ÓĆÓŠĆ¢æ¹²”(AARR)ŗĶĪŽĆ¢²»æ¹²”(aarr)µÄĮ½ÖÖĖ®µ¾×÷Ē×±¾£¬ÅąÓżĪŽĆ¢æ¹²”µÄĮ¼ÖÖĖ®µ¾¹©Å©ĆńŹ¹ÓĆ”£
”” (1)ÓĆŌÓ½»ÓżÖÖ·½·ØÅąÓżÕāŅ»Į¼ÖÖ¹©Å©ĆńŹ¹ÓĆÖĮÉŁŠčŅŖ4ÄźŹ±¼ä£¬ĆæŅ»ÄźµÄ·½·ØŗĶÄæµÄŹĒŹ²Ć“£æĒėĶź³ÉĻĀ±ķ£ŗ
|
Ź±¼ä |
·½·Ø |
ÄæµÄ |
|
µŚ1Äź |
”” ¢Ł”” |
»ńµĆF1ÖÖ×Ó |
|
µŚ2Äź |
”” ¢Ś”” |
»ńµĆ”” ¢Ū”” |
|
µŚ3Äź |
×Ō½» |
»ńµĆ”” ¢Ü”” |
|
µŚ4Äź |
×Ō½» |
»ńµĆĪȶØŅÅ“«µÄÖ²Öź |
”” (2)µŚ1Äź×÷ĪŖÄø±¾µÄĖ®µ¾Ó¦øĆŌŚæŖ»ØĒ°×÷”””””””” “¦Ąķ”£
”” (3)µŚ”””””””” ÄźæŖŹ¼³öĻÖĪŽĆ¢æ¹²”ĄąŠĶ£¬ĖüŌ¼Õ¼ČŗĢåµÄ±ČĀŹĪŖ”””””””” £»
”” (4)ČōÓƵ„±¶ĢåÓżÖÖ£¬Ó¦øĆŃ”ŌńµŚ”””””””” ÄźµÄĖ®µ¾Ö²ÖźµÄ»Ø·Ū½ųŠŠ×éÖÆÅąŃų£¬æŖŹ¼³öĻÖæ¹²”ĄąŠĶŌ¼Õ¼ČŗĢåµÄ±ČĀŹĪŖ”””””””””””””””””” ”£
”” (5)¾Ķæ¹²”ŗĶ²»æ¹²”Õā¶ŌĻą¶ŌŠŌד¶ųŃŌ£¬ČĆF1×Ō½»Čż“ś£¬ŌŚ×ŌČ»ĒéæöĻĀ£¬»łŅņʵĀŹµÄ±ä»ÆŹĒ”” ”””””””£
”””””” A£®RŌö“ó”””””””””””””””””””””””””””””””””””””””””” B£®rŌö“ó
”””””” C£®R=r”””””””””””””””””””””””””””””””””””””””””””””” D£®ĪŽ·ØČ·¶Ø
30£®»Ų“šĻĀĮŠÓŠ¹ŲÖ²ĪļÉśĆü»ī¶ÆµÄĪŹĢā£ŗ
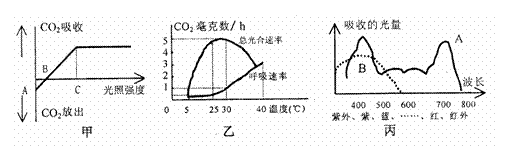 ”””””” I£®Ķ¼¼×”¢ŅŅ”¢±ū·Ö±š±ķŹ¾Ä³Ö²Īļ¹āČ«×÷ÓĆĖŁĀŹÓė¹āÕÕĒæ¶ČÖ®¼äµÄ¹ŲĻµ”¢ĪĀ¶ČÓė¹āŗĻĖŁĀŹÖ®¼äµÄ¹ŲĻµ¼°Ņ¶ĀĢĢåÉ«ĖŲ¶Ō²»Ķ¬²Ø³¤¹āĻßµÄĻą¶ŌĪüŹÕĮæ£ŗ
”””””” I£®Ķ¼¼×”¢ŅŅ”¢±ū·Ö±š±ķŹ¾Ä³Ö²Īļ¹āČ«×÷ÓĆĖŁĀŹÓė¹āÕÕĒæ¶ČÖ®¼äµÄ¹ŲĻµ”¢ĪĀ¶ČÓė¹āŗĻĖŁĀŹÖ®¼äµÄ¹ŲĻµ¼°Ņ¶ĀĢĢåÉ«ĖŲ¶Ō²»Ķ¬²Ø³¤¹āĻßµÄĻą¶ŌĪüŹÕĮæ£ŗ
”” (1)Čō¼×Ķ¼ĖłŹ¾ĒśĻßĪŖŅõÉśÖ²Īļ£¬ŌņŃōÉśÖ²ĪļĒśĻßÓėĻą±Č½ĻCµćĻņ”””””””””””””” ŅĘ”£
”” (2)ÓÉŅŅĶ¼æÉÖŖ£¬40”ꏱ£¬Ö²ĪļĢå”””””””””””””” (ÄÜ/²»ÄÜ)ĻŌŹ¾Éś³¤ĻÖĻ󣬶ų5”ꏱµÄ×ܹāŗĻĖŁĀŹÓėŗōĪüĖŁĀŹµÄ¹ŲĻµæÉÓĆ¼×Ķ¼ÖŠµÄ”””””””””””””” µć±ķŹ¾”£
”” (3)±ūĶ¼ÖŠĒśĻßA”¢B·Ö±š±ķŹ¾Ņ¶ĀĢĢåÖŠµÄĮ½ĄąÉ«ĖŲ£¬ĘäÖŠĒśĻßA±ķŹ¾µÄÉ«ĖŲŹĒ”””””””””””” ”””£
”” (4)ÓĆĖÜĮĻ“óÅļÖÖÖ²Źß²ĖŹ±£¬Ó¦Ń”ŌńµÄ¹āÕÕĒæ¶ČĪŖ¼×Ķ¼ÖŠµÄ”””””””””””””” µć”¢×īŹŹĪĀ¶ČĪŖŅŅĶ¼ÖŠµÄ”””””””””””””” ”ę¼°”””””””””””””” É«µÄĖÜĮĻ“óÅļ”£
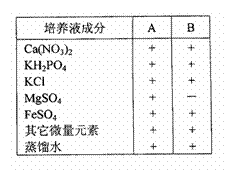 ”””””” II£®Ä³Ķ¬Ń§Č”Éś³¤×“Ģ¬ĻąĶ¬µÄĮ½×é·¬ĒŃÓ×Ćē£¬ÖĆÓŚ±ķÖŠĖłĮŠA”¢BĮ½ÖÖÅąŃųŅŗÖŠ£¬ŌŚĻąĶ¬µÄŹŹŅĖĢõ¼žĻĀÅąŃų£¬¼××éÓĆAÅąŃųŅŗ£¬ŅŅ×éÓĆB
”””””” II£®Ä³Ķ¬Ń§Č”Éś³¤×“Ģ¬ĻąĶ¬µÄĮ½×é·¬ĒŃÓ×Ćē£¬ÖĆÓŚ±ķÖŠĖłĮŠA”¢BĮ½ÖÖÅąŃųŅŗÖŠ£¬ŌŚĻąĶ¬µÄŹŹŅĖĢõ¼žĻĀÅąŃų£¬¼××éÓĆAÅąŃųŅŗ£¬ŅŅ×éÓĆB
ÅąŃųŅŗ”£(±ķÖŠ+±ķŹ¾ÓŠ£¬-±ķŹ¾ĪŽ)
”” (1)øĆĶ¬Ń§ŃŠ¾æµÄæĪĢāŹĒ£ŗ”””””””””””””””””” ”£
”” (2)ŹµŃéÖŠ£¬½«”””””””””””””” ×÷ĪŖ±äĮ棬·Ö³ÉĮĖ
Į½øö×é½ųŠŠŹµŃ飬ĘäÖŠŹµŃé×éŹĒ”””””””” ×锣
”” (3)ŹµŃéÖŠ£¬Ó¦øĆŃ”Ōń”””””””””””””” ×÷ĪŖ¹Ū²ģµÄ
Öø±ź”£
29£®(±¾Ģā¹²15·Ö)
”””””” ·¼Ļć×å»ÆŗĻĪļA”¢A1”¢B”¢B1µÄ»·ÉĻŅ»äå“śĪļ¾łÓŠČżÖÖ£¬ĒŅAÓėA1»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬BÓėB1µÄ»ÆѧŹ½ĻąĶ¬£¬ĘäĻą¹Ų×Ŗ»Æ¹ŲĻµČēĻĀĶ¼£ŗ
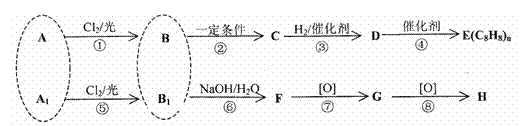
”””””” ŅŃÖŖ£ŗ±½µÄĶ¬ĻµĪļÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀŹĒŌŚ²ąĮ“ÉĻ·¢ÉśČ”“ś·“Ó¦”£
”””” M(C)+2=M(D)£¬M(F)-4=M(G)£¬M(G)+32=M(H)(ĘäÖŠ£¬MĪŖ»ÆŗĻĪļµÄĻą¶Ō·Ö×ÓÖŹĮæ)”£
”””””” ¾ŻÉĻŹö×Ŗ»Æ»Ų“šĻĀĮŠĪŹĢā£ŗ
”” (1)·“Ó¦¢ŚŹōÓŚ”””””””””””””” ·“Ó¦(ÓŠ»ś·“Ó¦ĄąŠĶ)£¬GÖŠµÄŗ¬Įæ¹ŁÄÜĶŵÄĆū³ĘŹĒ”””””””””””””” £»
”” (2)Š“³öAµÄ½į¹¹¼ņŹ½ŹĒ”””””””””””””” £¬Ķź³ÉµŚ¢Ü²½·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ”””””””””””””””””””””””””””” £»
”” (3)FŗĶHŌŚÅØĮņĖį“ęŌŚµÄĢõ¼žĻĀ¼ÓČČ£¬Éś³ÉµÄÓŠ»śĪļ»ÆѧŹ½ĪŖC16H14O5£¬0.2moløĆÓŠ»śĪļÓėNaOHČÜŅŗ³ä·Ö·“Ó¦Ź±ĻūŗÄNaOHµÄĪļÖŹµÄĮæĪŖ”””””””””””””” ””mol£»
”” (4)HµÄijÖÖĶ¬·ÖŅģ¹¹Ģ壬Ęä±½»·ÉĻÓŠČżÖÖ¹ŁÄÜĶÅ”¢ĒŅÄÜ·¢ÉśĖ®½ā·“Ó¦£¬ĒėČĪŅāŠ“³öŅ»ÖÖ·ūŗĻøĆĢõ¼žµÄHµÄĶ¬·ÖŅģ¹¹ĢåŹĒ”””””””””””””””””””””””””””” ”£
28£®(±¾Ģā¹²16·Ö)
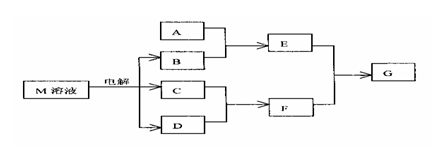 ”””””” ŅŃÖŖMŹĒÓÉX”¢YĮ½ÖÖĪ»ÓŚĶ¬ÖÜĘŚµÄŌŖĖŲ×é³ÉµÄĄė×Ó»ÆŗĻĪļ£¬ĒŅX+ÓėÄŹŌ×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬YŌŖĖŲµÄ×īøßÕż¼ŪÓėĖüµÄøŗ¼Ū“śŹżŗĶĪŖ6”£MÓėĻą¹ŲĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĻĀ(²æ·Ö²śĪļŅŃĀŌČ„)£»
”””””” ŅŃÖŖMŹĒÓÉX”¢YĮ½ÖÖĪ»ÓŚĶ¬ÖÜĘŚµÄŌŖĖŲ×é³ÉµÄĄė×Ó»ÆŗĻĪļ£¬ĒŅX+ÓėÄŹŌ×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬YŌŖĖŲµÄ×īøßÕż¼ŪÓėĖüµÄøŗ¼Ū“śŹżŗĶĪŖ6”£MÓėĻą¹ŲĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĻĀ(²æ·Ö²śĪļŅŃĀŌČ„)£»
”””””” Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
”” (1)YŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆ”””””””””””””” £¬ÓƶčŠŌµē¼«µē½āMČÜŅŗµÄĄė×Ó·“Ó¦·½³ĢŹ½”””””””””””””””””””””””””””””””””””””””””””””””””””””””” £»
”” (2)ČōAŌŖĖŲŹĒÓėXĪ»ÓŚĶ¬Ņ»ÖÜĘŚµÄ½šŹōŌŖĖŲ£¬ŌņAµÄµ„ÖŹÓėBČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””””””””” ””””£»
”” (3)ČōAŹĒŅ»ÖÖ³£¼ūĖįŠŌŃõ»ÆĪļ£¬ĒŅæÉÓĆÓŚÖĘŌģ²£Į§ŗĶ¹āµ¼ĻĖĪ¬£¬ŌņAŹōÓŚ””””””””””””””
¾§Ģ壬EČÜŅŗÓėFµÄĖ®ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ”””””””””””””””””””””””””””” £»
”” (4)ČōAÓėCĪŖĶ¬ÖÖĪļÖŹ£¬Ķł×ćĮæµÄEČÜŅŗÖŠµĪ¼ÓÉŁĮæµÄNa2SČÜŅŗ£¬Õńµ“ŗóĪŽĆ÷ĻŌĻÖĻó£¬ŌŁ¼ÓČėÓĆŃĪĖįĖį»ÆŗóµÄBaCl2ČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬ŌņEÓėNa2SČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ”””””””””””””””””””””””””””” ”£
27£®(±¾Ģā¹²17·Ö)
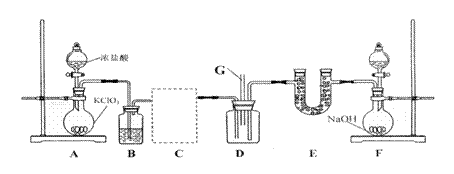 ”””” øÉŌļ“æ¾»µÄĀČĘųÓė°±Ęų·“Ó¦³żµĆµ½µŖĘųĶā£¬»¹ÓŠĮķŅ»ÖÖ²śĪļ”£Ä³ŃŠ¾æŠ”×éŌŚĢ½¾æøĆ²śĪļŹ±Éč¼ĘĮĖČēĻĀŹµŃé£ŗ
”””” øÉŌļ“æ¾»µÄĀČĘųÓė°±Ęų·“Ó¦³żµĆµ½µŖĘųĶā£¬»¹ÓŠĮķŅ»ÖÖ²śĪļ”£Ä³ŃŠ¾æŠ”×éŌŚĢ½¾æøĆ²śĪļŹ±Éč¼ĘĮĖČēĻĀŹµŃé£ŗ
”””””” ŹµŃéÖŠ¹Ū²ģµ½D×°ÖĆÖŠĻČ³öĻÖÅØŗńµÄ°×ŃĢ£¬ŗóŌŚÄŚ±ŚÄż½į³É°×É«¹ĢĢ唣Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
”” ””(1)ĪŖ“ļµ½ŹµŃéÄæµÄ£¬E×°ÖĆÖŠµÄŹŌ¼ĮŹĒ”””””””””” (ĢīŹŌ¼ĮĆū³Ę)£¬
”””””””” C×°ÖĆæÉŃ”ÓĆĻĀ±ķÖŠµÄ”””””””” ×°ÖĆ(Ģī×ÖÄø±ąŗÅ)£»
”” (2)ĪŖŹ¹ŹµŃéĖ³Ąū½ųŠŠ£¬Ēė¼ņŹöA”¢FÖŠµÄ·ÖŅŗĀ©¶·µÄÕżČ·²Ł×÷·½·Ø””””””””””””””””
”””””””” ”””””””””””””””””””””””””””””””””””””£
”” (3)×°ÖĆAÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””” £»µ±·“Ó¦¹ż³ĢÖŠ×ŖŅĘ5mole-£¬ŌņÉś³ÉµÄĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ŹĒ”””””””””” L£»
”” (4)½«×°ÖĆDÖŠÉś³ÉµÄ°×É«¹ĢĢåČ”³ö£¬²¢ÓėŹŹĮæŹģŹÆ»Ņ³ä·Ö»ģŗĻ¼ÓČČ£¬µĆµ½Ņ»ÖÖÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ唣
”””””””” Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½”””””””””””””””””””””””””””””””””””” £»
”” (5)×°ÖĆDÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””” £»
26£®(±¾Ģā¹²12·Ö)
”” (1)ijĪĀ¶ČĻĀ£¬ĻņĢå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė2molSO2ŗĶ1molO2”£2·ÖÖÓŗ󣬷“Ó¦“ļµ½Ę½ŗā”£“ĖŹ±²āµĆSO3µÄÅضČĪŖ0.5mol”¤L-1£¬ĘäĢå»ż·ÖŹżĪŖW%”£Ōņ2·ÖÖÓÄŚSO2µÄ·“Ó¦ĖŁĀŹĪŖ”””””””””””” ”£
”””””””” Čō“ļĘ½ŗāŗó£¬ŌŁĻņČŻĘ÷ÄŚĶØČė2molSO2ŗĶ1molO2(ČŻĘ÷Ģå»ż²»±ä)£¬µ±ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬SO3µÄĢå»ż·ÖŹż”””””””” W%(Ģī”°>”¢<»ņ=”±)
”” (2)øł¾ŻŃõ»Æ»¹Ō·“Ó¦£ŗ2Fe+2H2O+O2=2Fe(OH)2Éč¼ĘŅ»øöŌµē³Ų£¬Ōņ”””””””” ĪŖøŗ¼«£¬Õż¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ”””””””””””””””””””””””” ”£
”” (3)ŹŅĪĀĻĀÓŠĻĀĮŠĖÄÖÖČÜŅŗ
”””””””” ¢ŁpH=1°±Ė®”” ¢ŚpH=11µÄĒāŃõ»ÆÄĘ”” ¢ŪpH=3µÄ“×Ėį”” ¢ÜpH=3µÄĮņĖį
”””””””” Čō·Ö±š¼ÓĖ®¾łĻ”ŹĶ10±¶£¬ŌņpHÓɓ󵽊”µÄĖ³ŠņŹĒ”””””””””””” (ĢīŠņŗÅ)
”””””””” Čō½«¢Ł”¢¢ÜĮ½ČÜŅŗ°“Ņ»¶ØĢå»ż»ģŗĻĖłĖłµĆČÜŅŗµÄpH=7£¬“ĖŹ±ČÜŅŗÖŠŅ»¶Ø“ęŌŚc(SO42-)=”””””””””” c(NH4+)”£(ĢīŹż×Ö)
25£®(20·Ö)ČēĶ¼ĖłŹ¾£¬½šŹō°ōa“ÓøßĪŖh“¦Óɾ²Ö¹ŃŲ¹ā»¬µÄ»”ŠĪµ¼¹ģĻĀ»¬½ųČė¹ā»¬µ¼¹ģµÄĖ®Ę½²æ·Ö£¬µ¼¹ģµÄĖ®Ę½²æ·Ö“¦ÓŚŹśÖ±ĻņĻĀµÄŌČĒæ“ų”ÖŠ”£ŌŚĖ®Ę½²æ·ÖŌĻČ¾²Ö¹ÓŠĮķŅ»øł½šŹō°ōb£¬ŅŃÖŖma=2m,mb=m£¬ÕūøöĖ®Ę½µ¼¹ģ×ć¹»³¤£¬²¢“¦ÓŚ¹ćĄ«µÄŌČĒæ“ų”ÖŠ£¬¼ŁÉč½šŹō°ōaŹ¼ÖÕĆ»øś½šŹō°ōbĻąÅö£¬ÖŲĮ¦¼ÓĖŁ¶ČĪŖg”£Ēó£ŗ
”” (1)½šŹō°ōaøÕ½ųČėĖ®Ę½µ¼¹ģŹ±µÄĖŁ¶Č£»
”” (2)Į½°ōµÄ×īÖÕĖŁ¶Č£»
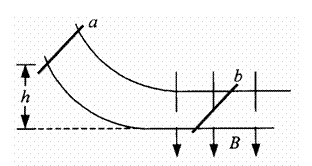 ”” (3)ŌŚÉĻŹöÕūøö¹ż³ĢÖŠĮ½øł½šŹō°ōŗĶµ¼¹ģĖł×é³ÉµÄ»ŲĀ·ÖŠĻūŗĵĵēÄÜ”£
”” (3)ŌŚÉĻŹöÕūøö¹ż³ĢÖŠĮ½øł½šŹō°ōŗĶµ¼¹ģĖł×é³ÉµÄ»ŲĀ·ÖŠĻūŗĵĵēÄÜ”£
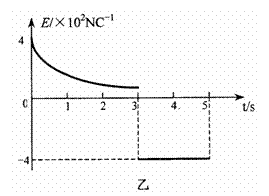
24£®(18·Ö)ČēĶ¼¼×ĖłŹ¾£¬Ņ»ÖŹĮæĪŖm=1©K”¢“ųµēĮæĪŖq=1.0”Į10-2CµÄĪļæé¾²Ö¹ŌŚ“Ö²Ś¾ųŌµĖ®Ę½ĆęÉĻµÄAµć”£“Ót=0Ź±æĢæŖŹ¼£¬ĪļæéŌŚµē³”Ēæ¶Č°“ČēĶ¼ŅŅĖłŹ¾¹ęĀɱä»ÆµÄĖ®Ę½µē³”×÷ÓĆĻĀĻņÓŅŌĖ¶Æ£¬µŚ3sÄ©ĪļæéŌĖ¶Æµ½BµćŹ±ĖŁ¶ČøÕŗĆĪŖ0£¬µŚ5sÄ©ĪļæéøÕŗĆ»Ųµ½Aµć”£ŅŃÖŖĪļæéÓė“Ö²ŚĖ®Ę½Ćę¼äµÄ¶ÆĦ²ĮŅņŹż¦Ģ=0.2£¬Č”g=10m/s2”£Ēó£ŗ
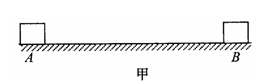 ”” (1)AB¼äµÄ¾ąĄė£»
”” (1)AB¼äµÄ¾ąĄė£»
”” (2)µē³”Į¦ŌŚ5sŹ±¼äÄŚ¶ŌĪļæéĖł×ö¹¦”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com