
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
2.гаЙиЯИАћКЫКЭЯИАћжЪвХДЋЕФа№ЪіЃЌе§ШЗЕФЪЧ
ЂйЯИАћжЪвХДЋЃЌСНЧзБОдгНЛЕФКѓДњЃЌвВПЩФмЛсГіЯжадзДЗжРыЁЁ ЂкКьТЬЩЋУЄвХДЋЃЌВЛБэЯжЮЊУЯЕТЖћвХДЋЕФЗжРыБШЃЌЪєгкЯИАћжЪвХДЋЁЁ ЂлвХДЋЮяжЪЗжБ№ЪЧDNAКЭRNAЁЁ ЂмКњТмВЗИљзщжЏХрбјЕФЗБжГЙ§ГЬВЛзёбУЯЕТЖћвХДЋЖЈТЩЁЁ
A.ЂйЂлЂмЁЁ B.ЂлЂмЁЁ C.ЂмЁЁЁЁ D.ЂйЂм
1.ЯТСагаЙиЩњЬЌЯЕЭГНсЙЙЕФа№ЪіЃЌе§ШЗЕФЪЧЃК
AЃЎУПжжЩњЮядкЩњЬЌЯЕЭГжажЛФмДІдквЛИігЊбјМЖЩЯ
BЃЎЖЏЮяЖМЪєгкЯћЗбепЃЌЦфжаЪГВнЖЏЮяДІгкЕкЖўгЊбјМЖ
CЃЎздбјЩњЮяЖМЪЧЩњВњепЃЌЪЧЩњЬЌЯЕЭГЕФжївЊГЩЗж
DЃЎЯИОњЖМЪєгкЗжНтепЃЌЦфвьЛЏзїгУРраЭгаашбѕаЭКЭбсбѕаЭСНРр
34ЁЂ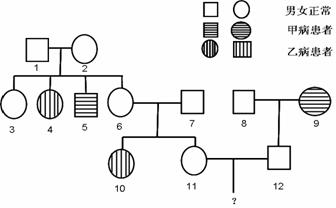 (14Зж)ЯТЭМЪЧФГМвзхЕФЯЕЦзЭМЃЌдкетИіМвзхжагаСНжжвХДЋВЁМз(ЛљвђЮЊAЁЂa)КЭвв(ЛљвђЮЊBЁЂb)ЃЌввВЁЛМепЕФадШОЩЋЬхгыФаадЯрЭЌЃЌЬхФкгаиКЭшЃЌЭтУВгые§ГЃХЎадвЛбљЃЌЕЋОљБэЯжВЛг§ЁЃМвзхжа7КХИіЬхЮоМзжТВЁЛљвђЃЌ1КХИіЬхЮоввВЁжТВЁЛљвђЁЃЧыИљОнЭМЦзЛиД№ЯТСаЮЪЬтЃК
(14Зж)ЯТЭМЪЧФГМвзхЕФЯЕЦзЭМЃЌдкетИіМвзхжагаСНжжвХДЋВЁМз(ЛљвђЮЊAЁЂa)КЭвв(ЛљвђЮЊBЁЂb)ЃЌввВЁЛМепЕФадШОЩЋЬхгыФаадЯрЭЌЃЌЬхФкгаиКЭшЃЌЭтУВгые§ГЃХЎадвЛбљЃЌЕЋОљБэЯжВЛг§ЁЃМвзхжа7КХИіЬхЮоМзжТВЁЛљвђЃЌ1КХИіЬхЮоввВЁжТВЁЛљвђЁЃЧыИљОнЭМЦзЛиД№ЯТСаЮЪЬтЃК
(1)МзВЁЕФвХДЋЗНЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛввВЁЕФвХДЋЗНЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)4КХИіЬхЕФЛљвђаЭПЩФмЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ5КХИіЬхЕФЛљвђЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)11КХКЭ12КХИіЬхНсЛщЃЌЩњЯТвЛИіЛММзВЁКЂзгЕФИХТЪЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ
ЛММзВЁЕЋВЛЛМввВЁЕФКЂзгЕФИХТЪЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ШчЙћжЛПМТЧввВЁЃЌЧыгУвХДЋЭМНтЃЌвд6КЭ7КХИіЬхЮЊР§ЃЌНтЪЭдкетИіМвзхжаХЎШЫЬиБ№ЖрЕФЯжЯѓЁЃ
2010НьжиЕужабЇСЊПМ
33.(9Зж)ЗЂЩњуыДЈДѓЕие№ЕФСњУХЩНЕие№ДјЪЧЮвЙњЩњЮяЖрбљадБЃЛЄЕФЙиМќЧјгђЃЌ 80%ЕФДѓамУЈжжШКЁЂЮвЙњНќ1/5ЕФЬигажжзгжВЮяЪєжж(ШчОУИКЪЂУћЕФжаЙњИызгЪї--чюЭЉ)ОљЗжВМгкДЫЁЃОнВЛЭъШЋЭГМЦЃЌЕие№КѓжВБЛЛйЫ№ДяЕН30%вдЩЯЃЌЛЙГіЯжСЫ200УзПэЁЂ1ЙЋРяГЄЁЂ30УзКёЕФДѓаЭФрЪЏСїДјЁЃЯТЭМЮЊЕие№ЛйЫ№ЕФФГздШЛБЃЛЄЧјШЫЮЊИЩдЄЯТЛжИДЙ§ГЬЕФФмСПСїЖЏЭМ(ЕЅЮЛЮЊ103kJ/m2ЁЄy)ЁЃ
ЁЁ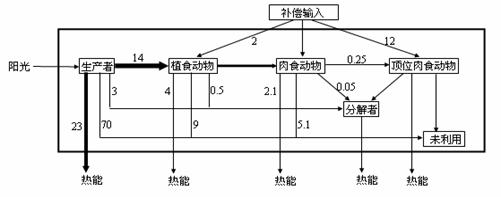
(1)ЪГЮяСДжаЃЌГ§ЩњВњепЭтЦфЫќгЊбјМЖашвЊВЙГЅФмСПЪфШыЕФдвђЪЧ_ЁЁЁЁЁЁЁЁЁЁ ЁЁ_ЁЃ
(2)МЦЫуПЩжЊЃЌШтЪГадЖЏЮяашВЙГЅЪфШыЕФФмСПжЕЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ______ЁЃгЩЭМПЩжЊгЊбјМЖ____________(ЬюЁАНЯИпЁБЛђЁАНЯЕЭЁБ)ЕФЩњЮяЃЌдкетГЁЕие№жаЪмЕНЕФгАЯьНЯДѓЁЃ
(3)дкШЫЮЊИЩдЄЯТЃЌФмСПдкЕкЖўгЊбјМЖЕНЕкШ§гЊбјМЖжЎМфДЋЕнаЇТЪЮЊ_________ЁЃ
(4)дкЩњЬЌЯЕЭГжаФмСПЕФДЋЕнаЇТЪЮЊЪВУДжЛга10-20%ЃЌдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(5)ЪдЗжЮіЯрЙиФрЪЏСїДјЖдИУЧјгђамУЈЗБжГдьГЩЕФПЩФмгАЯьЃК____________ЁЁЁЁЁЁ ____ЁЃ
32ЃЎ(8Зж)НЕИЦЫиРДдДгкМззДЯйТЫХнХдЯИАћ(CЯИАћ)ЃЌЪЧгЩ32ИіАБЛљЫсзщГЩЕФЕЅСДЖрыФЃЌЯрЖдЗжзгжЪСПЮЊ3400ЁЃе§ГЃбЊЧхжаЕФНЕИЦЫиХЈЖШЮЊ10~20mg/LЁЃзїгУжївЊЪЧДйНјГЩЙЧЯИАћЛюЖЏЪЙЙЧбЮГСзХгкЙЧжЪЃЌВЂвжжЦЮИГІЕРКЭЩіаЁЙмЮќЪеИЦРызгЃЌЪЙбЊИЦХЈЖШНЕЕЭЁЃЧыгУЫљИјЕФЪЕбщВФСЯКЭгУОпЩшМЦЪЕбщЃЌЪЙЦфФмЭЌЪБбщжЄНЕИЦЫиФмЙЛЪЙаЁЪѓМЁШтОЗТЮВЂЧвЪЧгЩгкНЕЕЭСЫбЊИЦЕФдвђЁЃвЊЧѓаДГіЪЕбщВНжшЁЂдЄВтЪЕбщНсЙћВЂЕУГіНсТлЁЃ
ЪЕбщВФСЯгыгУОпЃКе§ГЃЕФаЁЪѓШєИЩжЛЁЂ10%ЕФТШЛЏИЦШмвКЁЂЩњРэбЮЫЎЁЂЪЪгІХЈЖШЕФНЕИЦЫиШмвКЁЃ
ЪЕбщВНжшЃК
 ЂйНЋе§ГЃЕФаЁЪѓЫцЛњЗжГЩA(ЪЕбщзщ)ЁЂB(Ждеезщ)СНзщЃЌЙлВьВЂМЧТМЦфЛюЖЏзДПіЁЃ
ЂйНЋе§ГЃЕФаЁЪѓЫцЛњЗжГЩA(ЪЕбщзщ)ЁЂB(Ждеезщ)СНзщЃЌЙлВьВЂМЧТМЦфЛюЖЏзДПіЁЃ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂлШєГіЯжЕЭбЊИЦжЂзД(МЁШтОЗТЮ)КѓЃЌдйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦЪЕбщНсЙћдЄВтНсТлЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃНсТлЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
31ЁЂ(ЙВ11Зж)ЧыЛиД№ЯТСагаЙижВЮяЯИАћДњаЛгаЙиЕФЮЪЬтЁЃ
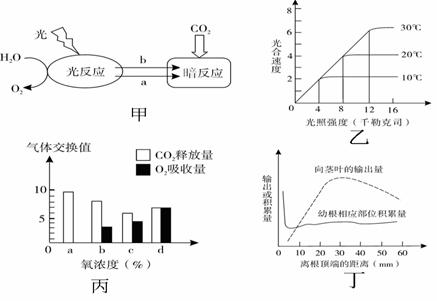
(1)ЭММзжаa ЮяжЪЕФаЮГЩЙ§ГЬжаЃЌЮЛгквЖТЬЬхЕФРрФвЬхФЄЩЯЕФЁЁ ЁЁЁЁНЋЙтФмзЊЛЛГЩЕчФмЁЃЁЁЁЁ
(2)ЭМввБэЪОдкЖўбѕЛЏЬМГфзуЕФЬѕМўЯТЃЌФГжВЮяЙтКЯЫйЖШгыЙтееЧПЖШКЭЮТЖШЕФЙиЯЕЁЃдкЮТЖШЮЊ10ЁцЪБЃЌЙтееЧПЖШДѓгкЁЁ ЁЁЁЁЧЇРеПЫЫОКѓЃЌИУжВжъЙтКЯЫйЖШВЛдйЫцЙтееЧПЖШдіМгЖјдіМгЁЃЕБЮТЖШЮЊ20ЁцЪБЃЌЙтееЧПЖШгЩ4ЧЇРеПЫЫОЫВЪБЩЯЩ§жС12ЧЇРеПЫЫОЃЌДЫПЬИУжВжъвЖТЬЬхФкC5ЛЏКЯЮя(RuBP)ЕФКЌСПНЋЁЁЁЁ ЁЃЕБЮТЖШЮЊ30ЁцЁЂЙтееЧПЖШаЁгк12ЧЇРеПЫЫОЪБЃЌЯожЦИУжВжъЙтКЯЫйЖШЕФвђЫиЪЧЁЁЁЁ ЁЁЁЁЁЁЁЃ
(3)ЭМБћБэЪОФГжВЮяЕФЗЧТЬЩЋЦїЙйдкбѕХЈЖШЮЊaЁЂbЁЂcЁЂdЪБЃЌCO2ЪЭЗХСПКЭO2ЮќЪеСПЕФЙиЯЕЭМЃЌдкaЁЂbЁЂcЁЂdЫФХЈЖШжа,зюЪЪКЯИУжВЮяЦїЙйДЂВиЕФбѕХЈЖШЪЧЁЁ ЁЁЁЁЃЛШєЯИАћКєЮќЕФЕзЮяЪЧЦЯЬбЬЧЃЌдђдкбѕХЈЖШЮЊbЪБЃЌбсбѕКєЮќЯћКФЦЯЬбЬЧЕФСПЪЧашбѕКєЮќЕФЯћКФЦЯЬбЬЧЕФСПЁЁ ЁЁЁЁБЖЁЃ
(4)ЖЁЭМБэЪОдкЪЪвЫЕФЬѕМўЯТЃЌвЛЖЈЪБМфФкФГЮоЛњРызгДгДѓТѓгзИљВЛЭЌВПЮЛЯђОЅвЖЕФЪфГіСПКЭдкДѓТѓгзИљЯргІВПЮЛЛ§РлСПЕФБфЛЏЁЃдкздШЛЧщПіЯТЃЌЭСШРжаИУЮоЛњРызгЕФХЈЖШБШИљЯИАћжаИУЮоЛњРызгЕФХЈЖШЁЁ ЁЁ(ЕЭЁЂИп)ЃЌЫљвдгзИљБэЦЄЯИАћЪЧЭЈЙ§ ЁЁ ЁЁЗНЪНЮќЪеЭСШРжаИУЮоЛњРызгЁЃжЛвРОнЁАгзИљЯргІВПЮЛЛ§РлСПЁББфЛЏЕФЧњЯпВЛФмШЗЖЈгзИљ20-60mmВПЮЛЖдИУЮоЛњРызгЕФЮќЪеСПЃЌРэгЩЪЧЁЁЁЁЁЁЁЁ ЁЁЁЃ
30.(16Зж)ввЛљЯуВнШЉ(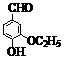 )ЪЧЪГЦЗЬэМгМСЕФдіЯудСЯЃЌЦфЯуЮЖБШЯуВнШЉИќМгХЈгєЁЃ
)ЪЧЪГЦЗЬэМгМСЕФдіЯудСЯЃЌЦфЯуЮЖБШЯуВнШЉИќМгХЈгєЁЃ
(1)аДГіввЛљЯуВнШЉЗжзгжаСНжжКЌбѕЙйФмЭХЕФУћГЦ_______________________ЁЃ
(2)ввЛљЯуВнШЉЕФЭЌЗжвьЙЙЬхAЪЧвЛжжгаЛњЫсЃЌAПЩЗЂЩњвдЯТБфЛЏЃК
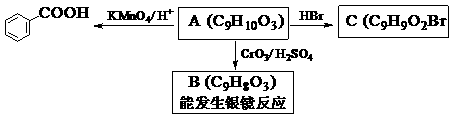
ЬсЪОЃКЂйRCH2OH RCHOЃЛ
RCHOЃЛ
ЂкгыБНЛЗжБНгЯрСЌЕФЬМдзгЩЯгаЧтЪБЃЌДЫЬМдзгВХПЩБЛЫсадKMnO4ШмвКбѕЛЏЮЊєШЛљЁЃ
(a)гЩAЁњCЕФЗДгІЪєгк_______________(ЬюЗДгІРраЭ)ЁЃ
(b)аДГіAЕФНсЙЙМђЪН________________________ЁЃ
(3)ввЛљЯуВнШЉЕФСэвЛжжЭЌЗжвьЙЙЬхD(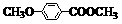 )ЪЧвЛжжвНвЉжаМфЬхЁЃЧыЩшМЦКЯРэЗНАИгУмюЯуШЉ(
)ЪЧвЛжжвНвЉжаМфЬхЁЃЧыЩшМЦКЯРэЗНАИгУмюЯуШЉ(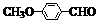 )КЯГЩD(ЦфЫћдСЯздбЁЃЌгУЗДгІСїГЬЭМБэЪОЃЌВЂзЂУїБивЊЕФЗДгІЬѕМў)ЁЃ
)КЯГЩD(ЦфЫћдСЯздбЁЃЌгУЗДгІСїГЬЭМБэЪОЃЌВЂзЂУїБивЊЕФЗДгІЬѕМў)ЁЃ
Р§ШчЃК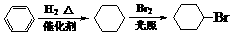
(4)ЧыаДГіввЛљЯуВнШЉЗћКЯвдЯТЬѕМўЕФЭЌЗжвьЙЙЬхЕФжжРрЪ§__________(ЬюЪ§зж)ЁЃ
ЂйКЌБНЛЗЃЌгаСНИіЖдЮЛЕФШЁДњЛљЃЛЂкФмЗЂЩњвјОЕЗДгІЃЌФмЪЙFe3+ШмвКБфзЯЩЋЃЛЂлЪєгкѕЅРрЁЃ
29ЃЎ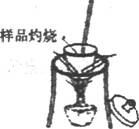 (14Зж)ДПМюЪЧЙЄвЕЩњВњКЭШеГЃЩњЛюжаЕФживЊЮяжЪЁЃФГаЫШЄаЁзщЮЊВтЖЈФГЙЄвЕДПМю(МйЩшНіКЌЬМЫсЧтФЦдгжЪ)жаЬМЫсФЦЕФжЪСПЗжЪ§ЃЌЩшМЦСЫЯТСаШ§жжЪЕбщЗНАИНјааЬНОПЁЃЧыЬюПеЃКЁЁ
(14Зж)ДПМюЪЧЙЄвЕЩњВњКЭШеГЃЩњЛюжаЕФживЊЮяжЪЁЃФГаЫШЄаЁзщЮЊВтЖЈФГЙЄвЕДПМю(МйЩшНіКЌЬМЫсЧтФЦдгжЪ)жаЬМЫсФЦЕФжЪСПЗжЪ§ЃЌЩшМЦСЫЯТСаШ§жжЪЕбщЗНАИНјааЬНОПЁЃЧыЬюПеЃКЁЁ
ЗНАИвЛЃКДПМюбљЦЗ ВтЖЈЪЃгрЙЬЬхжЪСП
ВтЖЈЪЃгрЙЬЬхжЪСП
(1)ЗжБ№ГЦШЁИЩдялсліКЭДПМюбљЦЗЕФжЪСПЃЌНЋДПМюбљЦЗЗХШылсліжаГфЗж
МгШШ(ШчгвЭМ)ЁЃлсліжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)НЋлсліжУгкИЩдяЦїжаРфШДКѓГЦСПЁЃЪЕбщЪБашвЊжиИДЁАМгШШвЛРфШДвЛ
ГЦСПЁБВйзїЖрДЮЃЌЦфФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЗНАИЖўЃКДПМюбљЦЗШмвК ВтЖЈГСЕэжЪСП
ВтЖЈГСЕэжЪСП
(3)ГЦШЁm 1gбљЦЗЃЌжУгкаЁЩеБжаЃЌМгЫЎШмНтЁЃЯђаЁЩеБжаЕЮМгзуСП
ТШЛЏИЦШмвКЁЃНЋЗДгІЛьКЭЮяЙ§ТЫКѓЕФЯТвЛВНВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)ГСЕэОИЩдяКѓГЦСПЮЊm 2g,дђИУбљЦЗжаЬМЫсФЦЕФжЪСПЗжЪ§ЮЊЁЁЁЁЁЁЁЁЁЁ
(5)ШчЙћгУЧтбѕЛЏИЦШмвКДњЬцТШЛЏИЦШмвКзїГСЕэМСЃЌдкЦфЫћВйзїе§ШЗЕФ
ЧщПіЯТЃЌВтЕУбљЦЗжаЕФЬМЫсФЦжЪСПЗжЪ§НЋБШЪЕМЪЁЁЁЁЁЁЁЁ (ЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАВЛБфЁБ)ЁЃ
ЗНАИШ§ЃКДПМюбљЦЗ ВтЖЈЩњГЩCO2ЕФжЪСП
ВтЖЈЩњГЩCO2ЕФжЪСП
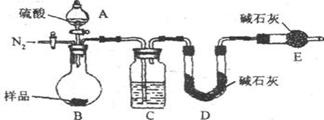
(6)ЗДгІЧАКѓЖМвЊЭЈШыN2ЃЌЗДгІЧАЭЈШыN2ЕФФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(7)ШчЙћУЛгаИЩдяЙмEЃЌдкЦфЫћВйзїе§ШЗЕФЧщПіЯТЃЌВтЕУбљЦЗжаЕФЬМЫсФЦжЪСПЗжЪ§НЋБШЪЕМЪЁЁЁЁЁЁЁЁ (ЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАВЛБфЁБ)
28ЃЎ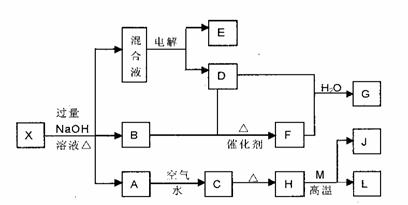 (15Зж)гавЛЛЏКЯЮяXЃЌЦфЫЎШмвКЮЊЧГТЬЩЋЃЌПЩЗЂЩњШчЯТЕФзЊЛЏЙиЯЕ(ВПЗжЗДгІЮяЁЂЩњГЩЮяДгТд)ЁЃЦфжаBЁЂDЁЂEЁЂFОљЮЊЮоЩЋЦјЬхЃЌMЁЂLЮЊГЃМћЕФН№ЪєЕЅжЪЃЌCЮЊФбШмгкЫЎЕФКьКжЩЋЙЬЬхЁЃдкЛьКЯвКжаМгШыBaCl2ШмвКПЩЩњГЩВЛШмгкЯЁбЮЫсЕФАзЩЋГСЕэЃЌHКЭMЗДгІПЩЗХГіДѓСПЕФШШЁЃ
(15Зж)гавЛЛЏКЯЮяXЃЌЦфЫЎШмвКЮЊЧГТЬЩЋЃЌПЩЗЂЩњШчЯТЕФзЊЛЏЙиЯЕ(ВПЗжЗДгІЮяЁЂЩњГЩЮяДгТд)ЁЃЦфжаBЁЂDЁЂEЁЂFОљЮЊЮоЩЋЦјЬхЃЌMЁЂLЮЊГЃМћЕФН№ЪєЕЅжЪЃЌCЮЊФбШмгкЫЎЕФКьКжЩЋЙЬЬхЁЃдкЛьКЯвКжаМгШыBaCl2ШмвКПЩЩњГЩВЛШмгкЯЁбЮЫсЕФАзЩЋГСЕэЃЌHКЭMЗДгІПЩЗХГіДѓСПЕФШШЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЮяжЪXЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)ЕчНтЛьКЯвКЪБбєМЋЗДгІЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)АДвЊЧѓаДГіЩЯЪізЊЛЏЙиЯЕжагаЙиЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЂйКЌгаLдЊЫиЕФЛЏКЯЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкКЌгаLдЊЫиЕФжУЛЛЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)LгыЙ§СПGЕФЯЁШмвКЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(5)вбжЊa g EЦјЬхдкDжаЭъШЋШМЩеЩњГЩЮШЖЈЕФЛЏКЯЮяЪБЃЌЗХГіb kJЕФШШСПЃЌаДГіEШМЩеШШЕФШШЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
27ЃЎ(15Зж)ЧыАДвЊЧѓЛиД№ЮЪЬтЃК
ЂёЃЎ(5Зж)XЁЂYЁЂWЁЂQЖМЪЧЖЬжмЦкдЊЫиЃЌвбжЊYЁЂXЁЂWЁЂQЕФдзгАыОЖвРДЮдіДѓЃЌXЁЂYЭЌжмЦкЃЌXЁЂWЭЌжїзхЃЌWдзгКЫФкЕФжЪзгЪ§ЕШгкXЁЂYдзгКЫФкЕФжЪзгЪ§жЎКЭЃЌWдзгзюЭтВуЕФЕчзгЪ§ЪЧQдзгзюЭтВуЕчзгЪ§ЕФ3БЖ
ЪдЛиД№ЯТСаЮЪЬтЃК
(1)YЁЂWЁЂQШ§жждЊЫиаЮГЩЕФМђЕЅРызгЕФАыОЖгЩДѓЕНаЁЕФЫГађЪЧ(дЊЫиЗћКХБэЪО)ЁЁЁЁЁЁ ЁЃЁЁ
(2)НігЩYЁЂWСНдЊЫизщГЩЕФвѕРызгЕФЫЎНтЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂђЃЎ(5Зж)дк25ЁцЪБЃЌгУЪЏФЋЕчМЋЕчНт100mL 1molЁЄL-1 AgNO3ШмвКЃЌШчга0.2molЕчзгЗЂЩњзЊвЦЃЌЪдЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)вѕМЋЩЯЗЂЩњЕФЕчМЋЗДгІЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (2)БъзМзДПіЯТЗДгІЙВВњЩњЕФЦјЬхЬхЛ§ЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
Ђѓ.(5Зж)ИжЬњЁАЗЂРЖЁБЪЧдкИжЬњБэУцаЮГЩвЛВужТУмЕФFe3O4БЁФЄЕФММЪѕЁЃЦфжавЛжжЗНЗЈЪЧНЋИжЬњжЦЦЗНўЕНNaNO2КЭХЈNaOHЕФЛьКЯШмвКжаМгШШЕН130ЁцЁЃЦфЙ§ГЬПЩвдгУШчЯТЛЏбЇЗНГЬЪНБэЪОЃК
Ђй3Fe+NaNO2+5NaOHЃН3Na2FeO2+H2O+NH3Ёќ
Ђк6Na2FeO2+NaNO2+5H2OЃН3Na2Fe2O4+NH3Ёќ+7NaOH
ЂлNa2FeO2+Na2Fe2O4+2H2OЃНFe3O4+4NaOH
дђЗДгІЂкжаЕФбѕЛЏМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЛЏбЇЪН)ЃЌећИіЗДгІЙ§ГЬжаЃЌУПга168 g FeВЮМгЗДгІ,дђзЊвЦЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ molЕчзгЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com