
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
2Θ°
(1) NaHCO3ΘΜΓΓ Al(OH)3
(2) HCO3Θ≠ + H+ ΘΫ H2O +CO2Γϋ
(3) Al(OH)3 + 3H+ ΘΫ Al3+ + 3H2O Θ§ Al(OH)3 + OHΘ≠ ΘΫ AlO2Θ≠ + 2H2O
1Θ°
|
”Π”Ο |
ΆΤ≤βΕΰ―θΜ·ΙηΥυΨΏ”–ΒΡ–‘÷ (–¥≥ωœύΙΊΖΫ≥Χ Ϋ) |
|
ΡΞΝœΘ§Φ”ΙΛ”ώ · |
”≤Ε»¥σ |
|
έαέω |
»έΒψΗΏ |
|
·”Δέαέω≤ΜΡήΦ”»»«β―θΜ·ΡΤ |
SiO2 + 2NaOH ==
Na2SiO3 + H2O |
|
”Ο«βΖζΥα‘Ύ≤ΘΝß…œΒώΜ® |
SiO2
+ 4HF == SiF4Γϋ + 2H2O |
|
Τ’Ά®œΓΈόΜζΥαΩ…«εœ¥ |
Μ·―ß–‘÷ ΫœΈ»Ε® |
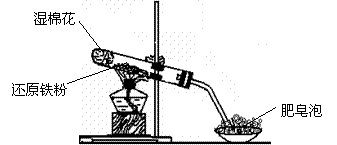
7Θ°Ρ≥Ά§―ßάϊ”Οœ¬ΆΦΥυ ΨΒΡ Β―ιΉΑ÷ΟΫχ––ΧζΗζΥ°’τΤχΖ¥”ΠΒΡ Β―ιΘ§≤ΔΦΧ–χ―–ΨΩΧζΦΑΤδΜ·ΚœΈοΒΡ≤ΩΖ÷–‘÷ ΓΘ
 ΓΓ
ΓΓ
«κΜΊ¥πœ¬Ν–Έ ΧβΓΘ
(1)”≤÷ ‘Ιή÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)ΗΟΆ§―ß”ϊ»ΖΕ®Ζ¥”ΠΚσ”≤÷ ‘Ιή÷–ΙΧΧεΈο÷ ΒΡ≥…Ζ÷Θ§…ηΦΤΝΥ»γœ¬ Β―ιΖΫΑΗΘΚ
ΔΌ¥ΐ”≤÷ ‘Ιήά以ΚσΘ§»Γ…Ό–μΤδ÷–ΒΡΙΧΧεΈο÷ »ή”ΎœΓΝρΥαΒΟ»ή“ΚBΘΜ
ΔΎ»Γ…ΌΝΩ»ή“ΚBΒΈΦ”KSCN»ή“ΚΘ§»τ»ή“Κ±δΚλ…Ϊ‘ρΥΒΟς”≤÷ ‘Ιή÷–ΙΧΧεΈο÷ ΒΡ≥…Ζ÷ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§»τ»ή“ΚΈ¥±δΚλ…Ϊ‘ρΥΒΟς”≤÷ ‘Ιή÷–ΙΧΧεΈο÷ ΒΡ≥…Ζ÷ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
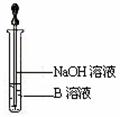
(3)ΗΟΆ§―ßΑ¥…œ ω Β―ιΖΫΑΗΫχ––ΝΥ Β―ιΘ§ΫαΙϊ»ή“ΚΈ¥±δΚλ…ΪΘ§‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΘ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΘ
(4)ΗΟΆ§―ß¬μ…œΝμ»Γ…ΌΝΩ»ή“ΚBΘ§ ΙΤδΗζNaOH»ή“ΚΖ¥”ΠΓΘ»τΑ¥”“ΆΦΥυ ΨΒΡ≤ΌΉςΘ§Ω…Ιέ≤λΒΫ…ζ≥…ΑΉ…Ϊ≥ΝΒμΘ§―ΗΥΌ±δ≥…Μ“¬Χ…ΪΘ§ΉνΚσ±δ≥…ΚλΚ÷…ΪΒΡœ÷œσΘ§«κ–¥≥ω”κ…œ ωœ÷œσœύΙΊΒΡΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(5)“ΜΕΈ ±ΦδΚσΘ§ΗΟΆ§―ßΖΔœ÷(3)÷–Έ¥±δΚλΒΡ»ή“Κ±δ≥…Κλ…ΪΘ§ΥΒΟςFe2+ ΨΏ”–ΓΓΓΓΓΓ –‘ΓΘ”…¥ΥΩ…÷ΣΘ§ Β―ι “÷–Κ§Fe2+ΒΡ―Έ»ή“Κœ÷”Οœ÷≈δ÷ΤΒΡ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
≤Δ«“≈δ÷ΤΚ§Fe2+ΒΡ―Έ»ή“Κ ±”ΠΦ”»κ…ΌΝΩΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
±Ί–ό1ΡΘΩι≥ΘΦϊΈόΜζΈοΗ¥œΑ≈δΧΉΝΖœΑ(»ΐ)
6Θ°”–“ΜΑϋΑΉ…ΪΙΧΧε(“Μ÷÷Εΰ‘ΣΥαΒΡ’ΐ―Έ)Θ§œ¬±μΈΣΫχ––œύΙΊ Β―ιΒΡ≤ΩΖ÷ Β―ι±®ΗφΓΘ
(1)«κΗυΨί Β―ιœ÷œσΘ§ΫΪΡψΉς≥ωΒΡ≈–ΕœΧν‘Ύ±μΗώΡΎΒΡœύ”ΠΈΜ÷ΟΓΘ
|
≤Ϋ÷η–ρΚ≈ |
≤ΌΉς |
Β―ιœ÷œσ |
≈–ΓΓΓΓΓΓ Εœ |
|
ΔΌ |
ΓΓ»ΓΙΧΧε»ή”ΎΥ°Θ§ΒΟ»ή“ΚX |
ΒΟΒΫΈό…Ϊ»ή“Κ |
ΓΓ |
|
ΔΎ |
»Γ…ΌΝΩ»ή“ΚXΘ§Φ”»κ¬»Μ·±Β»ή“Κ |
…ζ≥…ΑΉ…Ϊ≥ΝΒμ |
Ω…ΡήΚ§”–__________(ΧνάκΉ”ΖϊΚ≈) |
|
Δέ |
»Γ…ΌΝΩ»ή“ΚXΘ§Φ”»κ≈®«β―θΜ·ΡΤ»ή“ΚΘ§Φ”»»Θ§≤Δ‘Ύ ‘ΙήΩΎ”Ο Σ»σΒΡΚλ…Ϊ ·»ο ‘÷ΫΦλ―ι |
‘÷Ϋ±δάΕ |
Κ§”–_____________(ΧνάκΉ”ΖϊΚ≈) |
|
Ϋα¬έΘΚ¥ΥΑΉ…ΪΙΧΧεΩ…Ρή «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΘ |
(2)»τœκ»Ζ»œ¥ΥΑΉ…ΪΙΧΧεΒΡ≥…Ζ÷Θ§”Π‘Ύ≤Ϋ÷ηΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (Χν≤Ϋ÷η–ρΚ≈)÷–Φ”»κ ‘ΦΝAΘ§ ‘ΦΝAΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)»τ‘Ύ≤Ϋ÷ηΔΎΒΡ≤ΌΉς÷–Θ§Φ”»κ ‘ΦΝAΚσ»‘”–ΑΉ…Ϊ≥ΝΒμΘ§–¥≥ωΨί¥Υ»Ζ»œΒΡ»ή“ΚX”κ«β―θΜ·±Β»ή“ΚΦ”»»Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
5Θ° Β―ι “άοΆ®≥Θ”ΟMnO2”κ≈®―ΈΥαΖ¥”Π÷Τ»Γ¬»ΤχΘ§ΤδΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ
MnO2 + 4HCl(≈®) ==== MnCl2 + Cl2Γϋ+ 2H2O
(1)‘ΎΗΟΖ¥”Π÷–Θ§―θΜ·ΦΝ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§»γ”–1 mol Cl2…ζ≥…Θ§±Μ―θΜ·ΒΡHClΒΡΈο÷ ΒΡΝΩ «
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ molΘ§ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ molΘΜ
(2)ΫΪ÷ΤΒΟ¬»ΤχΆ®»κάδΒΡœϊ ·Μ“[Ca(OH)2 ]÷–Φ¥Ω…÷ΤΒΟΤ·ΑΉΖέΘ§ΤδΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ‘ΎΡ≥Έ¬Ε»œ¬Θ§ΫΪCl2Ά®»κNaOH»ή“Κ÷–Θ§Ζ¥”ΠΒΟΒΫΚ§”–ClO-”κClO3-Έο÷ ΒΡΝΩ÷°±»ΈΣ1ΓΟ1ΒΡΜλΚœ“ΚΘ§¥ΥΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
(3)Ϋχ––”–ΙΊ¬»ΤχΒΡ–‘÷ Β―ι ±Θ§–η2.24 LΒΡ¬»Τχ(±ξΉΦΉ¥Ωω)Θ§άμ¬έ…œ–η“ΣMnO2ΙΧΧεΒΡ÷ ΝΩΈΣ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ(≈®―ΈΥαΉψΝΩ)
(4)«ΑΕΈ ±ΦδΘ§±®÷Ϋ±®ΒάΝΥΕύΤπΈά…ζΦδ«εœ¥ ±Θ§“ρΜλΚœ Ι”ΟΓΑΫύ≤όΝιΓ±(÷ς“Σ≥…Ζ÷ «―ΈΥα)”κΓΑ84œϊΕΨ“ΚΓ±(÷ς“Σ≥…Ζ÷ «NaClO)Ζą欻Τχ÷–ΕΨΒΡ ¬ΦΰΓΘ ‘ΗυΨίΡψΒΡΜ·―ß÷Σ ΕΖ÷ΈωΘ§‘≠“ρ «(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
4Θ°Ζ÷άύΖ®‘ΎΜ·―ß―ßœΑ÷–”Π”ΟΖ«≥ΘΙψΖΚΓΘ
ΓΓœ÷”–“‘œ¬5÷÷Έο÷ ΘΚΔΌSO2ΓΔΔΎH2OΓΔΔέCO2ΓΔΔήCuSO4ΓΔΔίCH4ΚΆO2ΒΡΜλΚœΤχΧε(ΧεΜΐ±»ΈΣ2ΘΚ1)ΓΘ
ΓΓ (1)Χν–¥œ¬±μΩ’ΑΉΓΘ
|
ΓΓ –ρΚ≈ |
ΗΟάύ±πΒΡΈο÷ |
Ζ÷άύ±ξΉΦ |
|
ΨΌάΐ |
ΔΌΓΔΔή |
ΕΦΚ§”–Νρ‘ΣΥΊ |
|
AΉι |
ΔΌΓΔ |
ΓΓ |
|
BΉι |
ΔΌΓΔ |
ΓΓ |
|
CΉι |
ΔΌΓΔ |
ΓΓ |
(2)ΫΪSO2Ά®»κ≥Έ«ε ·Μ“Υ°÷–Θ§“ΜΑψΩ¥≤ΜΒΫΟςœ‘œ÷œσΘ§ΒΪ «¥Υ ±œρΗΟ»ή“Κ÷–ΒΈΦ”NaOH»ή“ΚΘ§”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΓΘ«κΗυΨί(1)÷–ΒΡΡ≥ΉιΖ÷άύΖ÷Έω‘≠“ρΘ§–¥≥ωœύ”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΘ
ΓΓΓΓ ΔΌΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(3)SO2ΚΆFe2+ΓΔN2”–œύΥΤ÷°¥ΠΓΘΥϋΟ«ΒΡœύΥΤ÷°¥Π‘Ύœ¬Ν–Ζ¥”Π÷–Ω…“‘Χεœ÷Θ§«κΆξ≥…œύ”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΘ
ΓΓ ΔΌSO2 + 2H2S ===ΓΓΓΓΓΓΓΓ + 2H2OΓΓΓΓΓΓΓΓΓΓΓΓ SO2 + Br2 + 2H2O ==ΓΓΓΓΓΓΓΓ +ΓΓΓΓΓΓΓΓ
ΓΓ ΔΎFe2+ + Zn ==== Zn2+ + FeΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Fe2+ + Cl2 ==== Fe3+ +2Cl-
ΓΓ ΔέN2 +3MgΓΓ ΓΓΓΓΗΏΈ¬ΓΓ ΓΓMg3N2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ N2 + O2 ΓΓΖ≈ΒγΓΓ ΓΓ2NO
3Θ°Ρ≥Έό…ΪΆΗΟς»ή“Κ÷–Ω…ΡήΚ§”–œ¬Ν–άκΉ”ΘΚK+ΓΔH+ΓΔBa 2+ΓΔOH-ΓΔCO32-ΓΔCl-ΓΔNO3-ΓΘ
»τΗΟ»ή“ΚΡή”κAlΖ¥”ΠΖ≈≥ωH2ΓΘ»Γ»ΐ÷ß ‘ΙήΘ§ΕΦΦ”»κ…ΌΝΩΖ¥”ΠΚσΒΡ»ή“ΚΓΘ
ΔΌ“Μ÷ßΒΈΦ”“ΜΕ®ΝΩΒΡKOH»ή“ΚΘ§”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΓΘ
ΔΎ“Μ÷ßΒΈΦ”œΓΝρΥαΘ§ΟΜ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΓΘ
Δέ“Μ÷ßΒΈΦ”œθΥα“χ»ή“ΚΘ§”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΓΘ
‘ρ(1)ΗΟ»ή“Κ÷–Έό¥σΝΩΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ άκΉ”ΓΘ
(2)ΗΟ»ή“Κ÷–”–ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ άκΉ”ΓΘ
ΓΓ (3)…ζ≥…ΑΉ…Ϊ≥ΝΒμΒΡάκΉ”ΖΫ≥Χ ΫΈΣ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
2Θ°ΥαΙΐΕύ «≥ΘΦϊΒΡΈΗ≤ΓΓΘœ¬Οφ «ΦΉΓΔ““ΝΫ÷÷≥ΘΦϊΈΗ“©ΒΡΥΒΟς’Σ“ΣΓΘ
ΦΉΘΚ(1)ΑΉ…ΪΫαΨßΉ¥ΖέΡ©Θ§Ω…ΜΚΜΚΖ÷ΫβΘΜ(2)Ρή»ή”ΎΥ°Θ§Υ°»ή“Κ≥ »θΦν–‘ΘΜ(3)”ωΥαΦΑΥα–‘“©Έο‘ρ≤ζ…ζΕΰ―θΜ·ΧΦΘΜ(4)ΈΗΥαΙΐΕύΜΦ’ΏΖΰ”ΟΕύΦϊΈΗ’ΆΤχΘ§…θ÷Ν”–“ΐΤπΈΗάΘ―ώ¥©ΩΉΒΡΈΘœ’ΓΘ
““ΘΚ(1)”κΈΗΥα «÷–ΚΆΉς”ΟΜΚ¬ΐΕχ≥÷ΨΟΘ§Ω…Έ§≥÷3-4–Γ ±ΓΘ(2)ΡΐΫΚ±Ψ…μΗ≤Η«”ΎάΘ―ώΟφ…œΘ§ΨΏ”–±ΘΜΛΉς”ΟΓΘ(3)Ω…»ή”ΎœΓΥαΜρ«β―θΜ·ΡΤ»ή“Κ÷–ΓΘ
(1)«κΡψΆΤ≤βΘ§ΦΉ÷–Κ§”–ΒΡ÷ς“ΣΜ·―ß≥…Ζί «ΓΓΓΓΓΓΓΓΓΓΓΓ (ΧνΜ·―ß Ϋ)ΘΜ““÷–Κ§”–ΒΡ÷ς“ΣΜ·―ß≥…Ζί «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΧνΜ·―ß Ϋ)ΓΘ
(2) ‘–¥≥ωΦΉ÷–Κ§”–ΒΡ÷ς“ΣΜ·―ß≥…Ζί“ΐΤπΈΗ’ΆΤχΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3) ‘–¥≥ω““÷–Κ§”–ΒΡ÷ς“ΣΜ·―ß≥…ΖίΖ÷±π”κœΓ―ΈΥαΚΆ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
24Θ°(8Ζ÷)≥Τ»Γ0.200gΡ≥≥ύΧζΩσ―υΤΖΘ§Ωσ―υ»ήΫβΚσΘ§ ΙΤδ÷–ΒΡΧζ»Ϊ≤ΩΉΣΜ·≥…Fe2+(ΥυΒΟ»ή“Κ÷–≤ΜΚ§ΤδΥϋΜΙ‘≠–‘Έο÷ )ΓΘΝμ≥Τ»Γ7.90gΝρΥανφοß2(NH4)2SO4.Ce(SO4)2.2H2O(ΡΠΕϊ÷ ΝΩΈΣ632gΓΛmolΘ≠1)Θ§»ήΫβΚσœΓ Ά÷Ν250mlΓΘ»ΓΗΟ»ή“Κ30ml«ΓΚΟ”κ…œ ωFe2+»ή“ΚΆξ»ΪΖ¥”ΠΘ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣCe4++Fe2+=Ce3++Fe3+ΓΘ«κΦΤΥψΗΟΩσ―υ÷–Fe2O3
ΒΡ÷ ΝΩΖ÷ ΐ(Fe2O3ΒΡΡΠΕϊ÷ ΝΩΈΣ160gΓΛmolΘ≠1)ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com