
题目列表(包括答案和解析)
13.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答:
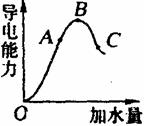 (1)“O”点导电能力为“0”的理由是_______________________。
(1)“O”点导电能力为“0”的理由是_______________________。
(2)A、B、C三点pH值由大到小的顺序是_______________________。
(3)A、B、C三点电离程度最大的是____________________
12.在一定温度下,有a盐酸,b硫酸,c醋酸,三种酸:
(1)当三种酸物质的量浓度相等时,c(H+)由大到小的顺序是
(2)若三者c(H+)相同,物质的量浓度由大到小的顺序是
(3)将c(H+)相同的三种酸均加水稀释至原来的100倍,c(H+)由大到小的顺序是
10. 在含有酚酞的0.1 mol/L氨水中加入少量的NH4Cl晶体,则溶液颜色
A.变蓝色 B.变深 C.变浅 D.不变
11 将0.1mol·L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起
A.溶液的pH增加 B.促进CH3COOH的电离
C.溶液的导电能力减弱 D.溶液中c(OH-)减少
9. 在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:
CH3COOH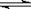 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
8. 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是
A.通入二氧化碳气体 B.加入氢氧化钠固体
C.通入氯化氢气体 D.加入饱和石灰水溶液
7.一定量的盐酸与过量的锌粉反应时,为了减缓反应速率,但不影响生成H2的总量,可向盐酸中加入适量的 ( )
A、NaOH(固) B、H2O C、NaCl(固) D、CH3COONa(固)
5. 下列物质中,最难电离出氢离子的是( )
A.CH3COOH B. NaHCO3 C. H3PO4. D.H2SO4
6 下列事实一定能说明HNO2是弱电解质的是( )
①常温下 NaNO2溶液的 pH > 7;②用 HNO2溶液做导电实验灯泡较暗;③0.1mol/L 的 HNO2溶液的 pH 为 2.1;④用0.1mol/L的 HCl与0.1mol/L的HNO2与同浓度的NaOH 溶液恰好反应,消耗NaOH 溶液体积相同
A.①② B.①③ C.②③ D.③④
4. 在相同温度时100mL0.01mol/L的醋酸溶液与10mL0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
A.中和时所需NaOH的量 B.电离度
C.H+的物质的量 D.CH3COOH的物质的量
3.下列说法正确的是( )
A.氯化钾溶液在电流作用下电离成钾离子和氯离子
B.二氧化硫溶于水能部分转化成离子,故二氧化硫属于弱电解质
C.硫酸钡难溶于水,所以硫酸钡属弱电解质
D .纯净的强电解质在液态时,有的导电有的不导电
2.在RNH2·H2O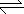 RNH
RNH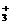 +OH-形成的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
+OH-形成的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
A.通入HCl B.加少量NaOH固体 C.加水 D.升温
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com