
题目列表(包括答案和解析)
5.下列属于分离、提纯固态有机物的操作的是
A.蒸馏 B.萃取 C.重结晶 D.分液
4.A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是
A.A和B一定是同分异构体 B.A和B不可能是同系物
C.A和B最简式一定相同 D.A和B的化学性质相似
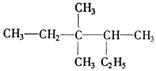
3.有机物 的正确命名为
A.2-乙基-3,3-二甲基-4-乙基戊烷 B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基已烷 D.2,3,3-三甲基已烷
2. 2008年九月我国发现三鹿、蒙牛等品牌婴幼儿奶粉受污染事件,
2008年九月我国发现三鹿、蒙牛等品牌婴幼儿奶粉受污染事件,
导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中
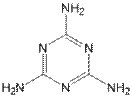
含有一种叫三聚氰胺的物质,它的分子式为C3N6H6(结构如图),
是一种白色无味的单斜棱晶体。下列有关三聚氰胺的说法不正确的是:
A.它是一种含氮的有机化合物
B.它的相对分子质量为126g/mol
C.它易溶于苯、四氯化碳等有机溶剂
 D.三聚氰胺不是芳香族化合物
D.三聚氰胺不是芳香族化合物
1.目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确是
A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B.碳原子性质活泼,可以跟多数元素原子形成共价键
C.碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键
D.多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合
6.(10分)联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
(1)已知:2NO2(g)===N2O4(g)
△H=-57.20kJ·mol-1。一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是 (填字母)。
N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是 (填字母)。
A.减小NO2的浓度 B.降低温度
C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H= kJ·mol-1。K^S*
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol·L-1、c(N2O4)=0.0120 mol·L-1。计算反应2NO2(g) N2O4(g)的平衡常数K。
N2O4(g)的平衡常数K。
(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2H4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
2009-2010学年(下)厦门理工学院附中
5.人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
A.CO与HbO2反应的平衡常数K=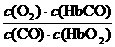
B.人体吸入的CO越多,与血红蛋白结合的O2越少
C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
4.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的( )
A.物质的量之比为3︰2 B.质量之比为3︰2
C.摩尔质量之比为2︰3 D.反应速率之比为2︰3
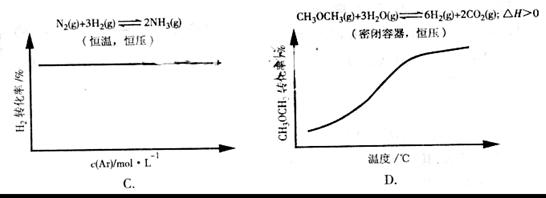
3.各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
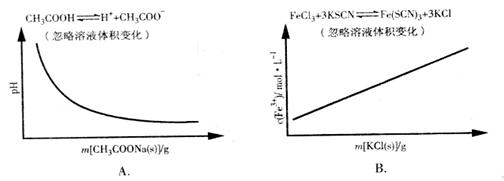
2.在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
|
物质 |
X |
Y |
Z |
|
初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
|
平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
下列说法错误的是:( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com