
题目列表(包括答案和解析)
12、已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A、X与Y形成化合物时,X可以显负价,Y显正价
B、在元素同周期表中X可能位于Y的右面
C、最高价含氧酸的酸性:X对应的酸性弱于于Y对应的酸性
D、Y的气态氢化物的稳定性小于X的气态氢化物的稳定性
11. 对充有氖气的霓红灯管通电,灯管发出红色光。产生这一现象的主要原因( )
A.电子由激发态向基态跃迁时以光的形式释放能量
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.在电流作用下,氖原子与构成灯管的物质反应
10.根据键能数据估算CH4 (g)+4F2 (g) =CF4 (g) +4HF(g)的反应热ΔH为( )
|
化学键 |
C-H |
C-F |
H-F |
F-F |
键能/(kJ·mol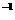 ) ) |
414 |
489 |
565 |
155[来] |
A.–1940 kJ · mol-1 B.1940 kJ · mol-1
C.–485 kJ · mol-1 D.485 kJ · mol-1
9. 用价层电子对互斥理论(VSEPR)预测H2S和COCl2的立体结构,两个结论都正确的是( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
8. 下列说法中错误的是( )
A.根据对角线规则,铍和铝的性质具有相似性
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.P4和CH4都是正四面体分子且键角都为109o28ˊ
7. 某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后两面面心中的B元素的原子未能画出)。晶体中A、B、C的原子个数比为 ( )
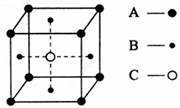 A.1∶3∶1 B.2∶3∶1
A.1∶3∶1 B.2∶3∶1
C.2∶2∶1 D.1∶3∶3
6.下列说法错误的是( ) A.s轨道呈圆形,p轨道呈哑铃形
B.Cu元素在元素周期表的ds区
C.1.5g CH3+中含有的电子数为0.8NA
D.DNA中的碱基互补配对是通过氢键来实现的
5.已知X、Y是主族元素,I为电离能,单位是KJ/mol。根据下表所列数据判断错误的是( )
|
元素 |
I1 |
I2 |
I3 |
I4 |
|
X |
496 |
4562 |
6912 |
9543 |
|
Y |
578 |
1817[来源 |
2745 |
11600 |
A.元素X的常见化合价是+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
4.下列无机含氧酸的酸性强弱比较正确的是( )
A.HNO2>HNO3 B.HNO3>H3PO4 C.HClO>HClO2 D.H2CO3>HNO3
3.下列叙述中正确的是( )
A.分子晶体的熔点和沸点都很高
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、Hl的稳定性依次增强
D.H2O是一种非常稳定的化合物,这是由于氢键所致
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com