
题目列表(包括答案和解析)
1.化学与人类生产和生活密切相关。下列说法不正确的是w_w w.k_s_5*
A.苯酚有一定毒性,但它的稀溶液可直接用作消毒剂和防腐剂
 B.蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物
B.蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物
C. 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分
D.改液化石油气为天然气作燃料,燃烧时应减小进空气量或增大进天然气量
24.(13分)A、Z、R、D、E、F、G是七种原子序数依次增大且不大于20的元素,其中有两种非金属元素位于同一主族。已知A、Z、D均能与R形成原子(或离子)个数不同的几种常见化合物。请回答下列有关问题。

 w_w w. k#s5_
w_w w. k#s5_
(1)X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14。X、Y的晶体熔点相对高低为(写化学式) ,导致这种差异存在的原因____________________________________在相同温度下,等物质的量的X、Y的溶液中,由水电离出的c(H+)的相对大小关系为 。w_w*w.k_s_5_
(2)A与Z、E均可形成正四面体构型的气态分子Q、P, 其稳定性Q____P(>,<,=),工业上用Z制备E的反应方程式为________________________________。一定条件下Z、E生成的化合物为_______晶体,Z的一种单质具有导电性,则该单质的晶体中最小环为______元环,1molZ原子形成的该单质晶体中上述环有____________个。
(3)上述七种元素间能形成多种常见二元化合物,其中Z与G形成的一种化合物存在两类化学键,该物质溶于稀HCl溶液的化学反应方程式为
。ZR2的结构式为
,R、D形成的化合物具有漂白性,该化合物的电子式为__________________
。

 w_w w. k#s5_
w_w w. k#s5_
(4)R能形成多种单质,如R2、R3等。据报道,最近科学家制得了一种组成为R4的分子,每个R原子均与另外两个R原子各形成一个键,则1mol R4中共用电子对数为 NA,下列有关R4的说法正确的是 。(填编号)w_w*w.k_s_5_
①R4与R2、R3互为同位素 ②R4不能与A、Z、D的单质反应
③R4中各原子最外电子层均为8电子结构 ④R4固体属于分子晶体


 w_w w. k#s5_
w_w w. k#s5_
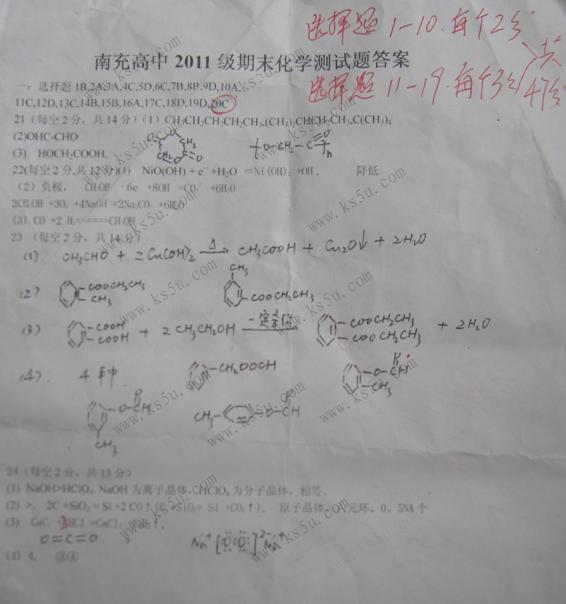
23. (14分)芳香族化合物B、C、F与链状有机物A、D、E、G间的变化关系如下图所示。B中苯环上的一溴代物有四种,D可发生银镜反应,C、G属同类有机物。以下变化中,某些反应条件及产物未标明。
(14分)芳香族化合物B、C、F与链状有机物A、D、E、G间的变化关系如下图所示。B中苯环上的一溴代物有四种,D可发生银镜反应,C、G属同类有机物。以下变化中,某些反应条件及产物未标明。

 w_w w. k#s5_
w_w w. k#s5_
(1)D与新制Cu(OH)2悬浊液反应的化学方程式: 。
(2)写出有机物C可能的结构简式
____________________________________________________________________________。
(3)一定条件下,F与足量的A发生反应的化学方程式:
。(只写一例)
(4)同时符合下列条件的B的同分异构体有 种,写出其中任意两种的结构简式;
; 。
a.分子中含有苯环 b.能发生水解反应 c.能发生银镜反应
22.(12分)(1)混合动力汽车因具有能量利用率高(95%以上)、节省汽油、发动机噪音低和几乎没有尾气污染等优良性能,受到越来越多的关注,某种混合动力汽车的动力系统由“1.3L汽油机+5速手动变速器+10kw电机+144v镍氢电池”组成。 ①镍氢电池的使用可减少重金属离子污染,其采用储氢金属作为负极,碱液(主要是KOH)作为电解液,镍氢电池做原电池时发生反应: NiO(OH)+1/2 H2= Ni(OH)2

 w_w w. k#s5_
w_w w. k#s5_
其放电时的正极电极反应式为 。
负极区PH值 (升高、降低、不变)。w_w*w.k_s_5_
②某电池采用的原料为:甲醇、空气、氢氧化钠溶液,通甲醇的一极为________极,其电极反应方程式为 ,该原电池的总反应方程式为___________________________________________ .
③甲醇可通过煤的汽化 产生的CO、H2 在一定条件下制得,其反应方程式为_______________________________________。
21.(11分)今有相对分子质量为M的有机物,燃烧后只生成CO2 和H2O。
①若有机物是M = 72的烃,请写出所有可能的结构简式: 、
、 。
②若M = 58,且1mol该有机物与足量的银氨溶液作用,可析出4mol Ag,其结构简式为_ 。
③若A的M=76,既能与酸又能与醇发生酯化反应,则A的结构简式为________________,A在一定条件下可形成六元环状结构的分子或高分子化合物,则二者的结构简式分别为
,_____________________________。
20.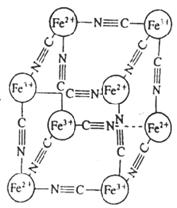 分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上。其晶体中的阴离子晶胞结构如图示,下列说法正确的是
分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上。其晶体中的阴离子晶胞结构如图示,下列说法正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.该晶体中含有极性共价键,是原子晶体w_w*w.k_s_5_
B.M的离子位于上述晶胞面心,呈+2价
C.晶体的化学式可表示为MFe2(CN)6,且M为+1价
D.M的离子位于上述晶胞体心,呈+2价

 第Ⅱ卷(非选择题,共50分)
第Ⅱ卷(非选择题,共50分)
19.将2.1g Mg和Al的混合物投入足量盐酸中,产生标况下的H2 2.24 L,然后加入1 mol/L NaOH 溶液反应后,过滤、洗涤、干燥后固体的质量(不考虑固体因分解失重)不可能为
A.3.0 g B.3.5 g C.5.5 g D.5.6 g
18.与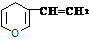 互为同分异构体的芳香族化合物有
互为同分异构体的芳香族化合物有

 w_w w. k#s5_
w_w w. k#s5_
A.2种 B.3种 C.4种 D.5种
17.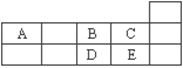 右表为元素周期表短周期的一部分。下列有关A、B、 C、
D、E五种元素的叙述中,不正确的是
右表为元素周期表短周期的一部分。下列有关A、B、 C、
D、E五种元素的叙述中,不正确的是
A.A与B形成的阴离子可能有:AB32-、A2B42-
B.五种元素形成的气态氢化物中,C的氢化物最稳定
C.D的氢化物在过量的B中燃烧的主要产物为DB3
D.由这5种元素中的几种形成的只含极性键的非极性分子多于3种
16.150℃、101K
Pa 时,由两种烃组成的混合气体0.5L在4.5L O2 中完全燃烧,测得反应后气体总体积小于5L,其中含CO2
0.8L,则生成水蒸气的体积为

 w_w w. k#s5_
w_w w. k#s5_
A.0.7L B.1.4L C.1.6L D.2.8L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com