
题目列表(包括答案和解析)
9.下面的排序不正确的是 ( )
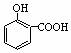
A.晶体熔点的高低: 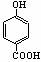 >
>
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小: NaF> NaCl> NaBr>NaI
8.下列说法正确是 ( )
①所有基态原子核外电子排布都遵循构造原理
②同一周期从左到右,元素第一电离能、电负性都是越来越大
③所有化学键和氢键都具有相同特征:方向性和饱和性
④所有配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极性键的分子都是极性分子
⑥所有离子晶体中都含有离子键
⑦所有金属晶体熔点肯定高于分子晶体
A.①② B.⑥ C.③④⑤ D.①②⑥
7.下列分子或离子中键角由大到小排列顺序是 ( )
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2
A.⑤④①②③ B.⑤①④②③ C.④①②⑤③ D.③②④①⑤
6.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是 ( )
A.S和Si B.CCl4和KCl C.NaCl和HCl D.CO2和H2O
5.下列式子中,真实表示物质分子组成的是 ( )
A.H2O B.NH4Cl C.SiO2 D.C
4.根据等电子原理,等电子体之间结构相似、物理性质也相近。以下各组粒子不能互称为等电子体的是( )
A.CO和N2 B.O3和SO2
C.CO2和N2O D.N2H4 和C2H4
3.下列性质中,可以较充分说明某晶体是离子晶体的是 ( )
A. 具有较高的熔点 B. 固态不导电,水溶液能导电
C. 固态不导电,熔融状态能导电 D.可溶于水
2.金属的下列性质中,不能用金属的电子气理论加以解释的是 ( )
A.易导电 B.易导热 C.有延展性 D.易锈蚀
1.以下能级符号正确的是 ( )
A.6s B.2d C.3f D.2f
25.(11分)A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
|
阳离子 |
Ag+ Na+ |
|
阴离子 |
NO3- SO42- Cl- |
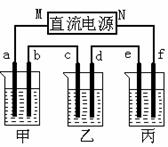
 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。
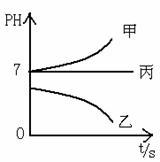
接通电源,经过一段时间后,测得乙中C电极质量增加了27克。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的_______极(填写“正”或“负”),甲、乙电解质分别为_______、_______(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积_____________。
(3)写出乙烧杯的电解池总反应_____________________________。
(4)若电解后甲溶液的体积为25L,则该溶液的pH为___________ 。
(5)要使丙恢复到原来的状态,应加入 g 。(填写化学式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com