
题目列表(包括答案和解析)
22.在三个烧杯中分别盛有等体积、浓度均为0.1mol/L的(1)KCl(2)AgNO3(3)K2SO4溶液,用铂电极与导线将三只烧杯装成串联电路,并通入直流电。一段时间后,若(1)杯的阴极析出气体的体积在标准状况下为0.448L时,则(2)杯的阴极产物是______,质量是______g;(3)杯的阳极产物是______,其物质的量是______mol。
21.含Cr2O72-的工业酸性废水会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转变为Cr(OH)3除去。工业上采取的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH不断升高,溶液由酸性转为碱性。在以上处理过程中,溶液pH升高的原因是 [ ]
A.电解时废水体积减小
B.鼓入空气使溶液中OH-浓度增大
C.电解时H+在阴极被还原
D.Cr2O72-被还原为Cr3+时消耗了H+
20.向电解质溶液中插入M,N电极,并连接直流电源进行电解,可以看到两电极上均有气泡产生。电解后测定电解液,其中溶液中的H+浓度无变化。符合这些条件的是 [ ]
A.两个电极均为铁片,M是阴极,电解液是0.4%的NaOH溶液
B.两个电极均为石墨,M是阳极,电解液是0.4%的H2SO4溶液
C.两个电极均为石墨,M是阳极,电解液是0.4%的KOH溶液
D.M是铁片、N为石墨,M是阴极,电解液是0.4%的KNO3溶液
19.用质量均为100g的Cu作电极,电解AgNO3溶液。电解一段时间后,两电极的质量相差28g,此时两电极的质量分别为 [ ]
A.阳极93.6g,阴极121.6g
B.阳极100g,阴极128g
C.阳极91.0g,阴极119.0g
D.阳极86.0g,阴极114.0g
18.在盛有饱和Na2CO3溶液的烧杯中插入惰性电极进行电解,若温度始终不变,则通电一段时间后 [ ]
A.溶液的pH增大
B.溶液中水分子数与碳酸根离子的比值将变小
C.溶液中将有晶体析出
D.溶液中Na+数目将减小
17.用惰性电极电解下列各组中的3种电解质溶液,在电解过程中溶液pH依次为升高、降低、不变的组是 [ ]
A.AgNO3,CuCl2,Cu(NO3)2
B.CaCl2,KOH,NaNO3
C.KBr,CuSO4,Na2SO4
D.HCl,HNO3,K2SO4
16.用石墨电极电解硝酸银溶液,在阳极收集到0.40g氧气,中和电解时生成的酸需要250mL氢氧化钠溶液,则氢氧化钠溶液的物质的量浓度是 [ ]
A.0.05mol/L B.0.10mol/L C.0.15mol/L D.0.20mol/L
15.将含0.4molCuSO4和0.4molNaCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol铜,在另一个电极上析出气体在标准状况下的体积是______(不考虑生成的气体在水中的溶解) [ ]
A.5.6L B.6.72L
C.13.44L D.11.2L
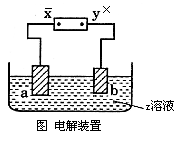
14.图中x,y分别为直流电源的两极,通电后发现a极板质量增加,b极处有无色无臭气体放出,符合这一情况的是 [ ]

13.电解84.7mL16%的NaOH溶液(密度为1.18g/cm3)过了一段时间,电解后溶液中溶质的质量分数为19.5%(用石墨作电极),这是因为 [ ]
A.溶质增加3.5g
B.有1mol水被电解
C.在阳极生成2gH2
D.在阳极生成了16gO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com