
题目列表(包括答案和解析)
3.现有以下几种措施:①对煤燃烧时产生的尾气进行除硫处理②少用原煤作燃料 ③燃煤时鼓入足量空气④开发清洁能源。其中能减少酸雨产生的措施是
A.①②③ B.②③④ C.①③④ D.①②④
2.油井发生火灾,产生大量废气,包括:(1)浓烟中的炭粒;(2)氮的氧化物;(3)碳的氧化物;(4)硫的氧化物;(5)碳氢化合物及其氧化物的蒸气。其中对大气造成污染并导致雨水酸化的有害气体是
A.(1)(3)(5) B.(2)(4) C.(2)(3)(4) D.(2)(4)(5)
1.查阅资料发现,金属钠不仅能跟氧气和水反应.还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同点, 下列的研究方法中没有用到的是
A.实验法 B.观察法 C.分类法 D.比较法
29.如下图所示,甲、乙装置中电极均为惰性电极。将8.88g硝酸盐晶体M(NO3)m·nH2O(相对分子质量296)溶于水配成600mL溶液,将此溶液装入甲池中,在乙池中装入稀H2SO4溶液,通电进行电解,当乙池中的A电极上产生336mL(标准状况)气体时,甲池中溶液中金属离子全部析出,停止通电。称量后,阴极增重1.92g。求(1)金属M的相对原子质量以及m和n值。(2)电解后甲池溶液的pH(假设电解前后甲池中溶液的体积不变)。
28.有一硝酸盐晶体,化学式为M(NO3)x·nH2O,经测定其摩质量为242g/mol,取1.21g此晶体溶于水,配制成100mL溶液,将其置于电解池中用惰性材料为电极进行电解,当有0.01mol电子通过电极时,溶液中全部金属离子即在电极上析出、经测定、阴极增重0.32g,①问1.21g此盐晶体是几摩?x值是多少?②求M的相对原子质量和n值。③如电解过程中,溶液体积不变,计算电解结束后溶液的pH。
27.在Rn(XO4)m(m≠n)溶液中插入两个惰性电极,通电一段时间后,测得溶液的酸性增强,且阴极有R的金属单质析出。写出电解反应的化学方程式:______。
26.在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,如下图:
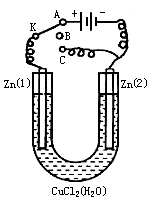
(1)如果把电键K接A,那么A是______装置,Zn①极是______极,电极附近的现象______,电极反应式是______;Zn②极是______极,电极反应式是______。
(2)上述反应进行5min后,转换电键K到C,这一装置形成______,Zn①极是______极,电极反应式是______;Zn②极是______极,电极反应式是______,电流的方向是从______极流向______极。
(3)上述装置进行2min后,再转换电键K到B,在Zn②极发生的化学反应是______,Zn①极发生的有关反应是______。
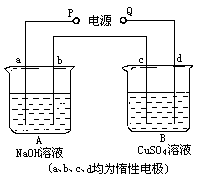
25.按下图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液,通电一段时间后,c极上有Cu析出,又测得A杯中NaOH溶液浓度为10.23%,试回答:①电源P为______极,②b极产生气体的体积为______L(标准状况),③c极上析出沉淀的质量为______g,④d极上所发生的电极反应式_______。(a、b、c、d均为惰性电极)
24.电解精炼铜时以含有少量锌、银、金、镍(Ni)等杂质的粗铜作为阳极,以纯铜片作为阴极,以CuSO4溶液为电解液,进行电解。回答下列问题:
(1)阴极发生反应的电极方程式为:______;阳极发生反应的电极方程式为:______。
(2)通电一段时间后切断电源,测得阴极增重3.2kg,则导线上通过的电子物质的量为______mol,CuSO4溶液的pH是否发生改变?______。
23.用铂电极电解下列溶液一段时间后,停止电解,分别取出所有溶液,加入一种物质使其恢复成原浓度的溶液,所加入的物质分别为:H2SO4______,CuCl2______,CuSO4______,KCl______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com