
题目列表(包括答案和解析)
21.( 10分) 将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。
 问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
|
序号 |
实际生产中采取的措施 |
工业生产实例(写名称) |
|
(1) |
通过增大压强提高原料转化率 |
|
|
(2) |
使用催化剂增大反应的速率 |
|
问题3:化学反应中均伴随着能量的变化。如果一个化学
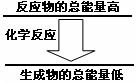 反应中,反应物的总能量和生成物的总能量有如图所示的
反应中,反应物的总能量和生成物的总能量有如图所示的
关系,则该反应过程中的能量变化是 。
已知热化学方程式为:
C(g) + O2(g)= CO2 (g) △H= -393.5KJ/mol
H2 (g) + 1/2O2 (g)= H2O (l) △H= -285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 (保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。如:4Na+O2=2Na2O 2Na+O2 Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
反应的原理不同: 。
20.(8分)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子间距离相同。
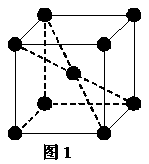
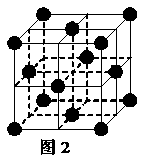
(1)在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为_______个;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为___________;
(2)纯铁晶体在晶型转变前后,二者基本结构单元的边长之比为(1183 K以下与1183 K以上之比)___________。
(3)转变温度前后两者的密度比(1183 K以下与1183 K以上之比)____。
19.(8分)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol。某同学用22g液化气(以C3H8计)做实验,测定燃烧放出热量有关数据如下:
①完全燃烧生成CO2和H2O(g)时,放出热量a kJ ;
②不完全燃烧生成CO和H2O(g)时,放出热量b kJ;
③不完全燃烧生成CO、CO2和H2O(g)时,放出热量 c kJ ;
请写出(1)能表示液化气燃烧热的热化学方程式:
(2)CO的燃烧热为 :
(3)第③次实验生成CO的物质的量为 :
18. (13分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
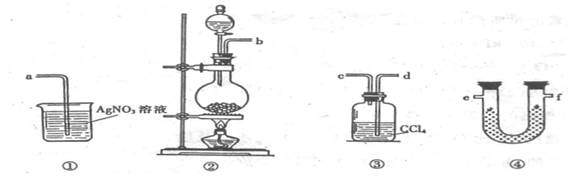
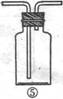 ⑴请根据甲同学的意图,连接相应的装置,接口顺序:
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接 , 接 , 接a。
⑵U形管中所盛试剂的化学式为 。
⑶装置③中CCl4的作用是 。
⑷乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在 之间(填装置序号),瓶中可以放入 。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成 ,如果观察到
______________________________的现象,则证明制Cl2时有HCl挥发出来。
(6)乙同学把生成的氯气能通入湿润的红色布条中,发现红色褪去。对于使红色布条褪色的物质,乙同学认为氯水中存在的几种粒子都有可能。请你设计实验证明并非氯气的强氧化性或盐酸的酸性在起此作用(请简要叙述实验步骤):
17.(9分)⑴指出下列实验用品或仪器(已洗涤干净)使用时的第一步操作:
①石蕊试纸(检验气体性质)
②容量瓶
⑵下列实验中所选用的仪器或结论不合理的是 (填字母,多选扣分)
A.用托盘天平称量重11.7g氯化钠晶体
B.用碱式滴定管量取25.00mL溴水
C.不宜用瓷坩埚灼烧氢氧化钠、碳酸钠
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
E.用酸式滴定管量取浓硫酸配制一定浓度的稀硫酸时,某同学取前平视,取后俯视,所配硫酸的浓度偏高。
F. 把水滴加到脱脂棉包住的过氧化钠粉末上,脱脂棉可以燃烧,说明该反应为放热反应。
(3)某含结晶水的无色透明晶体,可能是明矾或草酸晶体,为确定其成分,某校化学兴趣小组的同学设计了几种方法:①检验K+;②溶于水检验Al3+;③溶于水利用胶体性质进行检验;④溶于水用石蕊试液检验;⑤与浓硫酸混合共热,将产生的气体用澄清石灰水检验;⑥溶于水再用酸化的高锰酸钾溶液检验。你认为其中的操作步骤没有必要的是________________(填序号,多选扣分)
16.把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示:
|
物 质 |
A |
B |
C |
D |
|
反应前质量/g |
19.7 |
8.7 |
21.6 |
0.4 |
|
反应后质量/g |
待测 |
17.4 |
0 |
3.6 |
下列说法正确的是( )
A、物质C一定是化合物,物质B可能是单质
B、反应后密闭容器中A的质量为19.7g
C、反应过程中,物质B和物质D变化的质量比为87∶36
D、若物质A与物质C的相对分子质量之比为194∶216,则反应中A和C的物质的量之比为1∶2
15.一定温度时有摩尔质量为Mg/mol的某溶质R的溶液,当加入Ag不含结晶水的R或蒸发掉Bg水,恢复到原温度时溶液均达饱和,下列说法不正确的是:
A.该温度下R的饱和溶液质量分数是A/(A+B)%
B.该温度下若R的饱和溶液物质的量浓度为Cmol/L,则溶液密度为(A+B)CM/1000B g/mL
C.R在该温度下的溶解度为100A/Bg
D.若原溶液质量分数为50A/(A+B)%,则原溶液质量为2Bg。
14.下列反应的离子方程式正确的是
A.碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O
B.向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
C.1 mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:
2AlO2-+5H+ = Al(OH)3↓+Al3++H2O
D.向硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H++H2O2=Fe3++2H2O
13.NA代表阿伏加德罗常数的值,下列说法正确的是
A.含有1 mol P的白磷晶体中,含有的P-P键的数目为1.5 NA
B.含有1 mol硅原子的二氧化硅晶体中,Si-O共价键数为2 NA
C.8.0 g Cu2S和CuO的混合物中约含有铜原子数为0.1NA
D.常温常压下,0.1mol铁与0.1molCl2充分反应,转移的电子数约为0.3NA
12.某溶液可能含有Na+、Ag+、Al3+、AlO2―、S2-、CO32-、SO32―、NO3-等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色。根据以上实验现象,下列结论中不正确的是( )
A.此溶液中一定有S2-、SO32―、Na+ B.此溶液中可能有AlO2―、CO32-
C.此溶液中一定没有Ag+、Al3+ D.此溶液中可能有S2-和NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com