
题目列表(包括答案和解析)
27.(8分)中国是《日内瓦协定书》的缔约国,一贯反对使用化学武器,反对任何形式的化学武器扩散。苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式为: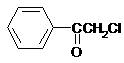 ,试回答下列问题:
,试回答下列问题:
(1)苯氯乙酮分子中,在同一平面上的碳原子最多有 个。
(2)苯氯乙酮不可能具有的化学性质是:_____________(填序号)。
A.加成反应 B.取代反应 C.消去反应 D.水解反应 E.银镜反应
(3)与苯氯乙酮互为同分异构体,且能发生银镜反应,分子有苯环但不含-CH3的化合物有多种,它们的结构简式是:
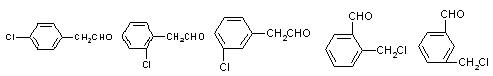
请写出与上述不同的两种同分异构体: ; 。
26.(10分)在标准状况下,取甲、乙、丙各30.0 mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不发生变化)。
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
255 |
385 |
459 |
|
气体体积/ mL |
280 |
336 |
336 |
请回答:
(1)甲组实验中,盐酸(选填“适量”“过量”或“不足量”,下同)________________;乙组实验中盐酸 ________________。
(2)盐酸的物质的量浓度为________________。
(3)合金中Mg、Al的物质的量之比为________________。
25.(12分)物质A是化合物,B、C、D、K都是单质,反应②-⑤都是常见的工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
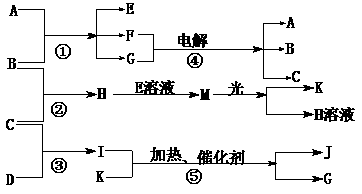
请填写下列空白:
(1)写出下列物质的化学式:B ; C ; D ;
K ;G ;J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。
②I溶于G 。
24.(14分)A、B、C、D是化学中常见的单质,其中A是用量最大、应用最广泛的金属,D是地壳中含量最多的金属元素,甲、乙、丙为化合物,其中甲为黑色晶体,乙在常温常压下为无色无味的液体。它们之间存在如图所示的转化关系,由此可推知:
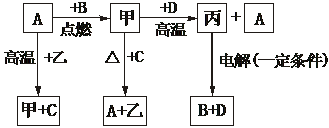
(1)元素A在周期表中的位置为___________。
(2)乙的电子式为___________。
(3)写出甲和D反应的化学方程式(注明条件)________________________,在此反应中生成1 mol A转移电子的物质的量为___________mol。
(4)已知D能与烧碱溶液反应,写出D与烧碱溶液反应的离子方程式:_____________。
(5)元素A的某种化合物常用于净水,请用离子方程式表示其净化原理____________。
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
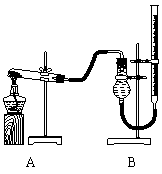 用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3质量 |
其它物质质量 |
待测数据 |
|
④ |
1.2 g |
无其他物质 |
|
|
⑤ |
1.2 g |
CuO 0.5 g |
|
|
⑥ |
1.2 g |
MnO2 0.5 g |
|
回答下列问题:
⑶上述实验中的“待测数据”指_____________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,__________________________________________
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a._______________________________;
b.CuO的化学性质有没有改变。
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
⑴上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤①、③中研磨固体所用仪器的名称是___________________;
⑵步骤③中洗涤沉淀的操作是_____________________________________________
21(4分)下列实验操作正确的是___________。
A.为了加快过滤速率,可用玻璃棒搅拌过滤器中液体
B.苯酚沾在手上,马上用酒精洗涤
C.皮肤上沾有浓H2SO4,立刻用大量水冲洗
D.从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶
E.在中和滴定的实验过程中,目光应注视滴定管中的液面
F.用25 mL碱式滴定管量出14.80 mL的Na2CO3溶液
G.用托盘天平称量出25.20 g NaCl晶体
H.酒精灯在桌上失火,立即用湿布盖上熄灭
I.用加热蒸发FeCl3溶液的方法制取无水FeCl3
J.用蒸馏的方法分离苯和溴苯的混合物
22.(8分)现有下列仪器或用品:①铁架台(含铁圈、各种铁夹) ②锥形瓶③酸式滴定管与碱式滴定管 ④烧杯 ⑤玻璃棒 ⑥胶头滴管 ⑦天平(含砝码、镊子) ⑧滤纸 ⑨分液漏斗 ⑩普通漏斗 ?11双孔塞及导管 12药匙
现有下列试剂:碱石灰、标准NaOH溶液、未知浓度盐酸、蒸馏水、Na2CO3固体、MnO2、NH4Cl固体、H2O2溶液
(1)过滤时,应选用的仪器是_________________________________(填编号);
(2)配制500 mL 0.1 mol·L-1的Na2CO3溶液,还缺少的仪器是_________________;
(3)可用来制取的气体是________________(填化学式)。
23.(16分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
20.要求设计实验证明:某种盐的水解是吸热的,有四位同学分别作出如下回答,其中不正确的是( )
A.甲同学:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B.乙同学:用加热的方法可除去 溶液中混有的
溶液中混有的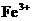 ,说明含
,说明含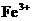 的盐水解是吸热的
的盐水解是吸热的
C.丙同学:通过实验发现同浓度的热的纯碱液比冷的纯碱液去油污效果好,说明碳酸钠水解是吸热的
D.丁同学:在醋酸钠溶液中滴入酚酞试液,加热(不考虑水蒸发)后若红色加深,说明醋酸钠水解是吸热的
第Ⅱ卷(共80分)
19. 下列比较正确的是( )
A.熔沸点高低:CH4 <SiH4 <GeH4<SnH4
B.离子半径大小:Cl-<Mg2+< O2-<F-
C.分散质微粒直径大小:Fe(OH)3胶体>CaCO3沉淀>NaCl溶液
D.酸性强弱:H2SO4> H3PO4> H2SiO3
18.以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是( )
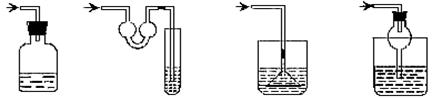
A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com