
题目列表(包括答案和解析)
5、完成化学方程式:(有机物用结构简式表示)
反应② 。
反应③ 。
4、4.4gC物质完全燃烧消耗 mol氧气。
3、反应①的反应类型为 ,反应③的反应类型为 。
2、A的官能团名称 ,B的官能团名称 。
有机物A是烃,有机物B易溶于水,且1molB能与足量的钠反应生成标准状况下的H211.2L,但不与NaHCO3溶液反应。已知A通过如下转化关系(有关反应条件已略去)制得化学式为C4H8O2的酯E,且当D→E时,相对分子质量增加28。
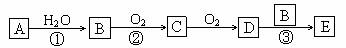
请回答下列问题:
1、A的名称 ,结构简式 ,A在标准状况下的密度为 g/L。
3、已知:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=-akJ/mol;
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=-bkJ/mol
则H2S与SO2两种气体转化为固体硫的热化学方程式为 。
2、在一定温度下的2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(O2)随时间的变化如表:
2SO3(g) △H<0,n(O2)随时间的变化如表:
|
时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(O2)/mol |
0.20 |
0.16 |
0.13 |
0.11 |
0.10 |
0.10 |
(1)用SO2表示0-4min内该反应的平均速率为 。
(2)若升高温度,则SO2的反应速率 (填“变大”、“变小”或“不变”,下同),平衡常数K值 。
(3)下列有关该反应的说法正确的是 (填序号)
A.反应在第4分钟时已达平衡状态。
B.保持容器体积不变,当混合气体的密度不变时,说明反应已达平衡状态。
C.达平衡后,缩小容器的体积,正反应速率变大,逆反应速率变小。
D.通入过量O2,SO2的转化率将增大。
1、短周期元素A、B、C、D原子序数依次增大,A是元素周期表中原子半径最小的元素,A、C同主族,B的最外层电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。
(1)化合物C2B2中含有的化学键类型为 。
(2)化合物CDB是家用消毒剂的主要成分,其水溶液显碱性。显碱性的原因用离子方程式表示为 。
(3)往CD溶液中滴加硝酸银溶液生成白色沉淀后,再滴加碘化钠溶液,可观察到的现象是 。[已知:KSP(AgCl)>KSP(AgI)]
5、MnO2可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,
则其正极的电极反应式为 。
4、实验室用MnO2制取氯气的化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com