
6°¢ÀÆæþ”–∑¥≥£∏þµƒ∑–µ„£¨÷˜“™ «“ÚŒ™∑÷◊”º‰¥Ê‘⁄
A£Æ¿Î◊”º¸°°°° B.π≤º€º¸°°°°°° C£Æ«‚º¸°°°°°° D.–¬–ժؗߺ¸
5°¢œ¬¡–∑÷◊” Ùº´–‘∑÷◊”µƒ «°°°°°°°°°°°°°°°°°°°°°°
A°¢H2O°°°°°°°° B°¢CO2°° °°°°°°°°C°¢BCl3°°°°°°°° D°¢CH4
4°¢œ¬¡–ª˘Ã¨‘≠◊”µƒº€µÁ◊”ππ–Õ÷–£¨’˝»∑µƒ «°°
A£Æ3d94s2°°°° °°B£Æ3d44s2°° °°°°°°C£Æ3d54s24p3°° °°D£Æ4d25s2
3°¢œ¬¡–ƒÐº∂÷–πϵ¿ ˝Œ™3µƒ «
A£ÆSƒÐº∂°° °°B£ÆPƒÐº∂ °°°°°°C£ÆdƒÐº∂°° °°°°D£ÆfƒÐº∂
2°¢œ¬¡–ªØ—ß Ω±Ì æµƒŒÔ÷ ÷–£¨∫¨¿Î◊”º¸≤¢«“∫¨”–º´–‘π≤º€º¸µƒ «
A°¢KCl°°°° B°¢KOH°°°° C°¢H2O°°°° D°¢CaCl2
“ª£Æ—°‘ÒÂ
1°¢œ¬¡–∑÷◊”÷–≤ª∫¨¶–º¸÷ª∫¨¶ƒº¸µƒ «
A°¢HC°‘CH°°°°°° B°¢N°‘N°°°° C°¢CH4 °°°°°°D°¢CO2
38£Æ£®15∑÷£©
”–ª˙ŒÔAŒ™—Ú»‚µƒÃÿ’˜œ„≥…∑÷£¨∆‰∫œ≥…¬∑œþ»Áœ¬£∫
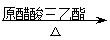
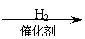
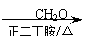 °°
°°
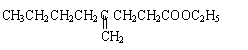 °° B°°°°°°°°°°°°°°
C°°°°°°°°°°°°
D°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°° B°°°°°°°°°°°°°°
C°°°°°°°°°°°°
D°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°
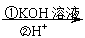
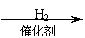 °°
°°
°°°°°°°°°°°°°°°° F°°°°°°°°°°°° A
°°°°°°°°°°°°°°°°°°°°°°°°°°
 °°°°
°°°°
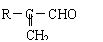 “—÷™£∫¢ŸRCH2CHO£´CH2O°°°°°°°°°°°°°°°°°°°°°°°°
“—÷™£∫¢ŸRCH2CHO£´CH2O°°°°°°°°°°°°°°°°°°°°°°°°
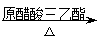 °°°°°°°°°°
°°°°°°°°°°
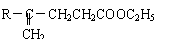
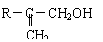 °°°°°°°°°°
¢⁄°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°
¢⁄°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°
°°
£®1£©B «Ã˛µƒ∫¨—ı—Ð…˙ŒÔ£¨÷ ∆◊±Ì√˜Bµƒœý∂‘∑÷◊”÷ ¡øŒ™100£¨∆‰÷–∫¨—ı‘™Àÿµƒ÷ ¡ø∑÷ ˝Œ™16%£¨BƒÐ∑¢…˙“¯æµ∑¥”¶£¨«“∑÷◊”Ω·ππ÷–÷ª”–“ª∏ˆ—CH3°£BµƒΩ·ππºÚ ΩŒ™°°°°°°°°°°°°°°°°°° °£
£®2£©DµƒΩ·ππºÚ ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°° £¨DƒÐ∑¢…˙µƒªØ—ß∑¥”¶¿ý–Õ”–°°°° £®ÃÓ–Ú∫≈£©°£
°°°°°° ¢Ÿı•ªØ∑¥”¶°°°°°°°°°°°°°°°°°° ¢⁄º”≥…∑¥”¶°°°°°°°°°°°°°°°°°° ¢€œ˚»•∑¥”¶°°°°°°°°°°°°°°°°°° ¢Ðæ€∫œ∑¥”¶
°°
£®3£©–¥≥ˆB°˙CµƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°°
£®4£©–¥≥ˆF‘⁄KOH»Ð“∫÷–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
£®5£©»Ù”√œµÕ≥√¸√˚∑®∏¯A√¸√˚£¨Aµƒ√˚≥∆Œ™°°°°°°°°°°°°°°°°°°°° °£
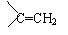 °°
°°
£®6£©”ÎC∫¨”–œýÕ¨πŸƒÐÕ≈£¨∑÷◊”Ω·ππ÷–∫¨”–“ª∏ˆ°°°°°°°° £¨∫À¥≈π≤’Ò«‚∆◊”–3∏ˆ∑£¨«“
°°
∑Â√ʪ˝÷Ʊ»Œ™9£∫2£∫1µƒÕ¨∑÷“ÏππõƒΩ·ππºÚ ΩŒ™°°°°°°°°°°°°°°°° °£
°°
°°
°°
°°
°°
°°
28£Æ£®π≤14∑÷£©
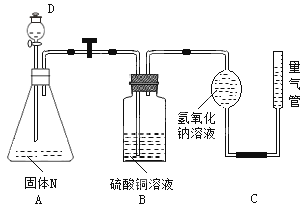
ƒ≥øŒÕ‚–À»§–°◊ÈŒ™¡ÀÃΩæøÃ˙”Ρڑ⁄∏Ùæ¯ø’∆¯µƒÃıº˛œ¬∑¥”¶À˘µ√πÃêÏ∫œŒÔNµƒ≥…∑÷£¨…˺∆¡À»Áœ¬ÕºÀ˘ æ◊∞÷√£∫ µ—Èø™ º ±£¨¥Úø™∑÷“∫¬©∂∑D÷–ªÓ»˚£¨ª∫¬˝º”»Îœ°—ŒÀ·÷¡π˝¡ø£¨¥˝∑¥”¶Õ£÷π∫Û£¨B÷–”–∫⁄…´≥¡µÌŒˆ≥ˆ£¨≤‚µ√Ω¯»Î¡ø∆¯◊∞÷√C÷–µƒ∆¯ÃÂê˝Œ™Vml£®“—ªªÀ„≥…±Í◊º◊¥øˆ£©°££®√øø’2∑÷£¨π≤12∑÷£©
°°
°°
°°
°°
°°
°°
°°
°°
°°
∏˘æð“‘…œ µ—È ¬ µªÿ¥œ¬¡–Œ £∫
£®1£©A÷–ø…ƒÐ∑¢…˙µƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °¢
°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
£®2£©¡ø∆¯◊∞÷√C÷–«‚—ıªØƒ∆»Ð“∫µƒ◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
£®3£©B÷–Œˆ≥ˆ∫⁄…´≥¡µÌ∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
£®4£©»ÙV£Ω0£¨œ°—ŒÀ·”ÎπÃêÏ∫œŒÔN∑¥”¶∫Û»ð∆˜÷–”–πÃÃÂ≤–¡Ù£¨“™∑÷¿Î∏√πÃã¨À˘–Ë≤£¡ß“«∆˜∞¸¿®…’±≠°¢≤£¡ß∞Ù∫Õ°°°°°°°° £ª”…¥Àø…»∑∂®πÃÃÂN÷–∫¨”–µƒŒÔ÷ Œ™
°°°° °°°°°°°°°°°°°°£®ÃÓªØ—ß Ω£©°£
£®5£©»ÙV°Ÿ0£¨œ°—ŒÀ·”ÎπÃêÏ∫œŒÔN∑¥”¶∫Û»ð∆˜÷–ŒÞπÃÃÂ≤–¡Ù£¨”…¥Àø…»∑∂®πÃÃÂN÷–∫¨”–µƒŒÔ÷ Œ™°°°°°°°°°°°°°°°° £®ÃÓªØ—ß Ω£©£ª«“∆‰÷–ƒ≥“ª≥…∑÷µƒ÷ ¡ø”¶Œ™°°°°°°°°°° g£®”√¥˙ ˝ Ω±Ì æ£©°£
°°
27£Æ£®14∑÷£©
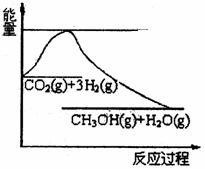
Œ™≥´µº°∞Ω⁄ƒÐºı≈≈°±∫Õ°∞µÕúæ≠º√°±£¨ΩµµÕ¥Û∆¯÷–CO2µƒ∫¨¡øº∞”––ßµÿø™∑¢¿˚”√CO2£¨ø∆—ߺ“’˝‘⁄—–æø»Á∫ŒΩ´CO2◊™ªØŒ™ø…¿˚”√µƒ◊ ‘¥°£ƒø«∞𧓵…œ”–“ª÷÷∑Ω∑® «”√CO2¿¥…˙≤˙»º¡œº◊¥º°£“ª∂®Ãıº˛œ¬∑¢…˙∑¥”¶£∫
CO2(g)+3H2(g) CH3OH(g)+H2O(g)£¨”“Õº±Ì æ∏√∑¥”¶°°
CH3OH(g)+H2O(g)£¨”“Õº±Ì æ∏√∑¥”¶°°
π˝≥Ã÷–ƒÐ¡ø£®µ•ŒªŒ™kJ·mol£≠1£©µƒ±‰ªØ£∫
£®1£©πÿ”⁄∏√∑¥”¶µƒœ¬¡–Àµ∑®÷–£¨’˝»∑µƒ «°°°°°°°° £®ÃÓ◊÷ƒ∏£©°£
A£Æ°˜H>0£¨°˜S>0°° B£Æ°˜H>0£¨°˜S<0°°
C£Æ°˜H<0£¨°˜S<0°° D£Æ°˜H<0£¨°˜S>0
£®2£©Œ™ÃΩæø∑¥”¶‘≠¿Ì£¨œ÷Ω¯––»Áœ¬ µ—È£¨‘⁄ê˝Œ™1 Lµƒ√Ð
±’»ð∆˜÷–£¨≥‰»Î1 mol CO2∫Õ3 mol H2£¨“ª∂®Ãıº˛œ¬∑¢…˙°°
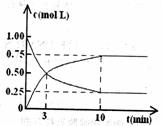 ∑¥”¶£∫CO2£®g£©+3H2£®g£©
∑¥”¶£∫CO2£®g£©+3H2£®g£© CH3OH£®g£©+H2O£®g£©£¨
CH3OH£®g£©+H2O£®g£©£¨
æ≠≤‚µ√CO2∫ÕCH3OH£®g£©µƒ≈®∂»ÀÊ ±º‰±‰ªØ»ÁÕºÀ˘ æ°£
¢Ÿ¥”∑¥”¶ø™ ºµΩ∆Ω∫‚£¨CO2µƒ∆Ωæ˘∑¥”¶ÀŸ¬
¶‘(CO2)=°°°°°°°°°°°°°°°°°°°°°° °£
°°
¢⁄∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩK=°°°°°°°°°°°°°°°°°°°°°° °£
¢€œ¬¡–¥Î ©÷–ƒÐ πªØ—ß∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂صƒ «°°°°°°
°°°° A£Æ…˝∏þŒ¬∂»°°°°°°°°°° B£ÆΩ´CH3OH(g)º∞ ±“∫ªØ≥È≥ˆ
°° °°°°C£Æ—°‘Ò∏þ–ߥþªØº¡°°°° D£Æ‘Ÿ≥‰»Îl molCO2∫Õ3 molH2
£®3£©25°Ê£¨1.01°¡105Pa ±£¨16g“∫èº◊¥ºÕÍ»´»º…’£¨µ±ª÷∏¥µΩ‘≠◊¥Ã¨ ±£¨∑≈≥ˆ369.2kJµƒ»»¡ø£¨–¥≥ˆ±Ì æº◊¥º»º…’»»µƒ»»ªØ—ß∑Ω≥Ã Ω£∫
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
£®4£©—°”√∫œ µƒ∫œΩŒ™µÁº´£¨“‘«‚—ıªØƒ∆°¢º◊¥º°¢ÀÆ°¢—ı∆¯Œ™‘≠¡œ£¨ø…“‘÷∆≥…“ª÷÷“‘º◊¥ºŒ™‘≠¡œµƒ»º¡œµÁ≥ÿ£¨¥ÀµÁ≥ÿµƒ∏∫º´”¶º”»ÎªÚÕ®»ÎµƒŒÔ÷ ”–°°°°°° °°°°°°°°°°°°£ª
∆‰’˝º´µƒµÁº´∑¥”¶ Ω «£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° .
°°
26£Æ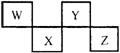 £®15∑÷£©
£®15∑÷£©
W°¢X°¢Y°¢ZÀƒ÷÷∂Ã÷Ð∆⁄‘™Àÿ‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√
»Á”“ÕºÀ˘ 棨∆‰÷–ZŒª”⁄¢˜A◊°£«Îªÿ¥œ¬¡–Œ °£
£®1£©Wµƒ‘≠◊”Ω·ππ æ“‚ÕºŒ™°°°°°°°°°°°°°°°° °£ƒÐÀµ√˜Zµƒ∑«Ω Ù–‘±»XµƒΩ Ù–‘«øµƒ ¬ µ «°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£®æŸ“ª¿˝£©°£
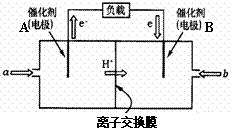 £®2£©W°¢Y∫Õ«‚ø…–Œ≥…‘≠◊”∏ˆ ˝±»Œ™1:1:4µƒªØ∫œŒÔ£¨π§“µæ∆æ´÷–∫¨”–¥ÀŒÔ÷ °£∏√ªØ∫œŒÔµƒ
£®2£©W°¢Y∫Õ«‚ø…–Œ≥…‘≠◊”∏ˆ ˝±»Œ™1:1:4µƒªØ∫œŒÔ£¨π§“µæ∆æ´÷–∫¨”–¥ÀŒÔ÷ °£∏√ªØ∫œŒÔµƒ
“ª∏ˆ÷ÿ“™◊˜”√ «”√◊˜»º¡œµÁ≥ÿ£¨»ÁÕº «2004ƒÍ≈˙¡ø
…˙≤˙µƒ“‘∏√ŒÔ÷ Œ™»º¡œµƒ»º¡œµÁ≥ÿΩ·ππ æ“‚Õº°£‘Úa
Õ®»ÎµƒŒÔ÷ Œ™°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°£¨
BµÁº´∑¥”¶ ΩŒ™°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°£
£®3£©µÁΩ‚NaZÀƻГ∫ ±£¨“ıº´µƒµÁº´∑¥”¶ Ω
Œ™°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°£
𧓵…œ£¨”√…œ ˆ∑¥”¶µƒ—Ùº´≤˙ŒÔ∫ÕCa(OH)2Œ™‘≠¡œ£¨°°
÷∆±∏∆Ø∞◊∑€∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
£®4£©“—÷™£∫298K ±£¨Ω Ùƒ∆”ÎY2∆¯ÃÂ∑¥”¶£¨…˙≥…1 mol Na2YπÃà±£¨∑≈≥ˆ»»¡ø414 kJ£ª…˙≥…1 mol Na2Y2πÃà±£¨∑≈≥ˆ»»¡ø511 kJ°£”…Na2YπÃÔÎY2∆¯ÃÂ∑¥”¶…˙≥…Na2Y2πÃõƒ»»ªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com