
3.下列叙述正确的是
A.油脂和糖类物质都能够为人体提供热量
B.青少年的生长过程需要大量蛋白质,所以要多吃水果
C.地壳中含量最多的元素是铝
D.焚烧塑料是解决“白色污染”的好办法
2.水是生命之源,既普通又宝贵。下列对水的“多”与“少”的描述错误的是
A.地球上水的总量多,淡水少
B.生活中接触的纯净水多,水溶液少
C.我国水资源总量多,人均水量少
D.“南水北调”工程说明南方水的储量多,北方水的储量少
1.在下列常见的清洗方法中,一定发生化学变化的是
A.用自来水洗手 B.用盐酸清洗铁锈
C.用汽油清洗油污 D.用洗涤济清洗餐具
31.现有10g某种钾肥样品,其成分为碳酸钾、硫酸钾及少量不含钾元素的难溶性杂质。为测定该钾肥样品中钾元素的质量分数,过程如下:
[反应原理]
K2
CO3 + H2SO4==K2
SO4 +H2O+O2
[方法及数据]
①将10g该钾肥样品溶于水,过滤出难溶性杂质,得到滤液。
②将溶质质量分数为20%的硫酸溶液逐滴加入到滤液中,至恰好完全反应。测得消耗硫酸溶液的质量为24.5g。
③将反应后的溶液蒸干,称量所得白色固体质量为11.29。
[数据处理]
根据实验数据计算(整个过程的损失忽略不计;计算结果精确到0.1):
(1)样品中碳酸钾的质量。
(2)样品中钾元素的质量分数。
30.图l4-12所示是药品标签上的说明,请完成下列问题:
(1)10片胃泰888含氢氧化镁 g。
(2)5片胃泰888含镁 g。
(3)胃病患者每天服用胃泰888中,所含氢氧化镁最少是 g。

29.某研究性学习小组在综合实践活动中对某化工厂化验室排出的废水感兴趣,并对其进行了探究:
[调查获悉]废水中含有硝酸亚铁、硝酸银
[查阅资料]含硝酸亚铁的溶液呈浅绿色
[实验目的]探究用锌从废水中最大程度地回收金属银的方法;探究锌和废水中硝酸亚铁、硝酸银的反应顺序
[实验用品]废水、所需化学试剂及相关的仪器、用品
[设计方案]他们设计了如图14-11所示方案:
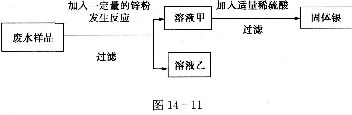
[发现问题]小组成员分别进行实验,在得到固体甲的同时发现:有些同学得到无色溶液乙,有些同学得到深浅不同的浅绿色溶液乙。小丹同学提出问题:哪种结果能最大程度地回收金属银呢?锌与废水中哪种物质先反应呢?
[讨论分析]小军同学认为:这个问题必须通过探究溶液乙或固体甲的组成才能回答,此观点得到了大家的赞同,经研究,他们决定探究溶液乙。于是他们分成两个小组,第一组对无色溶液进行探究,第二组对浅绿色溶液进行探究:
(1)首先他们对溶液乙中的溶质作出了多种猜想:
第一组:①溶质为Zn(NO3)2,②溶质为Zn(NO3)2、Ag NO3。
第二组:③溶质为Fe(NO3)2和 ,④溶质为Fe(NO3)2和
(2)小悦同学思考后指出:“通过实验或推理,都能排除第一组同学提出的猜想②,从而确立猜想①是合理的”,请你叙述其推理过程:
(3)第二组同学经过向不同的浅绿色溶液中加入一种试剂,观察实验现象后得出结论,使③④两种猜想都得以验证。请你参与到实验操作过程中并完成下表:
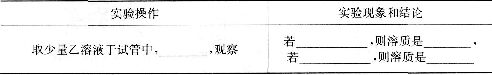
[交流后得出结论]
(4)当反应后溶液呈无色,溶质为 或当反应后溶液呈浅绿色,溶质为 和 时,能最大程度地回收金属银。通过探究,同学们认为:“使用过量的锌,过滤后得无色溶液”是方便、快捷并确保最大程度地回收金属银的一种方法。经过观察和思考,同学们还得出了Zn先和废水中 反应,再和 反应的结论。
[探究后反思]
(5)老师评价:这种方法虽然方便、快捷,但也有不足,请你指出它的不足:
28.根据实验示意图l4-10回答相关问题:
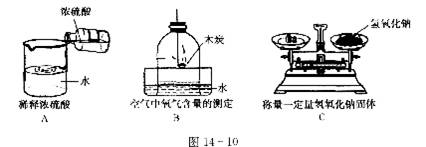
(1)图A中的操作错误是 。
(2)用图8的方法测定空气中氧气的体积分数结果偏低,其原因是 ,改进的措施是___________________________________________________________________________
(3)图C称量氢氧化钠固体的方法有 处错误。
27.(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、制得精盐。
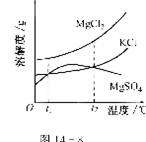
(2)晒盐后得到的卤水中含有Mg Cl2、KCl和Mg SO4等物质,图14-8是它们的溶解度曲线示意图。
①设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为以a、b、c则它们的大小关系为 。
②将卤水加热到t2℃以上,根据溶解度曲线,首先析出的晶体是 。
(3)目前世界上60%的镁是从海水中提取的。其主要步骤如图l4-9所示:
①提取Mg的过程中,试剂A可以选用 ,试剂B选用 ,由无水Mg Cl2制取Mg的反应类型为 。
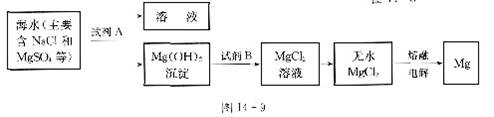
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2 CO3溶液,过滤,再向滤液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去 ;加入过量Na2CO3溶液的目的是 。
(4)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是 。海底矿产资源“可燃冰”,其主要成分是水合甲烷晶体(CH4·nH2O),若水合甲烷晶体中CH4的质量分数为l0%,则水合甲烷晶体的化学式为 。
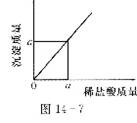
26.向溶质的质量分数为l7%的硝酸银中逐滴滴人稀盐酸,测得滴人稀盐酸与生成氯化银沉淀的质量关系如图l4-7所示,则恰好完全反应时所得溶液中溶质的质量分数为 。
25.有一种白色固体A可能由CuCl2、Na2CO3、NaCl、Ba(OH)2、Ba(NO3)2、K2 SO4中的两种或几种组成,取少量A做如下实验,主要现象如图l4-6所示,请用化学式填空:
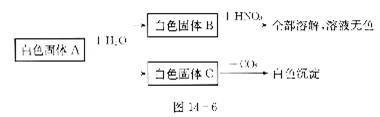
(1)白色沉淀B是 。
(2)A中肯定不存在的物质是 。
(3)A可能的组成是(只要求写出三组):① ; ② ;③ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com