
5.某学生做乙醛的还原性实验时,取1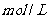 CuSO4溶液和0.5
CuSO4溶液和0.5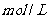 NaOH溶液各2mL,在一支洁净的试管内混合后,向其中加入1mL40%的乙醛溶液,加热煮沸。请你判断实验结果
NaOH溶液各2mL,在一支洁净的试管内混合后,向其中加入1mL40%的乙醛溶液,加热煮沸。请你判断实验结果
A.无红色沉淀
B.有红色沉淀
C.无沉淀
D.有白色沉淀
4.某学生用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收设计了如图的装置,则对装置内溶液的主要成分判断正确的是

A.NaOH 和NaCl
B.HClO和NaCl
C.HClO和HCl
D.NaClO和NaCl
3.下列表达式正确的是
A.甲基的电子式可写为: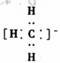
B.乙烯的结构式为:CH2CH2
C.乙醛的结构简式可写为:CH3COH
D.乙炔的最简式为:CH
2.下列说法正确的是
A.高分子分离膜可以分离任何物质
B.玻璃钢是玻璃与钢混和熔制而成的
C.到现在为止,尚未造出能导电的塑料
D.塑料通常是由树脂及各种助剂组成的
1.保护环境越来越受到人们的重视。某研究性小组在讨论回收废电池的原因时有以下几条,你认为正确的是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其它物品
D.回收其中石墨电极
0.01molA 盐C 盐D
①光谱测定显示:A分子结构中不存在甲基,A的结构简式为____________;
②B是A的同分异构体,它是苯的某种同系物经硝化反应后的惟一产物,B的结构简式为_________。
33.(8分)[化学-有机化学基础]
质子核磁共振谱(NMR)是研究有机物结构的有力手段之一。
(1)现有分子式均为C2H4O2的两种链状分子组成的混合物,如果在NMR谱上观察到氢原子给出的信号有两种情况:第一种情况峰的强度比为3:1;第二种情况峰的强度比为2:1:1。由此推断该混合物的组成(写结构简式)是:__________或___________。
(2)A、B两种有机物均由C、H、N、O四种元素组成,且分子中都含有苯环,A是天然蛋白质的水解产物,其中含氧元素的质量分数为19.4%,A有如下转化关系(假设每步反应均完全进行):
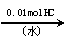
32.(8分)[化学-物质结构与性质]
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D.E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1。试回答:
(1)写出D原子的电子排布式_____________________________________。
(2)用电子式表示AE2的形成过程__________________________________。
(3)B、C两元素的第一电离能较大的元素是:_________(填写元素符号)。
(4)根据VSEPR模型预测C的氢化物的立体结构为________,中心原子C的轨道杂化类型为________。
(5)C的单质中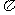 键的数目为____________,B、D两元素的气态氢化物的稳定性大小关系为:
键的数目为____________,B、D两元素的气态氢化物的稳定性大小关系为:
__________>_________(填写化学式)。
31.(8分)[化学-化学与技术]
海水中镁的总储量约为2.1×15t,目前世界上的60%的镁来自海水。工业规模海水提镁的流程如图所示:
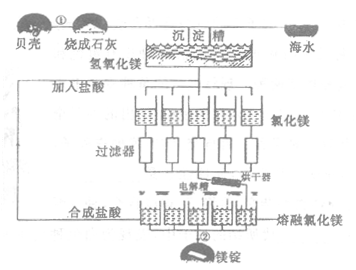

试回答下列问题:
(1)请写出海水提镁的过程中①②反应的化学方程式:①____________________________________;
②_________________________________________。
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为:
____________________________________________.
(3)工业上制取金属铝时不用电解AlCl3的方法而是用电解熔融Al2O3的方法,试解释铝电解槽中的阳极碳块为何要定期更换?__________________________________________。
30.(14分)下图为某些常见物质之间的转化关系。已知A为有色气体单质,
反应②是实验室制取气体F的常用方法。
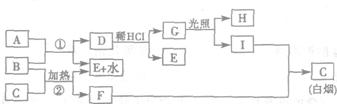
请按要求填空:
(1)E的电子式是__________,B中含有的化学键类型有__________________;
(2)反应②的化学方程式是___________________________________________;
(3)反应①在工业上有重要的用途,其化学方程式是________________________________________.
(4)取一试管A气体倒置于水槽中光照足够长的时间,(假设溶质不扩散到试管外,气体体积按标准状况下计算)所得溶液的物质的量浓度为____________。
(5)G为一元弱酸,设G的化学式为HX,常温下如果取0.1 mol·L-1HX溶液与0.1mol·L-1NaOH溶渡等体积混合(混合后溶液总体积等于两溶液体积之和),测得混合溶液的pH=8。
求出混合溶液中下列算式的精确计算结果:
c(Na+)-c(X-)=_________mol·L-1,c(OH-)-c(HX)=________mol·L-1
[选做部分]
共8个题,考生从中选择2个物理题、1个化学题和1个生物题作答。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com