
19.(8分)已知物质M由X、Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的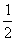 ,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
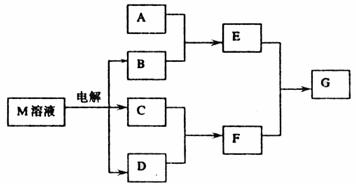
(1)若A是与X、Y同周期元素的一种常见金属单质,则A与B溶液反应的化学方程式是:
(2)若A是一种常见酸性氧化物,且可用于制造玻璃则E与F反应的离子方程式是:
(3)若A是一种常见的化肥,式量为79,且E与F反应生成G时有白烟产生,则G的电子式是
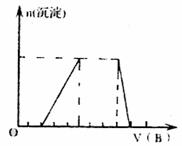
(4)若A是一种溶液,只可能含有H+、NH+4、Mg2+、Fe3+、Al3+、CO2-3、SO2-4中的某些离子,当向该溶液中加入B溶液时,发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是 。
18.金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
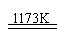 aTiO2+bCl2+cC
aTiCl4+cCO ………………反应(1)
aTiO2+bCl2+cC
aTiCl4+cCO ………………反应(1)
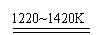 TiCl4
+ 2Mg
Ti + 2MgCl2 ………………反应(2)
TiCl4
+ 2Mg
Ti + 2MgCl2 ………………反应(2)
关于反应(1)、(2)的分析不正确的是 ( )
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂
②C、Mg在反应中均为还原剂,被还原
③在反应(1)、(2)中C的还原性大于TiCl4,Mg的还原性大于Ti
④a = 1,b = c =2
⑤每生成9.6g Ti,反应(1)、(2)中共转移0.8 mol e-
A.①②④ B.②③④ C.③④ D.②⑤
第Ⅱ卷(非选择题 共46分)
17.Cu(OH)2在水溶液中存在着如下沉淀溶解平衡:
 Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下KSP=2×10-20mol3/L3。在常温下如果要生成Cu(OH)2沉淀,需要向0.02mol/L的CuSO4溶液中加入碱溶液来调整溶液的pH,使溶液的pH大于 ( )
Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下KSP=2×10-20mol3/L3。在常温下如果要生成Cu(OH)2沉淀,需要向0.02mol/L的CuSO4溶液中加入碱溶液来调整溶液的pH,使溶液的pH大于 ( )
A.2 B.3 C.4 D.5
16. 已知可逆反应:aA(g)+bB(g) cC(g),物质的质量分数A%和C%随温度的变化曲线如图所示,下列说法正确的是
( )
已知可逆反应:aA(g)+bB(g) cC(g),物质的质量分数A%和C%随温度的变化曲线如图所示,下列说法正确的是
( )
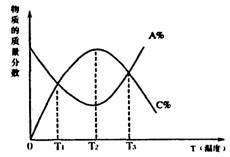
A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡向正反应方向移动
15.
 α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g) 2B(g)和2A(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是 ( )
α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g) 2B(g)和2A(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是 ( )
A.α1、α2均减小 B.α1、α2均增大
C.α1减小,α2增大 D.α1增大,α2减小
14.下列各组离子在指定溶液中一定能大量共存的是 ( )
①加入Al能放出H2的溶液中:Fe2+ Al3+ NO-3 Cl- S2-
②在pH=11的溶液中:Na+ AlO-3 NO3 -S2- SO2-3
③由水电离的c(H+)=10-12mol·L-1的溶液中:Cl- HCO-3 NO-3 NH+4 F-
④加入Mg能放出H2的溶液中:Mg2+ NH+4 Cl- K+ SO2-4
⑤使甲基橙变红的溶液中:Fe3+ NH+4 Cl- K+ SO2-4
A.①③④ B.①②④ C.②④⑤ D.①②⑤
13.25℃时,在20mL 0.1 mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是 ( )
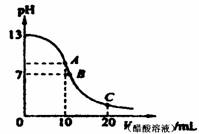
A.在A点:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
B.在B点:c(OH-) === c(H+), c(Na+) === c(CH3COO-)
C.在C点:c(CH3COO-) > c(Na+) > c(H+) > c(OH-)
D.在D点:c(CH3COO-) +c(CH3COOH) === 2c(Na+)
12.下列说法或表示法正确的是 ( )
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)=C(金刚石);△H=+1.90kJ·mol-1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ·mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.5kJ热量,氢气燃烧的热化学方程式表示为:2H2(g) + O2(g) ==== 2H2O(l);△H=-285.8kJ·mol-1
11.类推的思维方式在化学学习与研究中是经常用到的,但是有时会产生错误的结论,因此类推出的结论最终要经过实践的验证才能决定其正确与否。以下类推的结论正确的是
( )
A.Na、Mg、Al具有强还原性,Na常温下与水剧烈反应,故Mg、Al也是
B.盐酸、硝酸都是强酸,CaCO3与盐酸反应制取CO2,用硝酸也行
C.由2Fe+3Cl2=2FeCl3可推出2Fe+3I2=2FeI3成立
D.CO2和SO2都是酸性氧化物,SO2能使酸性KMnO4溶液褪色,故CO2也是
10.A、B、C短周期元素在周期表中的相对位置如图所示,已知A、C可分别与B形成化合物x和y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合是 ( )
①B与C均存在同素异形体
②x的种类比y的多
③常温上,在10mL B的氢化物中无H+
④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
A.①②③④ B.②③ C.①②④ D.①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com