
18.(10分)A、B、C、D为短周期内除稀有气体外的元素,它们的原子序数依次增大。四种元素中只有C为金属元素;A和C的最外层电子数相等;B、D属于同主族;C、D两元素原子的质子数之和为A、B两元素原子的质子数之和的3倍。请回答下列问题:
(1)A的元素符号为 ,B的原子结构示意图是 。
(2)C2B2中含有的化学键是 ,写出C2B2与A2B反应的离子方程式 。
(3)比较A、B、C、D离子半径由大到小的顺序为(用离子符合表示) 。
(4)用化学方程式证明元素原子的得电子能力B强于D 。
17.(6分)如图,在锥形瓶中按①②③④的顺序依次加入试剂后,立刻离开。可以观察到,大量的蓝色泡沫成柱状冲出锥形瓶,然后有白色泡沫迅速从锥形瓶口逸出,飞舞盘旋,并有大量水蒸气冒出。用手触摸锥形瓶,感觉比较烫。
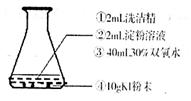
(1)开始冲出的泡沫呈蓝色,说明上述反应中生成了单质碘。试写出KI与H2O2反应生成碘的离子方程式 。
(2)已知1mol液态H2O2分解生成液态水和氧气,放出98.64kJ的热量。写出该反应的热化学方程式 。
(3)上述实验中KI粉末用KMnO4粉末代替,也可产生类似现象。在H2O2分别与这两种物质反应时,表现的性质有什么不同? 。
16.三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。在潮湿的空气中。NF3能与水蒸气发生氧化还原反应,其反应的产物有HF、NO和HNO3。下列说法正确的是( )
A.在NF3与H2O的反应中,H2O作还原剂
B.在制取NF3的反应中,氧化剂与还原剂的物质的量之比为3:1
C.若在制取NF3的反应中有0.5molNH3参加反应,转移电子的物质的量为3mol
D.NF3在空气中一旦泄漏,不易于发现
|
15.已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,测得放出热量ak J。又知道12.0g炭完全燃烧,放出热量为bk J。则热化学方程式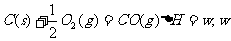 等于
等于
( )
A.-(a-b)kJ·mol-1 B.-(a+b)kJ·mol-1
C.-(5a-0.5b)kJ·mol-1 D.-(10a-b)kJ·mol-1
14.有以下七种饱和溶液:①Ba(NO3)2②Ca(OH)2③Ca(C1O)2④CaC12⑤Na2CO3⑥Na[A1(OH)4],分别持续通入CO2,最终能得到沉淀或析出晶体的是 ( )
A.②⑥ B.①③⑤ C.⑤⑥ D.④⑥
13.NA代表阿伏加德罗常数的值。下列说法中正确的是 ( )
A.1.0L0.10mol·L-1Ba(OH)2溶液中Ba2+的个数是0.10NA
B.反应2C+SiO2 Si+2CO↑,当生成14g硅时,转移电子总数是0.5NA
Si+2CO↑,当生成14g硅时,转移电子总数是0.5NA
C.1mol液态N2O4中原子总数小于NA
D.1molH2与1molC12混合后完全反应,体系中的原子总数为2NA
12.下列溶液中离子可能大量共存的是 ( )
A.含有大量Fe2+的溶液中:HCO3-、Na+、NO3-、C1-
B.酸性溶液中:Na+、K+、C1O-、[A1(OH)4]-
C.由水电离的c(OH-)=10-14mol·L-1的溶液中:CH3COO-、CO32-、Na+、K+
D.加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、C1-、Mg2+
11.化学实验室中常将溶液或试剂进行酸化,下列酸化处理合理的是 ( )
A.配制氯化铝溶液时,为防止其水解加入稀硫酸酸化
B.为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化
C.检验溶液中是否有Fe2+时,用硝酸酸化,再加KSCN溶液
D.用氯化钡溶液鉴别溶液中是否有SO42-时,溶液可用盐酸酸化
9.下列叙述正确的是 ( )
A.同一主族的元素,原子半径越大,其单质的氧化性越强
B.断裂化学键一定吸收能量
C.位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则这两种离子的半径一定是X>Y
D.将pH=2,体积相同的盐酸和醋酸溶液均稀释100倍后,分别加入足量的颗粒大小相同的锌,产生H2的起始速率相同,醋酸放出的氢气多
|
A.自然界中不存在游离态的硫
B.二氧化硫的排放会导致光化学烟雾的产生
C.二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
D.浓硫酸可用来干燥SO2、CO、C12等气体
8.下列说法正确的是 ( )
A.由于胶体的胶粒带电荷,所以能发生丁达尔现象
B.KHSO4只有在电流作用下才能电离成K+、H+和SO42-
C.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
D.碳酸氢钙溶液加入过量石灰水反应的化学方程式是
Ca(HCO3)2+Ca(OH)2=2CaCO3↓+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com